可能很多人有过这样的经历:辛辛苦苦减掉了十几斤,可一旦稍微放松饮食控制,体重就像坐了过山车一样迅速反弹。
过去,我们常常将这种现象归咎于“意志力不够坚定”或“管不住嘴”。然而,来自英国、爱尔兰、意大利等多国高校的研究团队发表于EMBO Reports的一项最新研究发现,肥胖会在免疫细胞上留下表观遗传记忆,即使体重已经恢复正常,这些细胞仍然记得自己曾经“胖过”,并持续推动着炎症反应,让人更难维持健康状态。

DOI:10.1038/s44319-026-00765-w
减肥成功后,免疫系统没有同步恢复
研究团队首先将4周大的雌性小鼠分为如下几组:对照组一直吃正常饮食,肥胖组一直吃高脂饮食,还有几组作为“恢复组”,先吃8周高脂饮食诱导肥胖,然后换回正常饮食,分别恢复6周或12周。
结果,在恢复正常饮食6周的小鼠中,虽然它们的体重已经回落,腹部脂肪也显著减少,但它们的CD4+效应记忆T细胞(Tem)却依然保持着肥胖组那种“易燃易爆炸”的炎症状态。这些细胞的表面高表达CXCR3和LFA1这两个与炎症反应相关的分子。
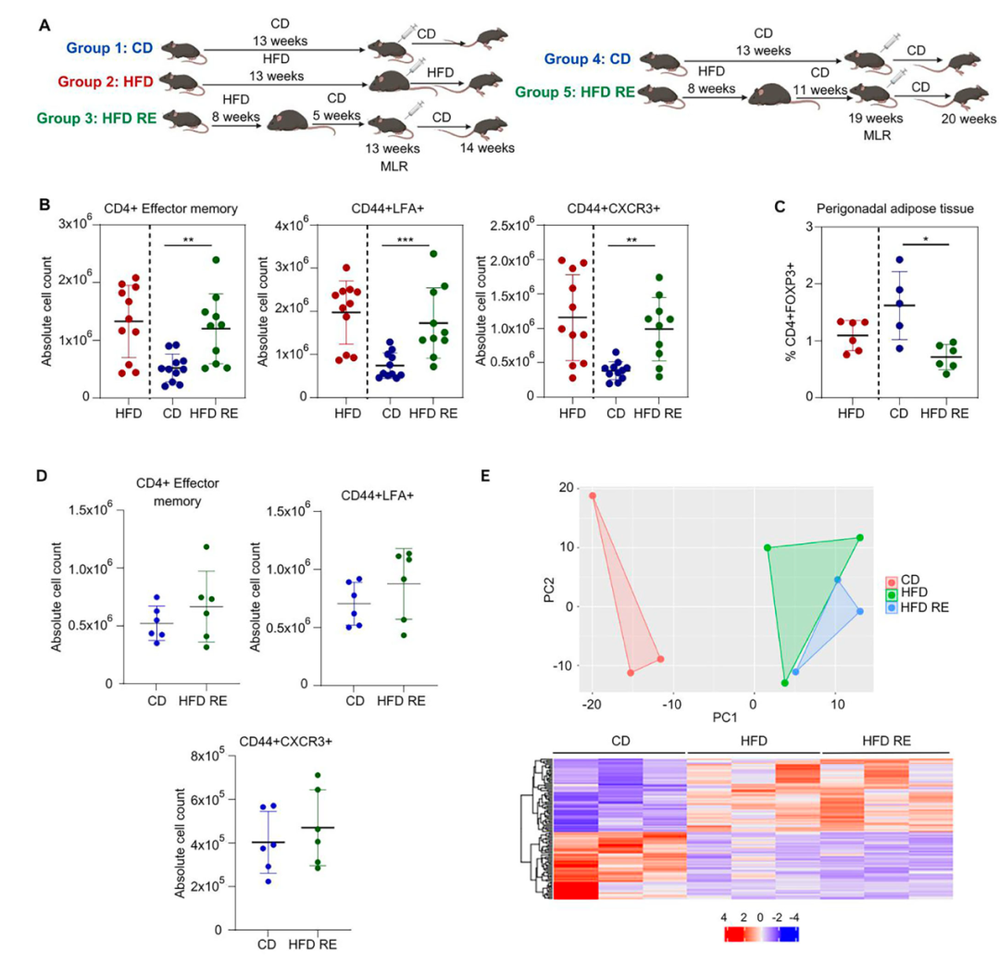
体重下降后,促炎效应记忆T细胞(Tem)无法轻易恢复到稳态
不过,这种“免疫记忆”并非是永久性的。当恢复正常饮食到12周时,Tem的反应逐渐恢复了正常。换算一下,这段“免疫遗忘”的时间跨度,大约相当于人类的5-10年。
这也意味着,哪怕减肥成功,免疫系统可能还需要将近十年的时间,才能真正摆脱肥胖曾经带来的影响。这期间,我们依然处于一种低度的慢性炎症状态,更容易受到代谢性疾病的侵扰,也更可能在体重的拉锯战中败下阵来。
三个人类队列验证
这些结论究竟是否适用于人类呢?于是,研究者又招募了三组不同特征的人类受试者,进行了验证。
第一组是接受了GLP-1受体激动剂司美格鲁肽治疗的肥胖患者。这些患者的平均BMI高达45.4 kg/m²,属于重度肥胖。在用药6个月后,他们的体重和BMI都出现了显著的下降。然而,他们外周血中Tem细胞的比例和炎症表型并没有因为体重的下降而发生而发生显著改变。
第二组是Alström综合征患者。这是一种罕见的常染色体隐性遗传病,患者会早发肥胖和严重的胰岛素抵抗。与健康对照组相比,这些患者的血液中Tem细胞的比例显著升高。
第三组是一项随机对照运动试验的参与者。他们进行了为期10周的结构化运动训练,但运动并未显著改变他们的体重、BMI或体脂率。并且,在没有减重的情况下,单纯的运动没有对脂肪组织和血液中的Tem细胞产生显著影响。
也就是说,无论是药物减重、运动锻炼,还是先天代谢异常,只要肥胖的状态曾经存在,T细胞似乎就“记住了”这一切,不会因为体重的短期正常化而轻易改变自己的行为模式。
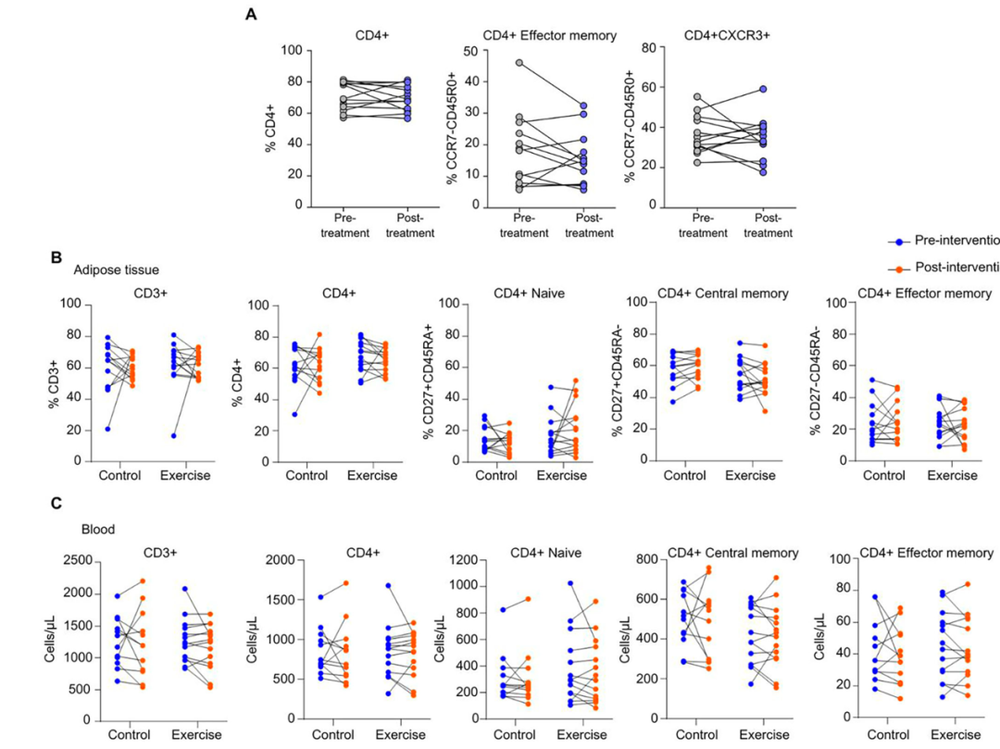
司美格鲁肽减重和运动干预,都未能让肥胖患者的促炎效应记忆T细胞恢复稳态
甲基化锁住肥胖记忆
这种顽固的“免疫记忆”到底是如何形成的?
进一步的分析指向了表观遗传调控,尤其是DNA甲基化这一类“分子开关”。研究者对不同状态下的CD4+ T细胞进行了全基因组扫描,他们发现:即使体重已经恢复正常,记忆T细胞的甲基化模式,依然更接近肥胖时期。
顺着这条线索往下,他们锁定了一部分处于低甲基化状态,更容易被持续激活的基因。STK26就在其中,它相当于调控自噬的“油门”。当STK26表达上调时,会通过调节相关蛋白促进自噬过程持续活跃,让细胞维持在一种更“敏感”的反应状态。
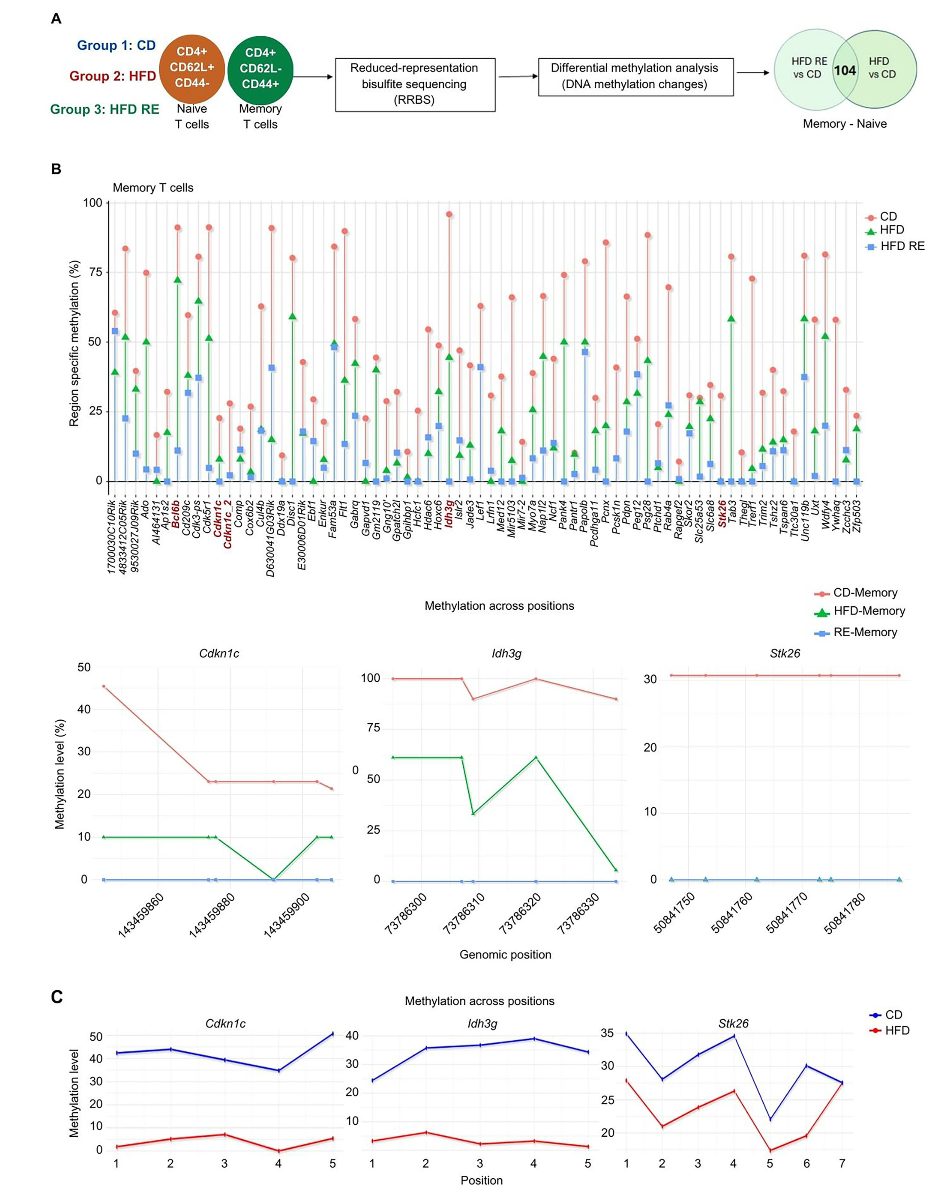
肥胖通过DNA甲基化修饰,给CD4⁺记忆T细胞打上“持久印记”
为了验证STK26是不是这一切的“罪魁祸首”,研究团队构建了STK26基因敲除小鼠。当这些小鼠被喂食高脂饮食时,与正常小鼠相比,它们的炎症性CD4+ T细胞的扩增被显著抑制了。
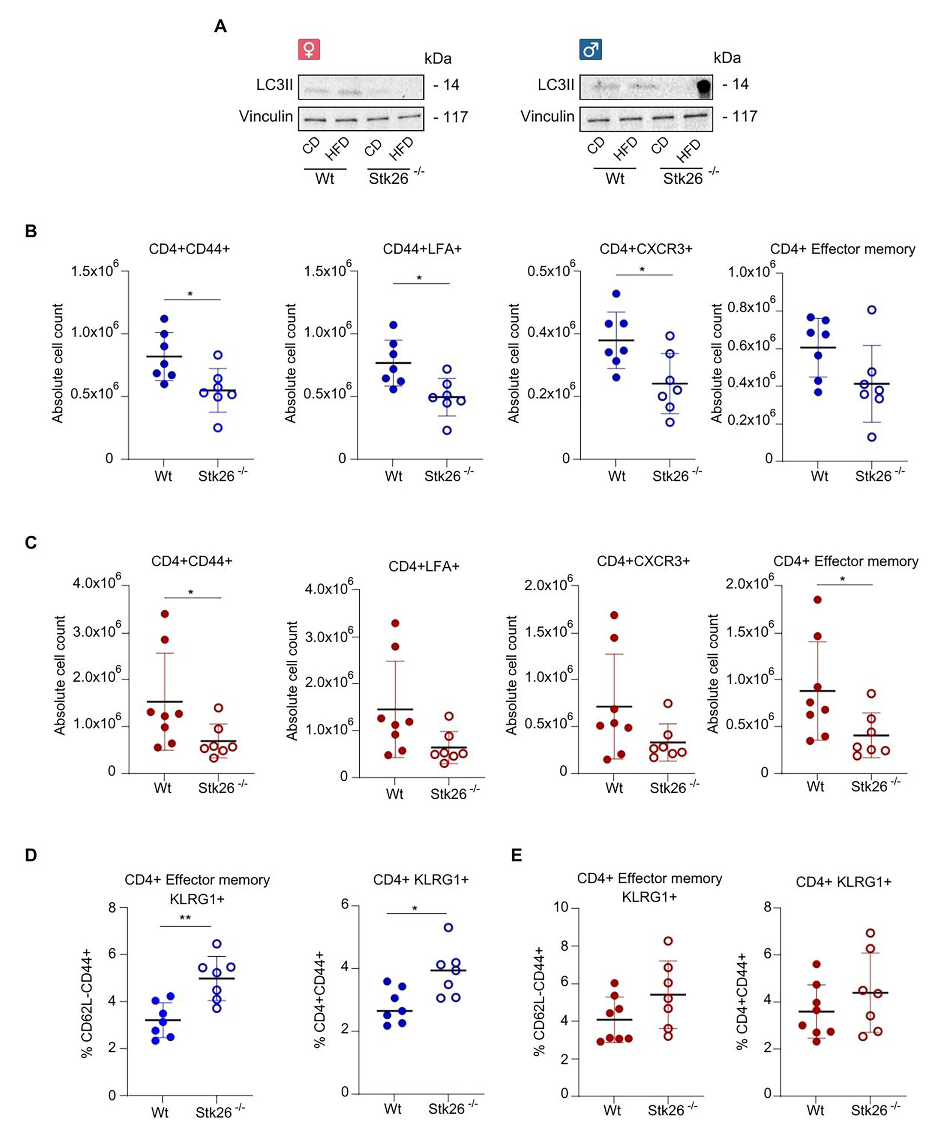
STK26是肥胖诱导促炎效应记忆T细胞(Tem)扩增和自噬激活的核心调控因子
从机制上来说,肥胖状态下升高的饱和脂肪酸,尤其是棕榈酸,会改变CD4⁺ T细胞膜的生物物理特性,进而引发全基因组范围的DNA甲基化异常。与此同时,棕榈酸所激活的异常T细胞还会反过来影响代谢过程,促进脂肪生成并干扰胰岛素信号通路,使机体逐渐进入免疫与代谢相互扰动的状态。最终,这种长期的双向影响会导致免疫稳态恢复显著滞后,成为体重易反弹的重要分子机制之一。
总体而言,上述研究解释了为什么减肥如此难以维持,为什么“易胖体质”可能真的存在。原来,免疫细胞可能记得我们曾经的放纵,并且在长达数年的时间里持续“报复”代谢健康。那些经历了减肥-复胖循环的人,并不是意志力薄弱,而是他们的免疫系统深处,有一道短期内无法抹去的“疤痕”。
当然,这道疤痕并非完全不可逆转。研究者发现的 STK26这一关键分子,也为未来的药物干预提供了极具潜力的靶点。
注:上述研究缺乏减重5-10年的人类长期随访队列,分析主要基于小鼠模型,在人类中的普适性仍需进一步验证。
[1]Niven, J., Kucuk, S., Gope, A. et al. DNA methylation-mediated memory of obesity in CD4 T lymphocytes perpetuates immune dysregulation. EMBO Rep (2026). https://doi.org/10.1038/s44319-026-00765-w
