在对抗癌症的免疫战争中,树突状细胞(DC)扮演着至关重要的“教官”角色。它们负责捕捉肿瘤抗原,“训练”并激活杀伤性T细胞,是癌症疫苗设计的核心。然而,DC疫苗的临床疗效常不尽如人意,一个根本原因在于肿瘤微环境会抑制DC的“教学”能力。

意外发现:
乳腺癌靶点ERα的“第二职业”
研究团队利用CRISPR/Cas9基因编辑技术,对DC进行了全基因组筛选,旨在找出那些调控抗原“交叉呈递”能力的关键基因(交叉呈递是DC激活CD8⁺ T细胞的核心步骤)。结果令人惊讶:雌激素受体α被鉴定为最强的负向调控因子之一。这意味着,在DC内部,ERα的存在会主动抑制其向免疫系统“展示”肿瘤抗原的能力。
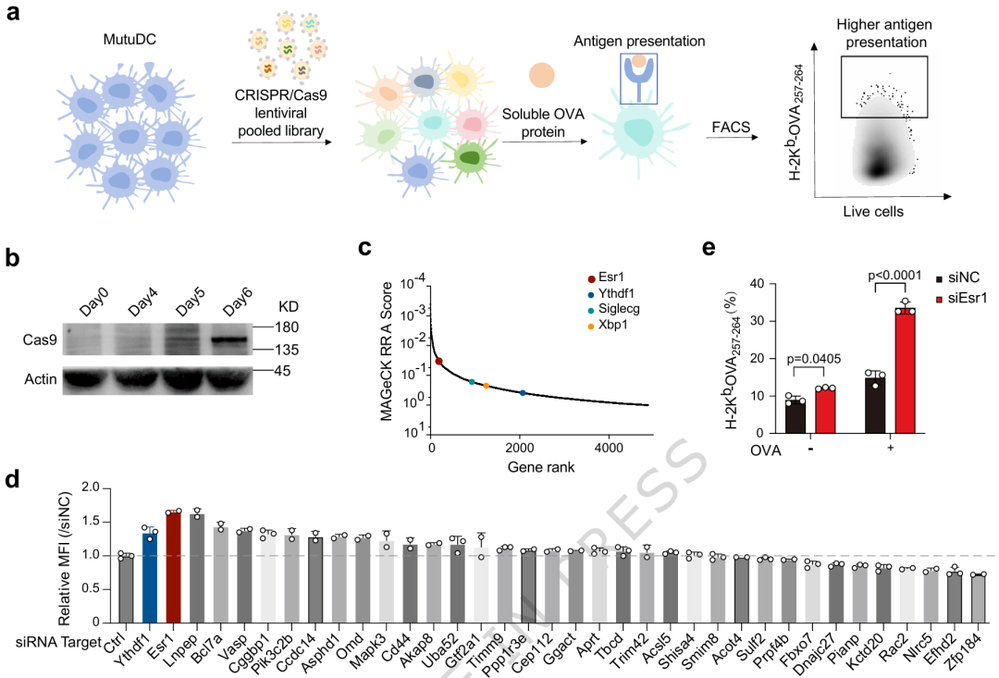
ERα 是 cDC1 抗原呈递过程中的负调控因子(图源自Nature Communications )
新颖机制:不依赖激素的“密封”作用
ERα如何发挥抑制作用?研究发现,这一过程完全独立于其经典的雌激素信号功能。机制研究表明,ERα通过调控一个名为半乳糖凝集素-3的蛋白,来维持ESCRT-III膜修复复合物在吞噬体(即DC吞入抗原的“包裹”)上的活性。这好比给吞噬体过度“封箱”,修复了其正常破损,导致抗原难以从“包裹”中泄漏至细胞质,从而无法进入后续的交叉呈递通路。
当敲除DC的ERα基因或使用药物诱导其降解后,吞噬体膜修复减弱,抗原更易泄漏,DC的抗原呈递和T细胞激活能力因此得到显著增强。
治疗验证:“老药新用”赋能癌症疫苗
这一基础发现指向了清晰的转化医学前景。在多种小鼠肿瘤模型中,研究人员制备了ERα缺陷的DC疫苗。结果显示,这种疫苗能激发更强、更多的肿瘤特异性CD8⁺ T细胞,并显著抑制肿瘤生长,效果远超传统DC疫苗。
更具临床意义的是,研究证实,已获批用于乳腺癌治疗的ERα抑制剂,同样能在体外有效增强人类DC的抗原呈递能力及其激活人类CD8⁺ T细胞的效果。这为“老药新用”快速转化提供了直接依据。
总结与展望
这项研究具有多重意义:
发现新靶点:首次将ERα定义为DC抗原交叉呈递的内在检查点,拓展了对其生物学功能的理解。
阐明新机制:揭示了ERα通过非经典信号通路调控吞噬体完整性的全新功能。
提供新策略:提出了通过靶向DC内的ERα(例如使用现有药物)来“松绑”DC功能,从而优化DC疫苗及其他T细胞免疫疗法的创新策略。
总之,该研究不仅破解了DC功能受抑的一个关键机制,更找到了一条能迅速衔接现有药物与新型免疫疗法的捷径,为攻克癌症疫苗疗效瓶颈带来了充满希望的新方向。
参考消息:https://www.nature.com/articles/s41467-026-72647-7
