癌症几乎能侵袭人体的每一个器官,从肺、肝、胃肠到骨骼、大脑,恶性肿瘤的踪迹几乎无处不在,却唯独对心脏“敬而远之”。
临床数据显示,原发性心脏肿瘤在尸检中的发生率仅为0.001%-0.03%,即便是恶性程度极高、极易发生全身转移的肿瘤,出现心脏转移的概率也远低于肝、肺、骨骼等器官。
这一现象让医学界困惑了近百年:心脏是人体血液循环的核心泵体,每分钟接收约全身5%的血液,源源不断的血流本应让循环中的癌细胞极易在此“登陆定植”,究竟是什么让心脏成为了癌细胞难以攻克的“抗癌堡垒”?
近日,发表在国际顶级期刊Science上题为“Mechanical load inhibits cancer growth in mouse and human hearts”的研究中,来自意大利国际遗传工程和生物技术中心、的里雅斯特大学等机构的科学家团队,终于揭开了这一谜题的答案:心脏永不停歇的跳动所产生的机械负荷,正是其抑制肿瘤生长的核心秘密。
这项研究不仅首次完整阐释了心脏罕见癌变的底层机制,更开辟了基于机械力干预的癌症治疗全新方向。

研究团队首先通过体内基因编辑模型,直接证实了心脏对癌变有着与生俱来的强大抵抗力。他们向7只LSL-K-RasG12D/+;p53f/f基因工程小鼠体内,静脉注射了表达Cre重组酶的AAV9病毒,通过基因重组同时激活致癌基因K-Ras突变、敲除抑癌基因p53——这两种是人类癌症中最常见的致癌驱动事件,足以在多个组织中诱发恶性肿瘤。
2个月后的检测结果显示,小鼠的肝脏、骨骼肌、心脏中发生了同等程度的基因重组,最终在四肢、躯干、颈部等部位的骨骼肌中形成了多例横纹肌肉瘤,却在心脏中未发现任何肿瘤形成的迹象。
这一结果直接推翻了“心脏只是没接触到致癌信号才幸免”的猜想,证明心脏内部存在着一套主动抑制癌细胞增殖的防御机制。
为了锁定这套防御机制的核心,研究人员设计了一套堪称精妙的体内外实验体系,精准验证机械负荷在其中的关键作用。
在体内实验中,他们建立了小鼠颈部异位心脏移植模型:将供体小鼠的心脏取出,把主动脉和肺动脉分别与受体小鼠的颈动脉、颈外静脉进行吻合,这样一来,移植的心脏虽然恢复了冠脉灌注,心肌细胞能得到充足的氧气和营养,却完全摆脱了正常心脏收缩射血所需承受的机械负荷,成为一个“机械卸载”的活体心脏。
超声心动图验证显示,与受体小鼠自身正常跳动的负荷心脏相比,移植的卸载心脏左室的心肌应变、收缩位移、纵向应变率等核心力学参数均出现了显著下降,同时还观察到卸载后的心肌细胞重新进入了细胞周期,出现了明显的增殖现象,这与临床中终末期心衰患者植入左心室辅助装置(LVAD)后,心肌卸载伴随增殖能力恢复的现象完全一致,完美复刻了心脏机械负荷的生理调控效应。
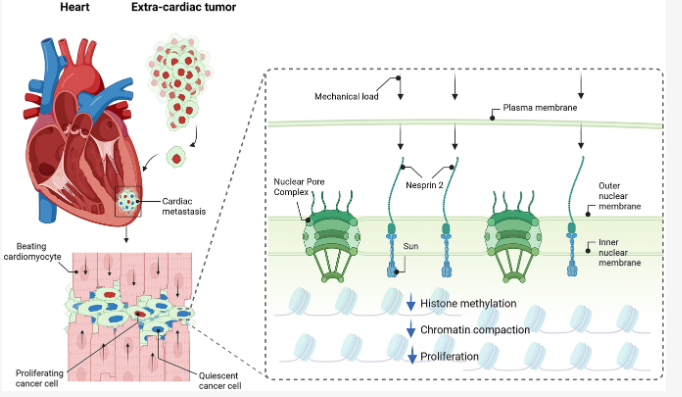
心脏中抑制癌细胞增殖的关键机制
与此同时,研究团队还构建了可精准调控力学环境的体外工程化心脏组织(EHT),这套体系由新生大鼠心肌细胞和成纤维细胞构建而成,能通过金属支架自主调节组织所承受的机械负荷,同时还能通过培养基钙浓度控制心肌的搏动状态,实现静态无负荷与生理搏动负荷的精准切换。
体内外两套模型的实验结果高度一致,给出了无可辩驳的结论:生理水平的机械负荷,能显著抑制肺癌、结肠癌、黑色素瘤细胞在心肌组织内的增殖,而一旦心肌组织的机械负荷被卸载,这些原本在心脏中难以生长的癌细胞,便会开启疯狂的增殖模式。
在体内异位心脏移植模型中,研究人员向负荷心脏与卸载心脏的左心室心肌内,分别注射了1×105个稳定表达绿色荧光蛋白(GFP)的肺癌细胞。结果显示,注射后第3天,两组心脏内的癌细胞定植数量完全一致,且通过 TUNEL、cleaved Caspase 3、RIP3染色检测,两组的癌细胞凋亡、坏死水平没有任何差异,彻底排除了“癌细胞在正常心脏中更容易死亡”的可能性。
但到了注射后第14天,两组的肿瘤生长出现了天壤之别:正常负荷的心脏中,癌细胞仅能零星生长,占据的左室面积极少超过20%;而卸载的心脏中,癌细胞已大规模浸润增殖,几乎完全替代了正常的心肌组织,Ki67、pHH3等增殖标志物阳性的癌细胞数量,是负荷心脏组的2倍以上。
体外工程化心脏组织的实验,进一步完善了这一结论。研究人员通过支架调节,将EHT分为正常负荷、卸载、过负荷三组,结果显示,卸载组的癌细胞增殖水平显著升高,而过负荷组的癌细胞增殖则被完全抑制。
在另一组实验中,研究人员通过钙剥夺让EHT停止搏动,与正常搏动的EHT形成对照,结果同样令人震撼:静态无搏动的EHT中,癌细胞均匀分布、大量增殖,占据了组织的绝大部分区域;而正常搏动的EHT中,癌细胞仅能分布在组织外层的低压力区域,在静水压力更高的组织中心,几乎看不到癌细胞的踪迹。
通过数学建模模拟,研究人员证实,EHT在搏动收缩时,组织中心会产生更高的静水压缩力,而癌细胞的分布密度,恰好与压力梯度呈完美的负相关。更关键的是,研究团队通过一系列实验彻底排除了“营养竞争”的干扰:无论是搏动还是静态EHT的培养上清,对癌细胞的增殖都没有影响;与心肌细胞共培养时,即便以180次/分钟的频率起搏心肌细胞,也不会因营养消耗抑制癌细胞增殖,直接证明了机械负荷才是抑制癌细胞生长的唯一核心因素。
那么,心脏的机械跳动,究竟是如何把癌细胞的增殖“牢牢按住”的?
研究人员结合人类临床样本与多组学技术,完整拆解了这一机械信号转化为抗癌效应的分子通路。他们收集了肺腺癌、结肠癌、皮肤黑色素瘤三种不同原发肿瘤患者的样本,这些患者均同时出现了心脏转移与心外器官转移,通过GeoMX空间转录组学技术,精准捕获并对比了同一患者体内,心脏转移灶与心外原发灶、转移灶中癌细胞的转录组特征。
结果发现,无论原发肿瘤来自哪个器官、属于哪种病理类型,心脏转移灶中的癌细胞都共享一套高度一致的转录特征,其中上调最显著的基因通路,便是组蛋白去甲基化,多个靶向组蛋白H3第9位赖氨酸的去甲基化酶(KDM4C、KDM4D)均出现了显著高表达。
与之相对应的是,心脏转移灶癌细胞的组蛋白H3第9位赖氨酸三甲基化(H3K9me3)水平,显著低于心外肿瘤。H3K9me3是异染色质形成的核心表观遗传标记,其水平直接决定了染色质的压缩程度:H3K9me3水平越高,染色质压缩越紧密,相关基因的转录就越难启动;反之,H3K9me3水平降低,染色质会发生去压缩,基因组的“包装方式”会发生彻底改变。
研究人员通过单细胞核转座酶可及性染色质测序(snATAC-seq)与染色质免疫共沉淀测序(ChIP-seq)进一步证实,在机械负荷的作用下,癌细胞的染色质可及性发生了全局性改变:与细胞周期停滞、机械感知、细胞骨架重塑相关的基因位点可及性显著升高,而驱动癌细胞增殖、癌症代谢、去分化的核心基因位点可及性则显著降低。
简单来说,心脏的机械力通过改变癌细胞基因组的“包装结构”,直接关闭了癌细胞的增殖开关,把它们“锁”在了无法分裂的状态。
为了验证这一机制的因果关系,研究人员在癌细胞中沉默了上调最显著的KDM4C和KDM4D,结果发现,癌细胞的H3K9me3水平显著回升,即便在正常搏动的工程化心脏组织中,也重新恢复了大规模增殖的能力,直接证明了组蛋白去甲基化与染色质重塑,是机械负荷抑制癌细胞增殖的核心环节。
而在整个机械信号的传导过程中,一个名为Nesprin-2的蛋白,扮演了无可替代的 “核心开关” 角色。Nesprin-2 是核骨架与细胞骨架连接子(LINC)复合物的核心组成部分,它就像一座横跨细胞质与细胞核的“桥梁”,能直接将细胞外的机械力信号传递到细胞核内部,是细胞中最重要的机械传感器之一。
研究人员在肺癌、结肠癌、黑色素瘤细胞中,分别沉默了编码Nesprin-2的Syne2基因,结果发现,失去Nesprin-2的癌细胞,完全丧失了对机械负荷的感知能力:在正常搏动的工程化心脏组织中,它们不再受到机械力的增殖抑制,出现了大规模的扩增;更关键的是,将沉默了Nesprin-2的肺癌细胞注射到小鼠正常跳动的心脏中后,这些癌细胞彻底突破了心脏的抗癌防御,在生理机械负荷下依然能大量增殖,形成了体积巨大的肿瘤。
进一步的检测显示,Nesprin-2沉默后,即便在机械负荷存在的条件下,癌细胞的染色质压缩程度与H3K9me3水平也完全恢复,直接证明了Nesprin-2正是心脏将机械跳动转化为抗癌效应的核心分子传感器。
这项研究的价值,远不止于破解了“心脏为何几乎不得癌”这一困扰医学界百年的谜题,更彻底刷新了我们对癌症调控的认知。在此之前,肿瘤研究多聚焦于基因、代谢、免疫等生物化学层面的调控。
而这项研究首次证实,纯粹的物理机械力——器官正常生理活动产生的周期性压缩应力,能通过机械-表观遗传调控,直接决定癌细胞的增殖命运,为癌症治疗开辟了一条前所未有的“物理抗癌”新赛道。
研究团队在讨论中指出,心脏的收缩产生的是正向压缩力,这与肺部呼吸产生的负压拉伸力完全不同,这也解释了为何同为持续节律运动的器官,肺部却极易发生原发与转移肿瘤,为不同器官的肿瘤易感性差异提供了全新的力学解释。
同时,这项研究也带来了重要的临床启示:目前已有多款靶向组蛋白去甲基化酶(KDMs)的表观遗传药物进入癌症临床试验,而这项研究的结果提示,这类药物可能会削弱心脏的天然抗癌防御,其心脏安全性需要更严格的评估;反过来,基于这项研究发现的机械-表观遗传调控通路,未来或许能开发出人工机械刺激设备,通过特定频率、强度的力学干预,让人体其他部位的肿瘤也“感受”到类似心脏的增殖抑制信号,为实体瘤治疗提供一种全新的、非药物的物理干预手段。
正如同期Science配发的评论中所言,这项研究让我们重新认识了机械力在生命活动中的核心地位。心脏用每一次永不停歇的跳动,为全身输送着维持生命的血液,而它隐藏在节律收缩中的“抗癌超能力”,不仅守护着自身的安全,更有望成为人类攻克癌症的下一个关键突破口。
[1]Giulio Ciucci,Daniela Lorizio,Nicoletta Bartoloni, et al. Mechanical load inhibits cancer growth in mouse and human hearts. Science(2026).doi:10.1126/science.ads9412.
