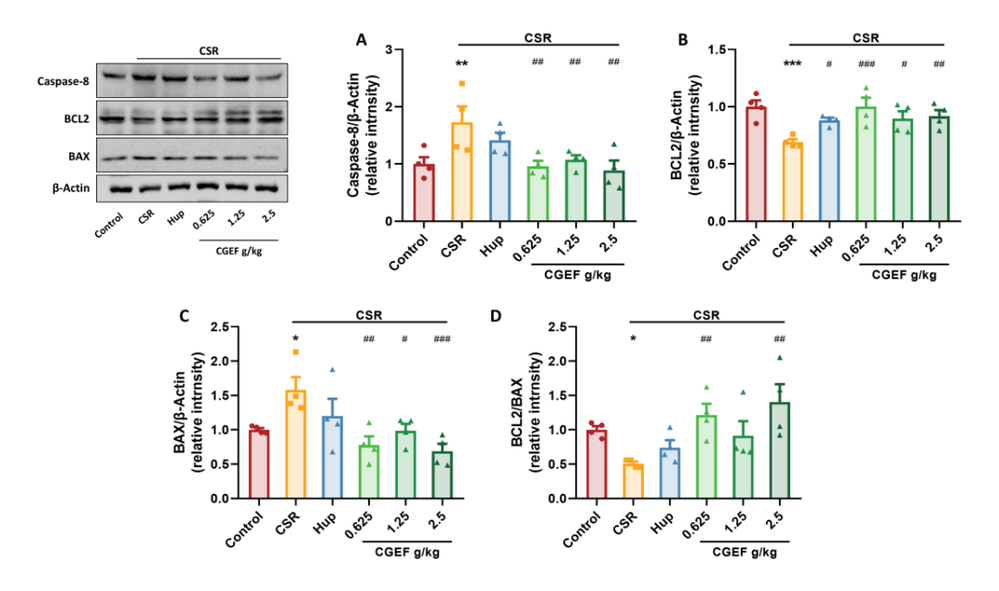
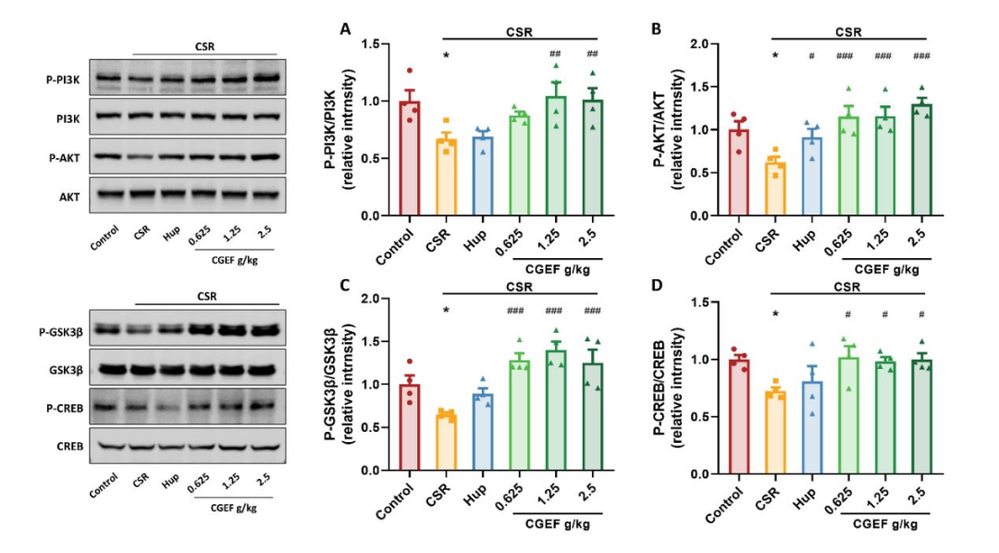
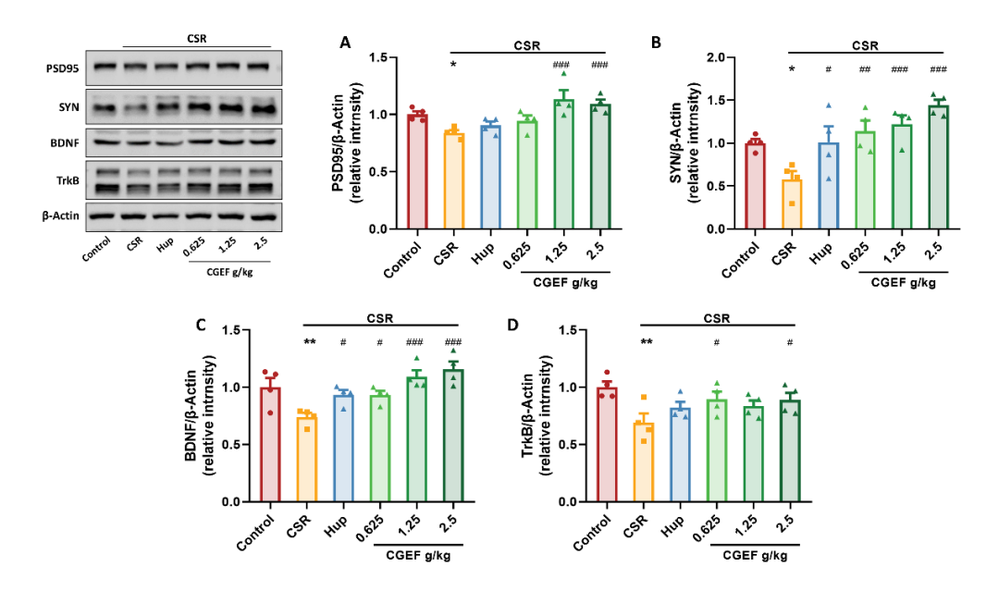
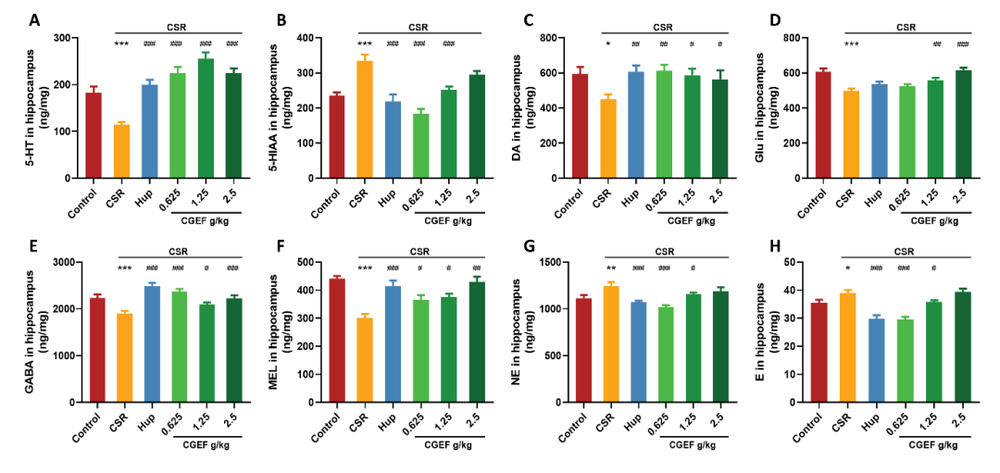
睡眠不足影响认知?传统中药或可逆转!中国医学科学院与北京协和医院联合发布:天麻、黄精和茯苓通过抗炎与神经保护改善认知功能
2026年4月14日
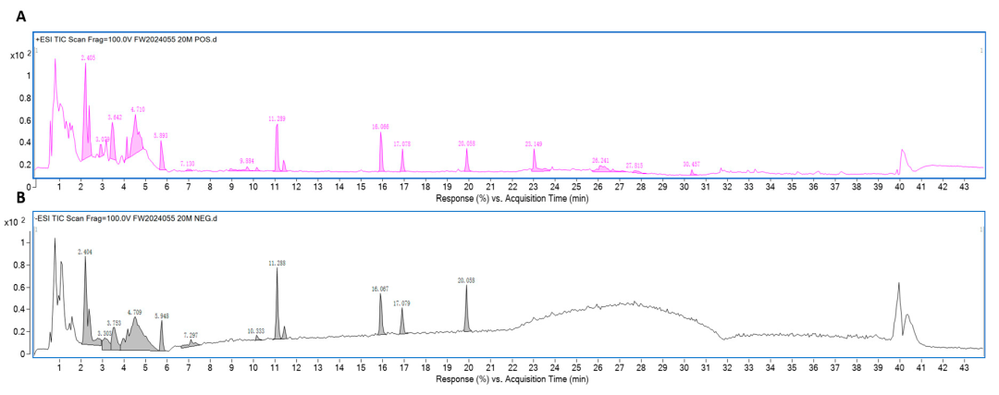
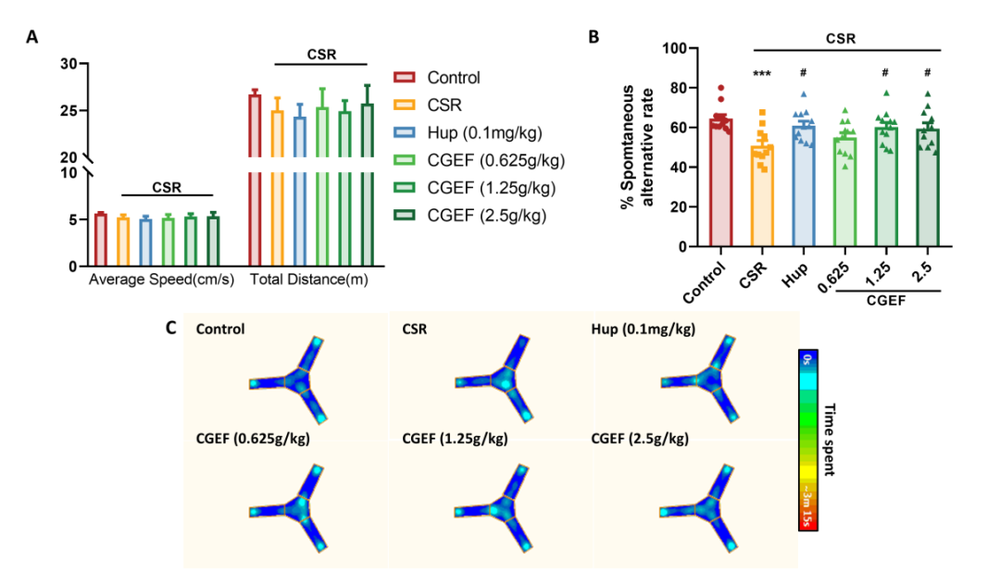
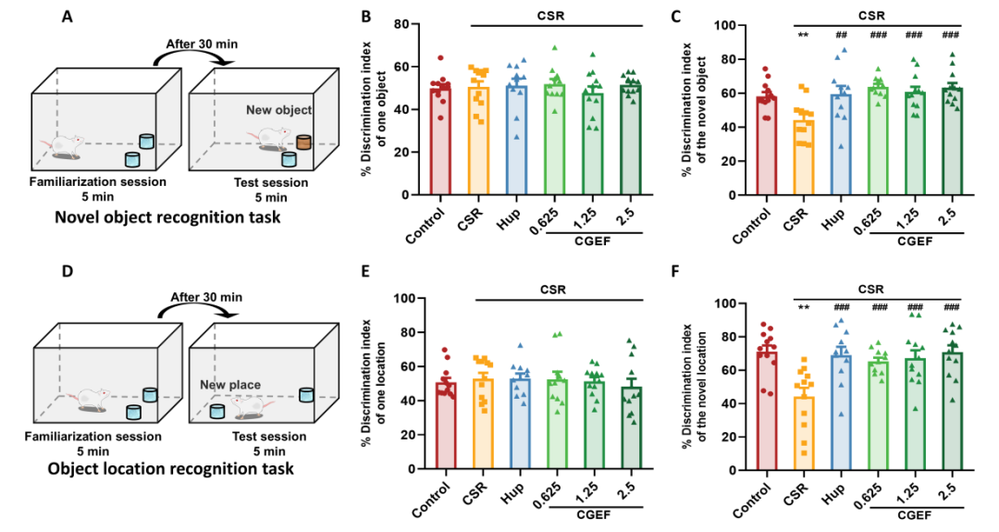
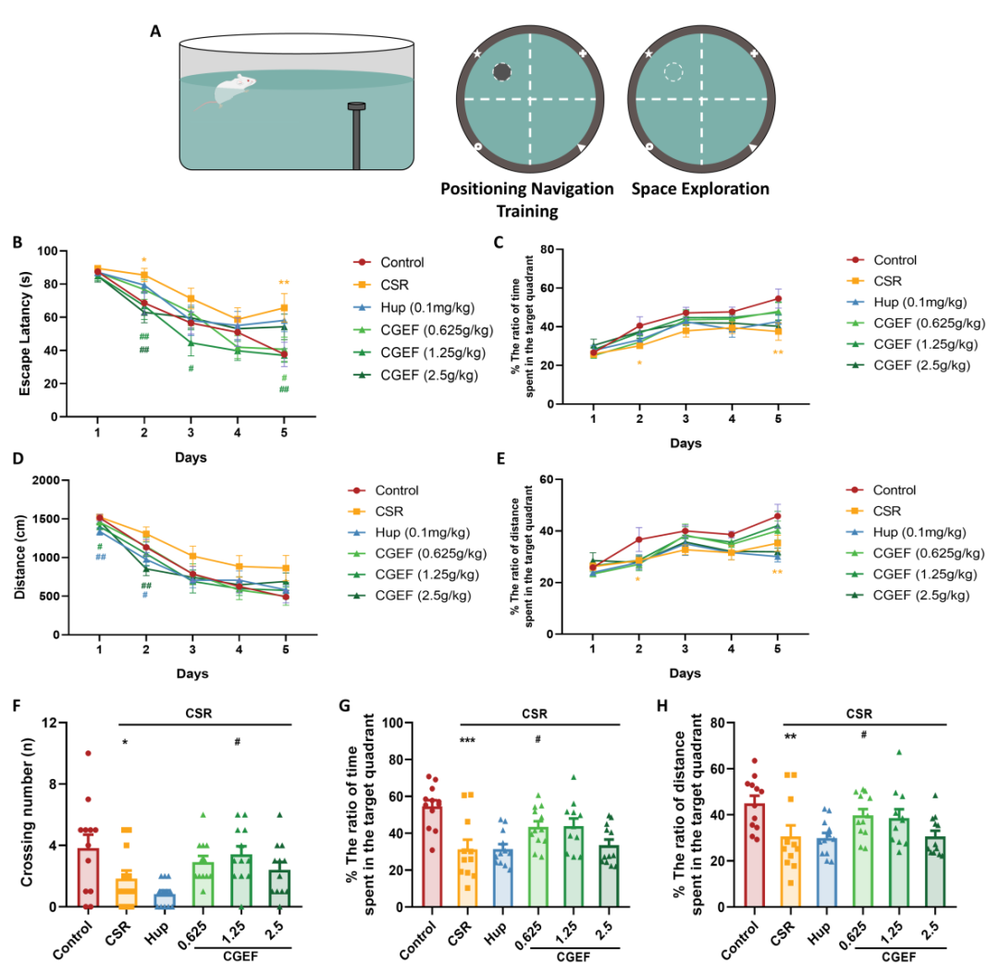
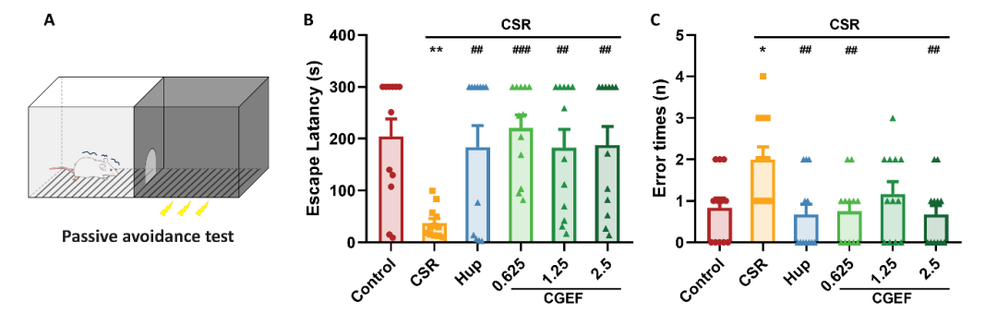
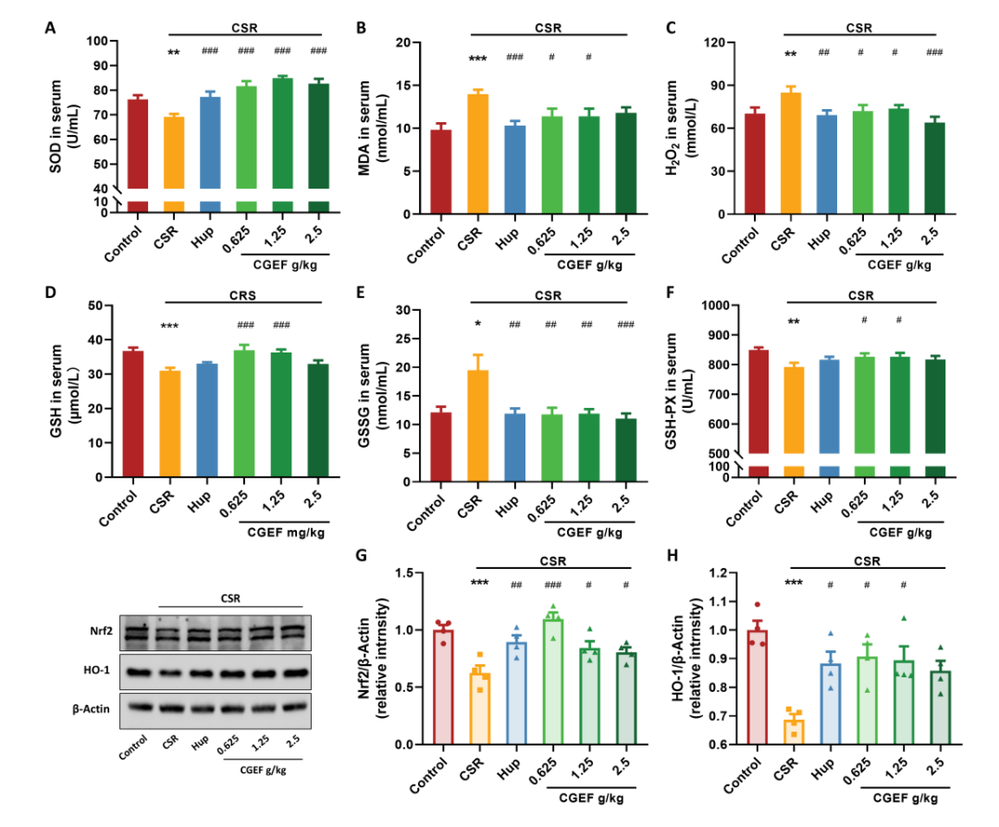
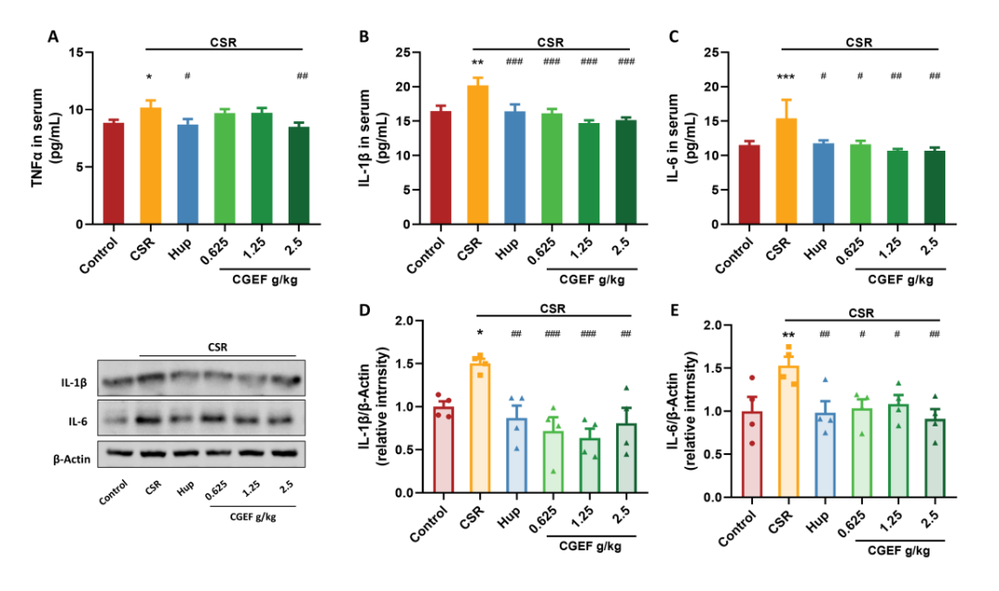
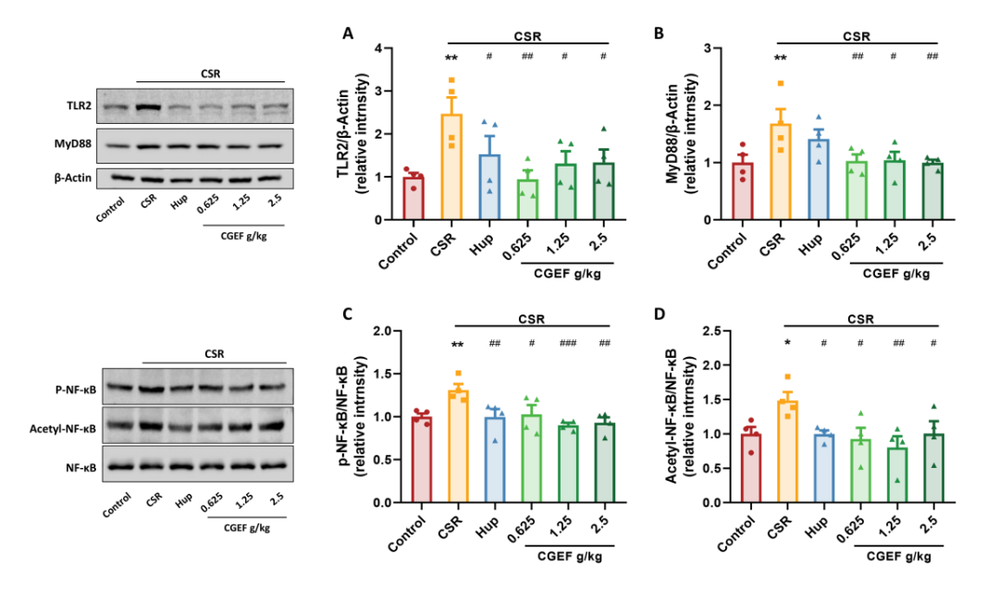
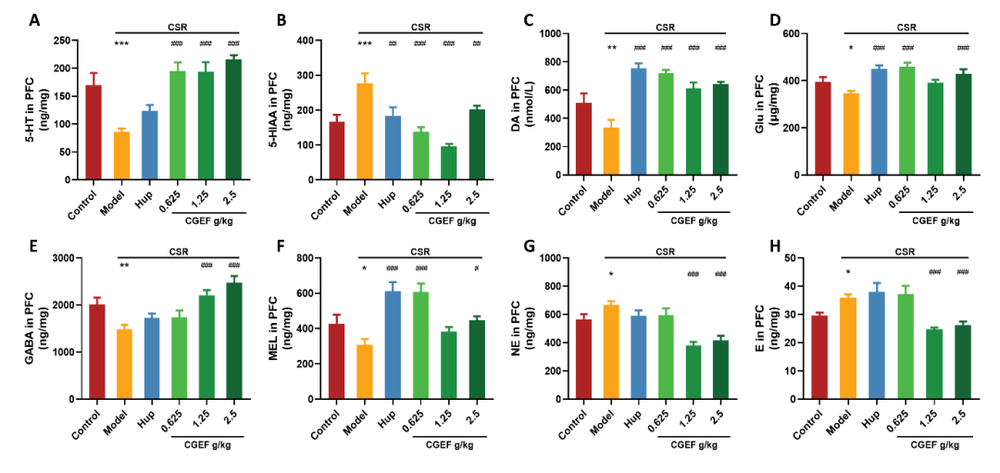
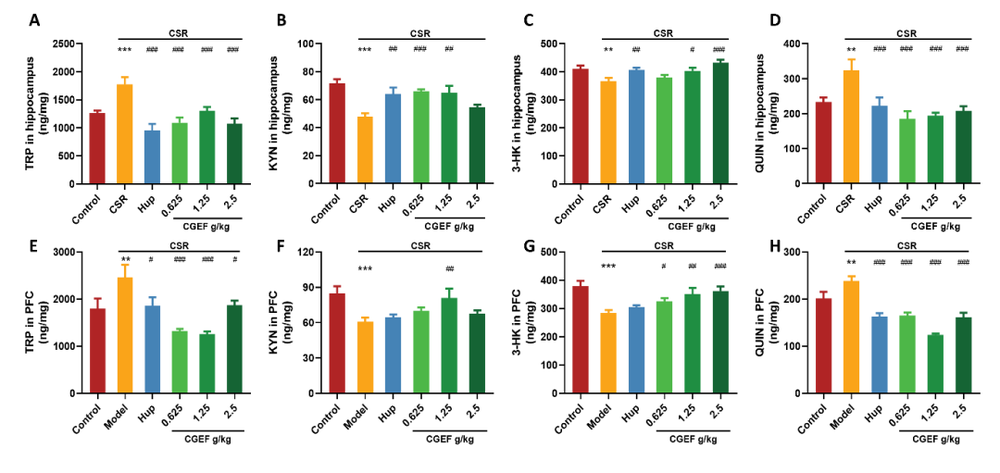
现代社会的快速发展带来了睡眠健康的严峻挑战,快节奏的生活方式、长时间屏幕暴露以及不断增加的工作压力共同导致了睡眠质量的普遍下降。睡眠障碍不仅降低了个体的生活满意度,还与认知功能障碍密切相关。研究表明,慢性睡眠不足或睡眠质量差与记忆力、注意力和执行功能缺陷相关,可能增加患痴呆症的风险。因此,开发安全有效的治疗方法来对抗睡眠剥夺相关的认知衰退需求日益迫切。随着健康意识的提高,从食药同源草药开发功能性食品受到越来越多的关注。天麻、黄精和茯苓作为常用的食药同源物质,传统上被认为可以补气养血、平肝息风、安神益智。近期,一项研究评估了一种由天麻、黄精和茯苓组成的草药功能性食品配方——天麻复方(CGEF),发现该复方通过调节多种生物标志物和信号通路,显著改善了慢性睡眠限制(CSR)小鼠的认知功能。CGEF 源自经典的中药方剂 “茯苓天麻汤”,在增强认知功能方面显示出潜力。CGEF由天麻、黄精和茯苓按1:1:1比例混合,经三次水提、过滤和浓缩制备而成。通过LCMS分析,研究人员在CGEF中鉴定出28个特征峰,对应三种草药的多种活性成分,包括天麻中的天麻素、对羟基苯甲醇,以及黄精和茯苓中的皂苷、单糖和多糖等。这些成分共同构成了CGEF的化学基础,为其后续的药理作用提供了物质基础。图2 CGEF成分的液相色谱-质谱(LCMS)特征在开放场测试中,CSR小鼠与对照组在运动距离、运动时间和速度方面均无显著差异,表明CSR本身并未影响小鼠的基础运动能力。更重要的是,CGEF给药后小鼠的运动活动也未发生显著改变。这一结果至关重要,说明CGEF的认知改善作用并非通过改变运动能力实现,而是直接作用于认知相关的神经机制,排除了运动功能干扰对后续认知行为学测试的影响。Y迷宫测试用于评估小鼠的短期空间记忆能力。结果显示,CSR小鼠的自发交替率显著低于对照组,证实了CSR诱导的短期空间记忆障碍。然而,CGEF中剂量(1.25g/kg)和高剂量(2.5g/kg)处理组的小鼠自发交替率显著改善。热图分析进一步显示,CSR小鼠表现出重复进入同一臂的刻板行为,而CGEF处理组小鼠则展现出更广泛的探索行为模式,表明CGEF对CSR引起的认知缺陷具有明确的保护作用。物体识别测试包括新物体识别测试(NORT)和物体位置识别测试(OLRT),分别评估新奇物体识别能力和空间记忆。CSR小鼠在这两项测试中的区分指数均显著下降,表明其对新奇物体的识别能力和空间记忆均受到损害。值得注意的是,阳性对照药物石杉碱甲以及所有剂量的CGEF均显著逆转了CSR引起的区分指数降低,提示CGEF能够有效改善CSR小鼠的陈述性记忆和空间记忆功能。Morris水迷宫是评估空间学习和记忆的金标准。在定位导航训练阶段,CSR小鼠的逃避潜伏期显著延长,且随训练天数增加而恶化。CGEF以剂量依赖性方式改善了这一缺陷:低剂量在第5天、中剂量在第2-5天、高剂量在第2天即显示出显著效果。在空间探索测试中,CSR小鼠的平台穿越次数、目标象限停留时间和距离百分比均显著降低,而CGEF处理显著改善了这些指标。这些结果有力证明CGEF能够显著缓解CSR引起的长期空间记忆损害。图6 CGEF对CSR小鼠Morris水迷宫表现的影响被动回避测试基于条件反射评估学习和记忆能力。CSR小鼠进入暗室的潜伏期显著缩短,错误次数增加,表明其学习和记忆巩固过程受损。CGEF给药显著延长了进入暗室的潜伏期,并减少了错误次数,与阳性对照药物效果相当。这表明CGEF对CSR小鼠的学习获取和记忆巩固过程具有明确的保护作用。氧化应激是睡眠剥夺相关认知障碍的关键机制。CSR小鼠血清中SOD活性降低,MDA和H₂O₂水平升高,GSH水平及GSH-Px活性下降,GSSG水平上升,呈现典型的氧化应激状态。CGEF显著逆转了这些变化,并上调了海马体中Nrf2/HO-1通路的活性。Nrf2作为细胞抗氧化防御的核心转录因子,其激活可诱导HO-1等抗氧化蛋白的表达,从而增强大脑抗氧化能力,减轻氧化应激引起的神经元损伤。图8 CGEF对CSR小鼠氧化应激相关生化指标的影响睡眠剥夺通过升高促炎细胞因子引发神经炎症。CSR小鼠血清中TNF-α、IL-1β和IL-6水平显著升高,海马体中IL-1β和IL-6表达也显著增加。CGEF给药显著抑制了这些炎症标志物的升高,且在所有测试剂量下均有效,表明CGEF具有稳健的抗炎作用,能够减轻CSR相关的神经炎症反应。CGEF对CSR小鼠TLR2/MyD88/NF-κB通路的影响TLR2/MyD88/NF-κB通路是神经炎症的核心调控通路。CSR显著上调了海马体中TLR2和MyD88的表达,并增加了NF-κB的磷酸化和乙酰化。CGEF在所有测试剂量下均显著抑制了这一信号通路的激活,表明CGEF通过抑制TLR2介导的炎症信号级联反应,从上游阻断神经炎症的发生,这是其发挥神经保护作用的重要分子机制。图10 CGEF对CSR小鼠TLR2/MyD88/NF-κB通路的影响神经炎症与神经元凋亡密切相关。CSR显著上调促凋亡蛋白caspase-8和BAX的表达,下调抗凋亡蛋白BCL2,导致BCL2/BAX比值失衡。CGEF给药显著逆转了这些变化,增加了BCL2表达,降低了caspase-8和BAX水平,恢复了正常的BCL2/BAX比值。这表明CGEF通过调节关键凋亡信号通路,有效对抗了CSR引起的神经元凋亡。图11 CGEF对CSR小鼠海马体凋亡蛋白表达的影响CGEF对CSR小鼠海马体PI3K/AKT/GSK3β和CREB信号通路的影响PI3K/AKT/GSK3β通路对神经元存活和突触可塑性至关重要。CSR抑制了该通路中PI3K、AKT和GSK3β的磷酸化,同时降低了CREB的磷酸化。CGEF显著恢复了这些蛋白的磷酸化水平,且在所有剂量下均有效。GSK3β的适度抑制可增强神经保护,而CGEF通过恢复GSK3β Ser9位点的磷酸化,实现了对其活性的精确调控,进而促进CREB激活,为突触可塑性和记忆形成提供分子基础。图12 CGEF对CSR小鼠海马体PI3K/AKT/GSK3β和CREB信号通路的影响突触可塑性蛋白和神经营养因子对认知功能至关重要。CSR显著降低了突触蛋白PSD95和SYN的表达,以及BDNF及其受体TrkB的水平。CGEF给药显著增加了SYN和BDNF的表达,高剂量还显著增强了PSD95表达,低剂量和高剂量均显著上调了TrkB表达。这些结果表明CGEF能够有效缓解CSR引起的突触功能障碍和神经营养缺陷,维持神经元的结构和功能完整性。图13 CGEF对CSR小鼠海马体神经保护蛋白的影响神经递质稳态对认知功能至关重要。CSR导致海马体中5-HT、DA、Glu、GABA和MEL水平显著降低,而5-HIAA、NE和E水平升高,呈现复杂的神经递质紊乱。CGEF有效逆转了这些异常,恢复了5-HT、DA、GABA和MEL水平,降低了5-HIAA、NE和E水平,中剂量和高剂量还显著增加了Glu水平。这表明CGEF在恢复神经递质平衡方面发挥了关键作用。图14 CGEF对CSR小鼠海马体神经递质水平的影响前额叶皮层的神经递质变化与海马体类似。CSR导致5-HT、DA、Glu、GABA和MEL水平降低,5-HIAA、NE和E水平升高。CGEF在所有剂量下均逆转了5-HT和5-HIAA的异常,显著增加了DA水平,低剂量和高剂量增强了Glu和MEL,中剂量和高剂量增加了GABA并降低了NE和E。这表明CGEF对皮层和海马体神经递质系统具有广泛的调节作用。图15 CGEF对CSR小鼠前额叶皮层神经递质水平的影响色氨酸代谢紊乱是睡眠剥夺相关认知障碍的重要机制。CSR导致TRP在海马体和前额叶皮层中积累,KYN和3-HK水平降低,而神经毒性代谢产物QUIN显著增加。CGEF显著降低了TRP和QUIN水平,增加了KYN和3-HK水平,改善了TRP-KYN代谢途径的平衡。通过抑制QUIN的产生,CGEF减少了神经毒性代谢产物的积累,保护神经元免受兴奋毒性损伤。图16 CGEF对CSR小鼠大脑中色氨酸代谢的影响本研究系统阐明了天麻-黄精-茯苓复方(CGEF)改善慢性睡眠限制小鼠认知功能障碍的多靶点机制。CGEF通过抑制TLR2/MyD88/NF-κB通路减轻神经炎症,调节PI3K/AKT/GSK3β通路维持神经元完整性和突触可塑性,激活Nrf2/HO-1通路增强抗氧化能力,调节凋亡相关蛋白减少神经元死亡,恢复神经递质稳态和色氨酸代谢平衡,最终实现对认知功能的全面保护。这些发现不仅为CGEF作为功能性食品开发提供了坚实的科学依据,也彰显了食药同源产品在现代神经保护研究中的广阔应用前景,为睡眠剥夺相关认知障碍的预防和干预提供了新的策略。Zhang Y, Chen F, Li X, Xu Y, Liu X, Barkat MQ, Choudhary MI, Chang Q, Jiang N. Gastrodia elata, Polygonatum sibiricum, and Poria cocos as a Functional Food Formula: Cognitive Enhancement via Modulation of Hippocampal Neuroinflammation and Neuroprotection in Sleep-Restricted Mice. Foods. 2025 Mar 22;14(7):1103. doi: 10.3390/foods14071103. PMID: 40238194; PMCID: PMC11988919.老中医(微信号:wxid_rszr95aw79ie22)