全球范围内,每1000名新生儿中就有2-3人受先天性听力损失困扰,其中高达60%的病例由遗传突变导致。在遗传性耳聋中,OTOF基因突变引起的常染色体隐性遗传性耳聋9型(DFNB9),虽仅占遗传性耳聋的2%-8%,却在儿童先天性听神经病谱系障碍中占比高达41%。
这类患者因内耳关键蛋白功能缺失,一出生便面临重度至极重度的双耳听力丧失,常规助听器、人工耳蜗仅能提供有限帮助,且此前全球范围内没有获批的根治性治疗手段,无数患者终身被困在无声世界。
而一项最新发布的国际多中心临床试验结果,为这一群体带来了重获听力的真正曙光。
日前,一篇发表在国际顶级期刊Nature上、题为Multicentre gene therapy for OTOF-related deafness followed up to 2.5 years的研究,发布了迄今为止全球样本量最大、随访时间最长、年龄覆盖最广的遗传性耳聋基因治疗临床试验成果。
该研究由复旦大学附属眼耳鼻喉科医院舒易来、李华伟团队领衔,联合哈佛医学院麻省眼耳医院Zheng-Yi Chen教授团队,以及国内8家临床中心共同完成,用扎实的临床数据证实了基因治疗根治这类耳聋的长期安全性与有效性。
这项单臂、多中心临床试验,从3193名受试者中完成严格筛选,最终纳入42 名携带OTOF致病/疑似致病突变的重度-全聋患者,年龄跨度从0.8岁到32.3岁,首次覆盖了婴幼儿、儿童、青少年和成人全年龄段,打破了此前同类研究仅纳入儿童患者的局限。
所有患者均通过微创耳内镜手术,单次向内耳注射携带人OTOF编码转基因的1型腺相关病毒载体(AAV1-hOTOF),研究设置了3个剂量梯度,其中36人接受单耳给药,6人接受双耳给药,总计48只治疗耳,随访时间最长达2.5年,中位随访时间52周。
研究的主要终点为治疗后 6 周内的剂量限制性毒性,次要终点全面评估治疗的长期疗效与不良事件发生情况。

安全性是基因治疗临床应用的核心前提,这项研究交出了令人安心的答卷。整个随访期内,未观察到任何剂量限制性毒性,也未发生任何与治疗相关的严重不良事件。
绝大多数不良事件为1-2级的轻微反应,仅3例患者出现3级中性粒细胞计数下降,所有病例均无发热、感染等相关临床症状,且血象异常可自行完全缓解。
治疗后最常见的实验室检查异常为淋巴细胞计数升高(45%)、胆固醇水平升高(43%),均为一过性反应;耳部相关不良事件发生率极低,仅3例出现1级眩晕,1例出现2级中耳炎,均经对症处理或自行完全痊愈,未留下任何后遗症。
免疫相关检测进一步验证了疗法的长期安全性:97%的患者在治疗后13周,针对AAV1衣壳的T细胞反应为阴性,85%的受试者治疗后体内载体DNA 检测为阴性,未出现持续的全身免疫反应。
在疗效层面,研究数据实现了历史性突破。治疗后,90%的受试者(38/42)、90%的治疗耳(43/48)实现了明确的听力恢复,部分患者最早在治疗后5天就报告能感知到外界声音。
听力改善呈现出“快速起效、持续稳步提升”的特点:治疗后6周内,患者就出现了显著的听力提升,这一阶段的改善幅度占到了 2.5年总获益的40%以上;在后续长达2.5年的随访中,患者的听力水平仍保持持续向好的稳定趋势,未出现疗效衰减。
客观听觉电生理检测显示,患者的听性脑干反应(ABR)阈值从基线时的>97±1dB nHL(正常听力水平),在治疗后1年、1.5年、2年、2.5年分别降至 54±3、51±3、50±3、42±5dB nHL;行为测听阈值从基线时的>96±3dB HL,降至2.5年时的37±5dB HL。
更令人振奋的是,有受试者在2.5年随访时达到了正常听力水平,ABR、听觉稳态反应(ASSR)和行为测听阈值分别低至25dB nHL、25dB nHL和16dB HL,实现了从全聋到正常听力的跨越。
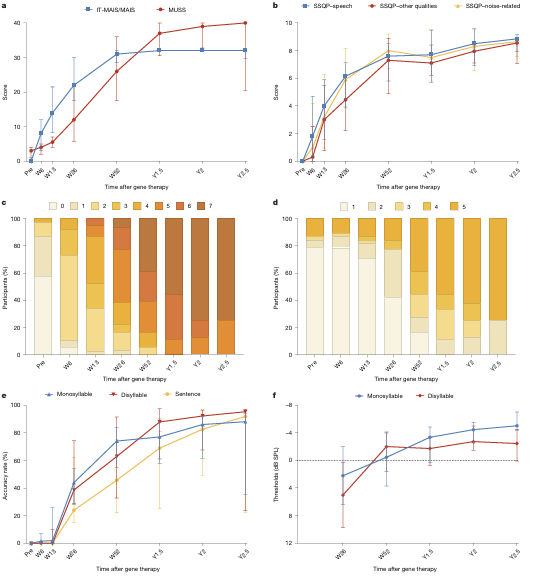
听力恢复参与者从基线到2.5年期间的言语问卷和测试
比“听到声音”更重要的,是患者言语感知与表达能力的全面恢复,这也是解决先天性耳聋患者语言发育障碍、回归正常生活的核心。随着听力的持续稳定恢复,患者的言语能力呈现渐进式的显著提升,且随访时间越长,改善效果越突出。
评估听觉功能的听觉行为分级(CAP)评分,从基线的0-1级(仅能感知环境声音或完全无反应),提升至2年、2.5年时的中位数7级;2年时,88%的患者无需借助任何助听设备,就能达到6级以上(无需读唇即可理解日常对话),75%的患者达到最高7级,实现了无障碍接打电话的核心需求。
评估言语清晰度的言语可懂度分级(SIR)评分,从基线的1级(言语无法被理解),提升至2年、2.5年时的中位数5级;2年时63%、2.5年时75%的患者达到最高5级,连贯言语能被所有听者轻松理解。
在安静环境中,患者的双音节词识别率从基线的0%,提升至2.5年时的中位数95.3%;即使在嘈杂的日常环境中,患者的言语识别能力也实现了质的飞跃,真正完成了从“听不到”到“听得清、能交流、可融入”的彻底改变。
研究还同时证实,接受双耳治疗的患者,在嘈杂环境下的听觉和言语表现显著优于单耳治疗者,为未来的双耳给药策略提供了直接的临床证据。
研究团队还进一步探索了影响治疗效果的关键因素,筛选出了可预测疗效的核心生物标志物,为未来的临床精准治疗提供了重要依据。
首先是年龄因素:0.5-18岁的未成年患者,听力改善幅度显著优于成人,其中0.5-3岁的婴幼儿治疗有效率达到100%,3-8岁儿童有效率92%,8-18岁青少年有效率 60%;而纳入研究的3名成人患者(20.4岁、29.2岁、32.3岁)中,2人实现了明确的听力恢复,尽管改善幅度不及未成年患者,但32.3岁的成人患者在治疗后52周,ABR阈值仍改善了27dB,安静环境下单音节识别率从基线的2%提升至56%。
这一结果打破了“成年后听觉系统可塑性丧失、无法通过治疗恢复听力”的传统认知,证实了人类听觉系统的灵活性远超此前预期。其次是基线内耳功能:治疗前畸变产物耳声发射(DPOAE,评估内耳外毛细胞功能的核心指标)可引出的数量越多、信噪比越高,患者的听力恢复效果越好;而基线无DPOAE引出的耳朵,治疗有效率仅为40%,这一发现提示基线DPOAE可作为疗效预测的重要无创生物标志物。
此外,OTOF变异类型也与恢复程度相关:携带双等位非截短型OTOF变异的患者,听力恢复效果优于携带截短型变异的患者,但值得注意的是,不同变异类型的患者,治疗总有效率无显著差异(88%-94%),意味着绝大多数OTOF 突变相关的耳聋患者,都有机会从该疗法中获益。
同时,研究未观察到3个剂量组之间存在明显的剂量依赖性疗效差异,这为未来探索更低治疗剂量、降低生产成本与治疗风险、扩大疗法可及性提供了重要依据。
从治疗机制来看,这项疗法实现了对耳聋的根源性修复。OTOF基因编码的otoferlin蛋白,是内耳内毛细胞中负责突触囊泡释放、将声音信号转化为神经信号传递给大脑的核心“开关”。
当OTOF发生双等位致病突变时,otoferlin蛋白功能完全缺失,声音信号无法传递到大脑听觉中枢,患者一出生便陷入无声世界,而常规的人工耳蜗无法解决神经信号传递的根本缺陷,治疗效果有限。
AAV1-hOTOF基因疗法,正是通过安全的腺相关病毒载体,将正常的OTOF基因精准递送到内耳毛细胞中,让细胞重新合成有功能的otoferlin蛋白,重启声音信号的生理传递通路,仅需单次注射,就能实现长期的听力修复效果。
这项研究是遗传性耳聋基因治疗领域的里程碑式突破,它不仅用全球最大规模的临床样本、最长的随访时间,证实了AAV1-hOTOF基因疗法的长期安全性与稳定疗效,更将治疗的适用人群从低龄儿童拓展到了成人,为全球数百万OTOF相关耳聋患者带来了根治疾病的希望。
当然,研究也存在一定的局限性,比如剂量探索范围较窄、超2年长期随访的样本量仍有限,仍有约10%的患者对治疗无反应,其背后的分子机制还需要进一步探索。
研究团队表示,未来将继续对受试者进行长期随访,同时计划启动海外临床试验,还将进一步拓展基因治疗的适用范围,开发针对其他类型遗传性耳聋的基因治疗与基因编辑技术,让更多类型的耳聋患者也能迎来重获听力的机会。
对于无数被遗传性耳聋困住的家庭而言,“听见世界、开口说话”不再是遥不可及的梦想,内耳基因治疗的时代,正在为他们打开有声世界的大门。
[1]Jiang, L., Cheng, X., Lv, J. et al. Multicentre gene therapy for OTOF-related deafness followed up to 2.5 years. Nature (2026). doi:10.1038/s41586-026-10393-y
