全球每年因心血管疾病死亡的人数高达1790万,这一数字让心血管疾病长期稳居全球人类死因首位,而2型糖尿病、肥胖正是驱动心血管风险持续攀升的两大核心危险因素,尤其在高风险人群中,二者并存时,心梗、卒中、心血管死亡的发生风险会出现显著升高。
近年来,胰高血糖素样肽-1受体激动剂(glucagon-like peptide-1 receptor agonists, GLP-1RAs)这类最初获批用于2型糖尿病治疗的药物,凭借明确的降糖、减重效果迅速走入大众视野,成为全网热议的焦点。
但大众对这类药物的认知大多停留在代谢指标改善层面,对于已经确诊心血管疾病、或合并多种危险因素的高风险人群,GLP-1RAs能否带来真正的心血管硬终点获益,始终是临床与大众共同关注的核心问题。
日前,一篇发表在国际期刊Cardiovascular Diabetology–Endocrinology Reports上的大型系统性回顾与荟萃分析,为这一问题给出了高确定性的答案。
在这项研究中,来自英国安格利亚鲁斯金大学等机构的科研团队,严格遵循 PRISMA 2020循证研究指南,系统检索了PubMed、Embase(OVID 平台)及 Cochrane图书馆三大数据库中,2015年1月至2025年5月期间发表的相关研究文献。
研究设定了严苛的纳入标准:仅纳入随机、安慰剂对照的心血管结局试验(CVOTs),且每项试验受试者总样本量不少于3000例,最低随访时长不低于 12 个月,以此确保研究结论能真实反映药物的长期心血管效应。

经过层层筛选,最终共有11项高质量临床试验符合纳入标准,合计纳入91490名成年高心血管风险受试者,受试者平均年龄63.8岁,其中66.1%为男性,研究整体中位随访时长2.7年,最长随访时间达5.4年。
研究所覆盖的GLP-1RAs囊括了临床主流应用的各类品种,包括利拉鲁肽、利司那肽、司美格鲁肽(注射剂+口服制剂)、艾塞那肽、阿必鲁肽、度拉糖肽、艾本那肽,完整覆盖了该类药物的不同剂型与给药方案。
研究的核心结果显示,与安慰剂相比,接受GLP-1RAs治疗的高心血管风险人群,主要不良心血管事件(MACE,心血管死亡、非致死性心梗、非致死性卒中的复合终点)发生风险出现了具有统计学意义的显著下降,合并风险比 HR=0.86,这意味着使用GLP-1RAs的受试者,发生心梗、卒中或心血管死亡的相对风险整体降低了14%。
更重要的是,经GRADE体系评估,包括主要终点在内的所有研究结局,证据确定性均为最高等级的“高确定性”,11项纳入试验中,有10项在所有偏倚风险维度均被评为低风险,进一步夯实了结论的可信度。
在次要终点的分析中,GLP-1RAs的心血管保护效应展现出了全链条的获益特征。数据显示,用药组受试者的心血管死亡率相对降低13%,全因死亡率同样出现13%的显著下降;非致死性心肌梗死与非致死性卒中的发生风险,也分别出现了15%的显著降低。此外,受试者因心力衰竭住院的风险也呈现12%的下降趋势。
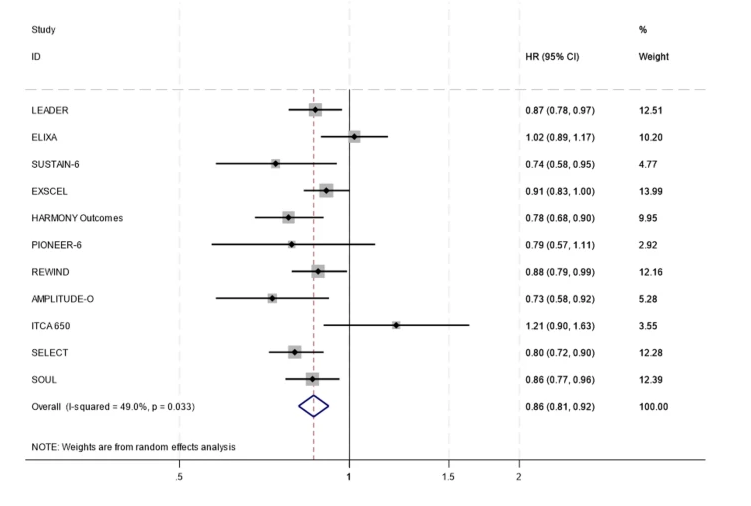
基于随机效应分析的GLP-1受体激动剂与安慰剂对比的主要不良心血管事件森林图
为了验证核心结论的稳健性,研究团队还开展了多项敏感性分析与事后亚组分析。在剔除唯一纳入糖尿病前期人群的SELECT试验后,GLP-1RAs降低MACE风险的核心结论并未发生实质性改变,证实这种心血管保护效应并非由某一特定人群驱动,而是在高心血管风险人群中具有普适性,且获益不依赖于受试者的血糖状态。
针对司美格鲁肽相关的4项临床试验进行的亚组分析显示,该药物带来的MACE降幅更为突出。但研究者也明确强调,这一结果来自事后分析,仅具有假设生成的意义,不能作为判定司美格鲁肽优于同类其他药物的直接证据。
在大众最为关注的安全性方面,这项荟萃分析也给出了清晰的答案。研究证实,GLP-1RAs并不会实质性增加严重低血糖或急性胰腺炎的发生风险,直接回应了长期以来围绕该类药物的两大安全争议。
其中,严重低血糖方面,用药组与安慰剂组的绝对风险差异仅在-0.9%至+0.9%之间,无临床意义上的风险升高,这得益于GLP-1RAs葡萄糖依赖性的降糖机制,与胰岛素、磺脲类传统降糖药相比,其低血糖风险呈现出本质性的优势。
急性胰腺炎方面,所有纳入试验中,整体事件发生率不足1%,用药组与安慰剂组的绝对风险差异通常不超过±0.3%,未发现GLP-1RAs会带来胰腺炎风险的升高。
而胃肠道不良事件(恶心、呕吐、腹泻等)确实是该类药物的典型类效应,在用药组中的发生率显著更高,组间绝对风险差异在0.6%至17%之间,这也是临床中患者停药或减量的最主要原因,但这类不良反应多为轻至中度,且大多出现在用药初期,可通过患者宣教、逐步剂量滴定、选择长效制剂等方式有效改善,显著提升用药耐受性。
从整体获益-风险平衡来看,GLP-1RAs 带来的明确心血管保护与生存获益,显著超过了其可控的不良反应风险。
这项研究的结论并非只有临床数据支撑,更有充分的生物学机制作为佐证。既往基础与转化研究已证实,心肌组织与心血管自主神经中枢中均存在GLP-1受体的表达,GLP-1RAs可通过直接激活这些靶点,改善血管内皮功能、减轻血管慢性炎症、抑制动脉粥样硬化的发生发展,同时调节心脏自主神经功能,发挥直接的心血管保护作用。
除此之外,其通过减重、降低血压、改善血脂谱、减少血糖波动带来的间接获益,也进一步协同降低了心血管疾病的发生与进展风险,这种“直接+间接”的双重作用模式,正是其能带来全链条心血管硬终点获益的核心原因。
与既往同类荟萃分析相比,这项研究采用了更严苛的纳入标准,仅聚焦于大样本、长随访的核心心血管结局试验,排除了小样本、短随访的探索性研究,最大程度减少了研究间的异质性,同时纳入了最新发布的SOUL、SELECT等重磅临床试验,数据更具时效性,也更贴合当前的临床实践。
研究也客观阐述了自身存在的局限性,比如采用的是试验层面的汇总数据,无法开展更深入的个体水平亚组分析,也未能系统探索不同给药剂量与心血管获益之间的量效关系,但这些局限并不影响核心结论的成立。
综合来看,这项涵盖近 10 万例受试者、平均随访时长超两年半的大型荟萃分析,以高确定性的循证证据证实:对于已确诊心血管疾病、或合并多种危险因素的2型糖尿病、肥胖等高心血管风险人群,GLP-1RAs不仅能实现降糖、减重的代谢管理目标,更能实实在在地降低心梗、卒中、心血管死亡与全因死亡的发生风险,同时具备良好的长期安全性。
这一结论彻底打破了大众对这类药物“仅能降糖减重”的刻板认知,对于正在使用或考虑使用GLP-1RAs的高风险人群而言,意味着在管理血糖、体重的过程中,心脏也能同步获得一层明确的保护。
而对于临床医生来说,这项研究进一步强化了在心血管高风险人群中优先考量GLP-1RAs的循证依据,证实其临床价值早已不限于内分泌代谢疾病的管理范畴,完全可以作为心血管风险综合防控策略中的重要一环。如何克服药物可及性、治疗成本等现实障碍,让更多高风险人群从这类药物中获得心血管保护获益,也成为了未来临床实践与公共卫生领域需要重点解决的问题。
[1]Peter, K., Roka, O., Sepp, E. et al. The long-term cardiovascular safety and efficacy of glucagon-like peptide-1 (GLP-1) receptor agonists in high-risk cardiovascular populations: a systematic review and meta-analysis. Cardiovasc. Diabetol. – Endocrinol. Rep. 12, 36 (2026). doi:10.1186/s40842-026-00295-3
