
当前大多数炎症性肠病(IBD)患者无法通过现有单药治疗实现疾病控制,生物制剂在52周治疗后的临床和内镜缓解率仅为30-40%。
这其中靶向p40(IL-12/IL-23)的抗体Ustekinumab已获批,基于控制适应性免疫的Th1/Th17轴,已经展现一定疗效。而IBD领域的下一代潜力靶点,调控先天+适应性免疫、黏膜修复和纤维化,两者的联合疗法或双抗成为下一个研发热点。

这其中辉瑞和Telavant合作开发了全球首个p40/TL1A双抗PF-07261271,2023年罗氏以72.5亿美元收购Telavant公司,除了获得TL1A单抗RVT-3101以外,还获得了与辉瑞就 p40/TL1A 双抗(RO7837195)进行全球合作的选择权。
目前该款产品已经在既往常规和/或高级疗法治疗失败的,中度至重度活动性溃疡性结肠炎启动一项二期临床试验(NCT06979336)。同时在刚刚结束的DDW 2026(消化疾病周)会议上,辉瑞则首次公布了PF-07261271的临床前和一期临床结果。
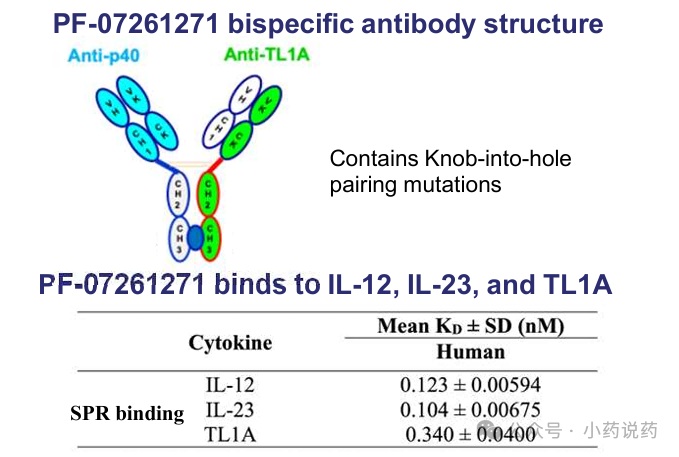
PF-07261271采用1+1的全长非对称结构,重链采用"Knobs-into-holes"技术进行构建,轻链采用crossmAb技术防止错配,与p40和TL1A的亲和力分别达到0.1nM和0.3nM级别。
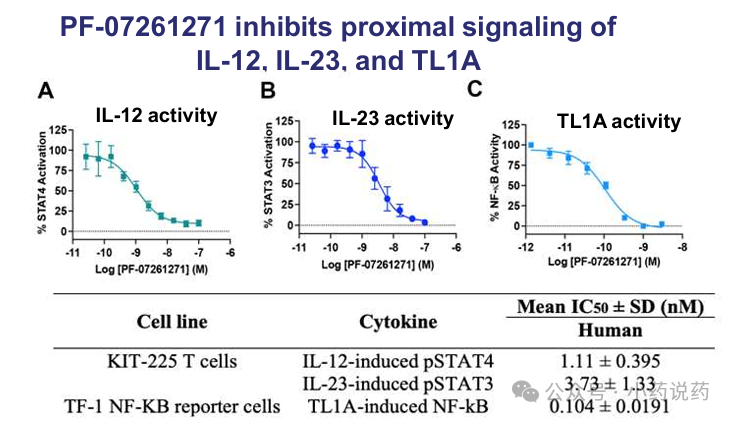
PF-07261271对TL1A通路的抑制最强(亚纳摩尔级别),对IL-12/IL-23抑制也在低纳摩尔级别,显示三重强效阻断。
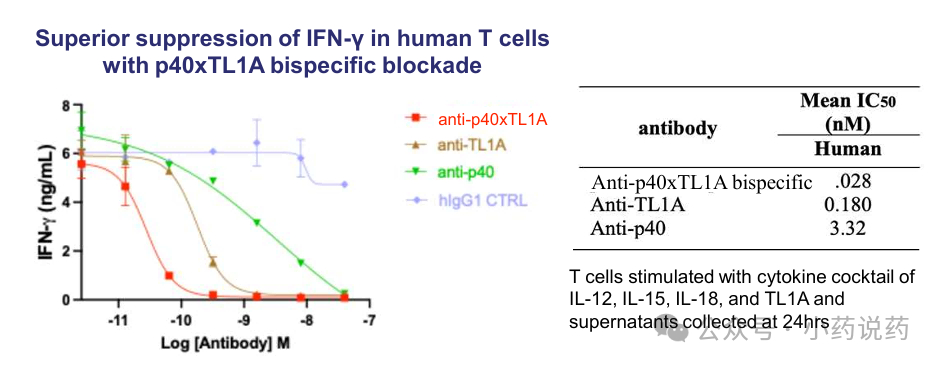
用IL-12、IL-15、IL-18和TL1A混合刺激T细胞,24小时后检测IFN-γ抑制作用显示,p40×TL1A双特异性抗体对IFN-γ的抑制,显著优于单独抗p40或抗TL1A,证明了双重阻断的协同效应。
使用抗CD3/CD28、LPS和免疫复合物刺激全血,诱导内源性IL-12和TL1A释放,PF-07261271同样对多个细胞因子实现最大抑制。

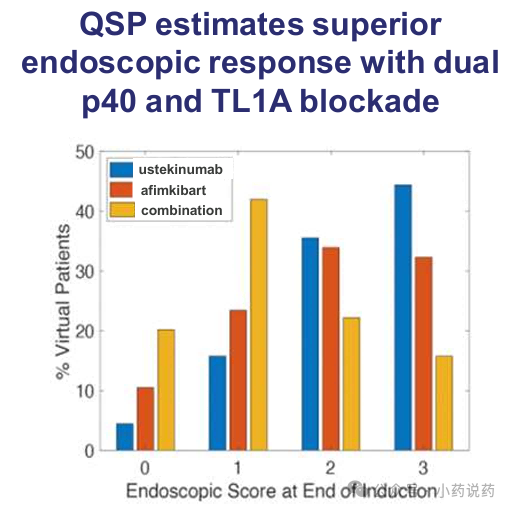
使用QSP模型预测的内镜评分分布,PF-07261271双重阻断在实现内镜评分0-1(缓解/接近缓解)的患者比例,显著优于任一单靶点治疗。
基于临床前的优异表现,PF-07261271已经在健康志愿者中完成一项I期研究(NCT05536440),总体安全且耐受性良好。
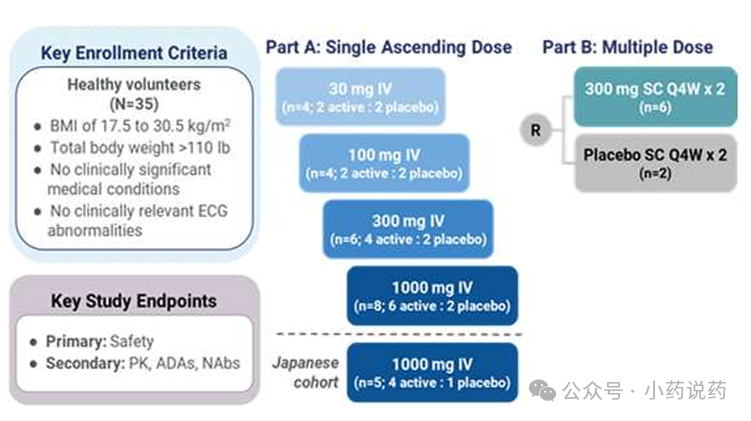
截止到报告期,35位受试者招募参加临床。安全性方面,所有不良事件均为轻度或中度,未报告严重或致命性不良事件。所有报告的注射部位反应均为轻度,且无需治疗即可在一天内消退。
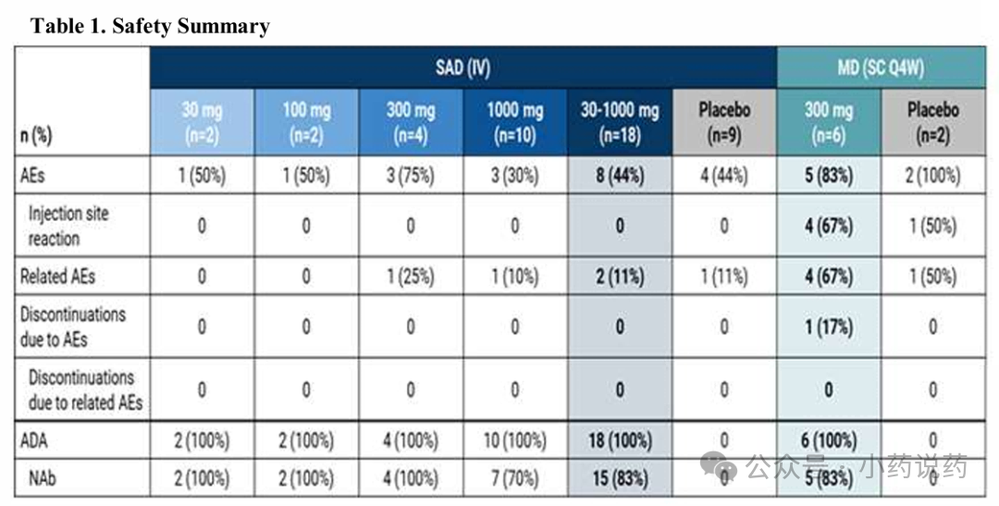
但是值得注意的是,所有患者中均出现了ADA效应,同时中和抗体发生率高达80%以上,但未观察到具有临床意义的免疫不良反应。
然而ADA始终是TNFα和TL1A靶点上的双抗开发的难题,强生,艾伯维、安进、阿斯利康、辉瑞和罗氏等多个公司的相关双抗,均因为ADA过高而停止研发。
以安进的TNF-α/TL1A双特异性抗体AMG 966为例,在针对健康志愿者的首次人体临床研究中,尽管在T细胞检测中观察到的T细胞表位较少,但AMG 966 在54名受试者中的53名(98.1%)体内引发了抗药物抗体(ADA)。这些ADA具有中和作用,并能够结合AMG 966的所有结构域。ADA的产生与药物暴露量的下降相关。
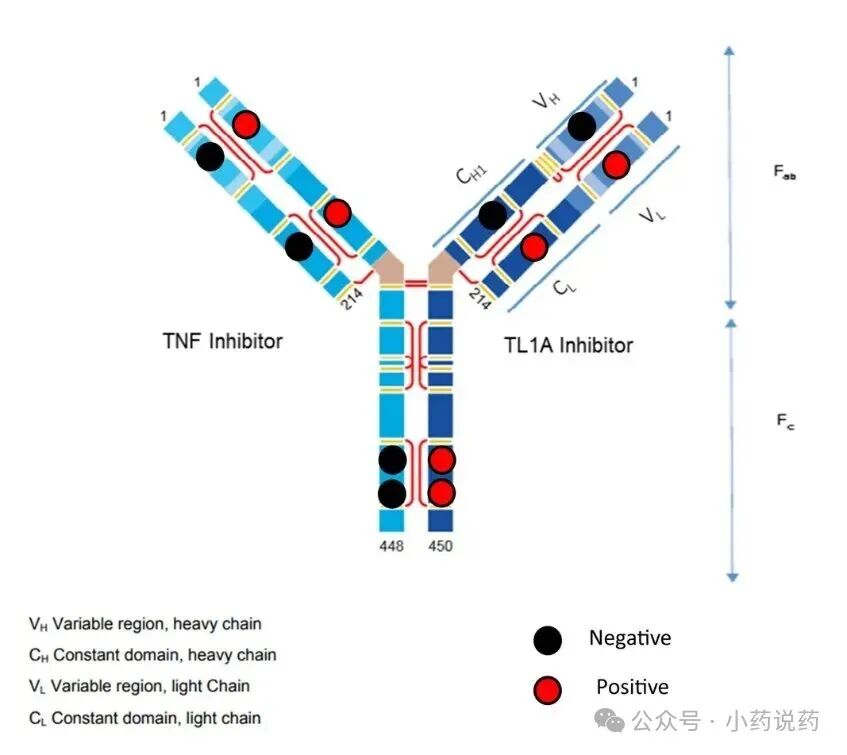
体外研究表明,在特定的药物与靶标比例下,AMG 966与TNFα和TL1A形成大型免疫复合物,部分恢复了去糖基化Fc结构域与FcγRIa和FcγRIIa的结合能力,从而导致ADA的形成,这也成为此类游离态多聚抗原靶点抗体开发的重大挑战。
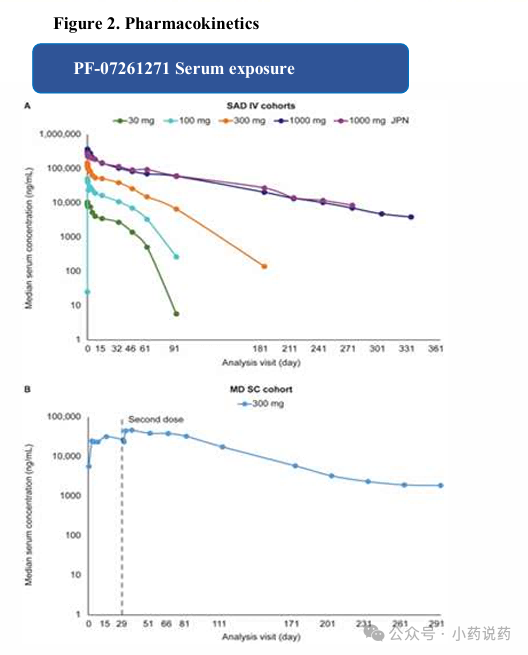
药物动力学结果显示,PF-07261271在75 mg 皮下注射及以上剂量,观察到对IL-12/IL-23和TL1A通路的近完全抑制,这支持了75 mg作为潜在的有效剂量下限,同时PD效应持续时间与PK半衰期一致,支持每4周给药。
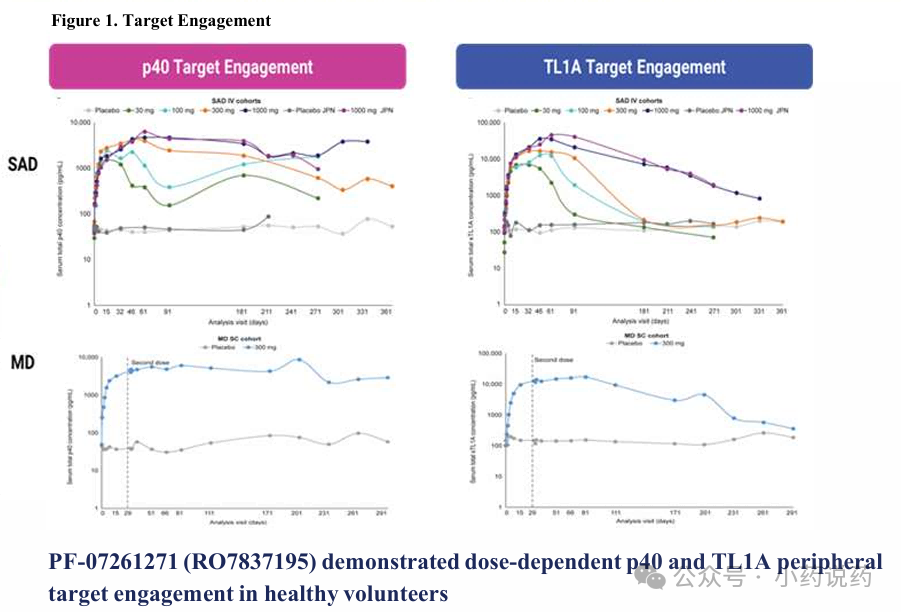
药代动力学方面结果显示,PF-07261271半衰期约2-3周,与典型IgG1抗体一致,支持每4周(Q4W)或每8周(Q8W)的给药方案,线性PK特征提示靶点介导的药物处置(TMDD)在测试剂量范围内不显著。
作为全球首款p40/TL1A双抗基于以上结果,为PF-07261271正在进行的IIb期UC试验(NCT06979336)提供了坚实的剂量选择和安全性基础。如果IIb期在内镜缓解率上验证QSP模型的预测,PF-07261271有望成为IBD治疗领域的新一代双特异性抗体标杆,但ADA的高发生率则仍然成为PF-07261271迈过生死关的首要挑战,值得关注。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
