引言
抗体偶联药物(ADC)的出现彻底改变了多种癌症的治疗格局。ADCs通常由三个主要部分组成:单克隆抗体、化学连接子和细胞毒性载荷。这些综合的治疗模式利用各组件的优势,提供了传统化疗无法实现的治疗反应。
抗体在决定肿瘤特异性、延长细胞毒性载荷的循环半衰期以及提供固有于原始抗体的额外作用机制方面发挥着关键作用,从而显著贡献于ADCs的整体表现。然而,ADCs也存在独特的安全性问题,如与正常组织中靶点介导的摄取相关的药物诱导不良事件和平台毒性,这部分源于抗体有限的肿瘤摄取。
-02-
一、抗体在ADC中的核心角色
抗体在ADC疗效中起着关键作用,通过靶点介导的摄取提供肿瘤特异性,延长细胞毒素的循环半衰期,并提供额外的机制,如受体中和、下游信号通路抑制和免疫效应功能激活。
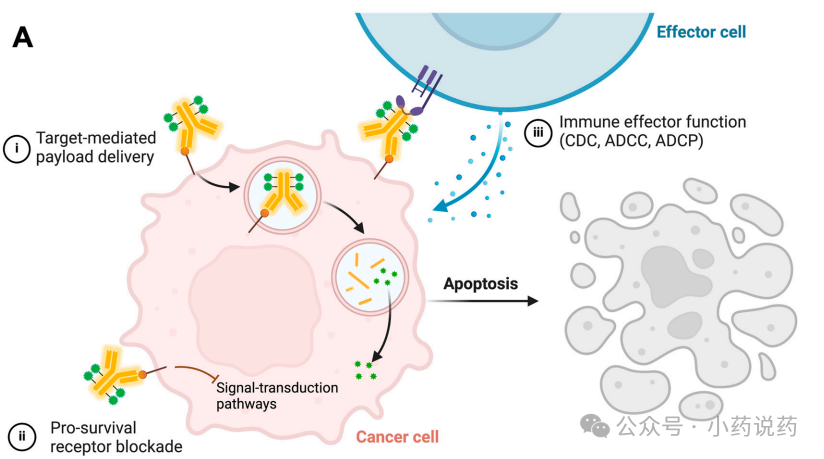
1. 靶点介导的摄取与内化
抗体被期望作为载体,驱动静脉注射ADCs的肿瘤摄取,并通过靶点介导的结合随后内化,选择性地将细胞毒性载荷递送到肿瘤部位。靶点介导的内化被认为是携带不可裂解连接子的ADCs所必需的;因为它们除了抗体代谢外没有其他药物释放机制,必须在溶酶体中代谢以释放其活性载荷。对于携带蛋白酶可裂解连接子或酸不稳定连接子的ADCs,靶向内化抗原的抗体也是首选,它们分别利用细胞内酶或酸性区室(如内体和溶酶体)进行载荷的活性释放。然而,在某些情况下,非内化ADCs也能发挥显著的抗肿瘤疗效。
2. 抗体固有的抗肿瘤活性
在选择用于ADC构建的骨架抗体时,抗体本身的抗肿瘤活性(如直接抑制细胞信号传导和受体多聚化)并不被认为像传统未修饰抗体治疗那样关键,因为ADCs治疗有效性的主要驱动因素是细胞毒性载荷的直接细胞杀伤。尽管如此,某些ADCs中的抗体保留了未修饰原始抗体的作用机制,抗体的直接抗肿瘤活性贡献于ADCs的整体抗肿瘤疗效。两种FDA批准的基于曲妥珠单抗的ADCs——曲妥珠单抗Emtansine和曲妥珠单抗Deruxtecan被认为保留了其骨架抗体曲妥珠单抗的原始机制,包括抑制磷脂酰肌醇3-激酶-AKT信号通路(导致细胞周期抑制剂p27积累和细胞周期停滞)、抑制人表皮生长因子受体2(HER2)裂解/脱落以及诱导抗体依赖性细胞毒性。
3. 免疫效应功能的激活
抗体介导ADCs作用机制的另一个贡献者是免疫效应功能的激活,如抗体依赖性细胞毒性、抗体依赖性细胞吞噬和补体依赖性细胞毒性。抗体支持免疫效应功能的强度取决于其结合Fcγ受体的能力;这种能力在免疫球蛋白G(IgG)亚类之间差异显著。IgG由四个高度保守的亚类组成,它们在重链氨基酸序列、重链和轻链的连接方式、铰链长度以及连接两条重链的二硫键数量上有所不同。在四个亚类中,IgG1能最强有力地结合免疫效应细胞(如自然杀伤细胞和巨噬细胞),引发抗体依赖性细胞毒性和补体依赖性细胞毒性,而IgG2和IgG4的效应功能不足或受限。因此,IgG1是ADCs骨架中最常用的IgG亚类,而一些ADCs使用IgG4或IgG2作为骨架,以在强效载荷与免疫效应功能结合导致的毒性不可耐受时管理整体毒性。
-03-
二、实体瘤中ADC靶抗原的特征
有利的抗原表达谱是抗体成功靶向肿瘤的前提——尽管这还不够。虽然ADCs中使用的抗体不一定需要满足所有这些标准(因为多种机制可参与直接结合抗原之外的过程),但满足这些标准仍有利于ADC的整体表现。
1. 正常组织中的抗原表达
抗原在正常组织上的表达是其适合抗体靶向的关键因素。重要正常组织中有限的抗原表达降低了ADC治疗中抗原依赖性毒性的风险。目前获批用于血液肿瘤的大多数ADC靶向B细胞谱系高度特异的蛋白,在非恶性细胞中表达极少或不表达。与此同时,用于实体瘤的ADCs,其靶蛋白的表达不仅限于恶性细胞,在一定程度上也表达于非恶性组织。然而,这些靶蛋白通常在肿瘤细胞中过表达,有时比非恶性组织高出数个数量级,有前景靶点的选择通常基于这些不同的表达谱进行论证。表达限于非重要器官或细胞群体的抗原仍可能被选为靶点,即使它们在正常和肿瘤组织间无差异表达。
2. 靶点表达水平对疗效的影响
有观点认为:(1)肿瘤有一个支持有效体内靶向和治疗抗体抗肿瘤活性的抗原表达下限;(2)靶抗原的密度或表达水平驱动治疗抗体的肿瘤摄取和空间分布。同样的原则可能适用于ADC治疗;抗原密度可能通过影响递送到肿瘤组织的载荷量来影响ADC的治疗疗效。然而,抗原密度与疗效的关系仍有争议且取决于特定的靶点-抗体组合;此外,该下限似乎低于传统治疗抗体,因为众多其他因素也影响ADC的抗肿瘤活性,如肿瘤和载荷类型、内化速率和效率、连接子化学以及偶联化疗载荷的旁观者效应。靶向实体瘤的抗原表达下限高于血液肿瘤。对于靶向TROP2的Dato-DXd,其药物抗体比(DAR)被调整为4,而其他含DXd的ADCs(如T-DXd、HER3-DXd和CDH6-DXd)的DAR为7-8,这可能是由于与TROP2在正常组织表达相关的药物相关不良事件。
3. 肿瘤类型与遗传因素的影响
除了密度和表达水平,靶抗原的多个其他方面在特定肿瘤类型中使药物递送效率和活性复杂化,并影响ADC的整体疗效。这包括但不限于抗原表达的空间和时间异质性、肿瘤潜在的基因组复杂性以及肿瘤微环境的差异。例如,T-DXd在不同肿瘤类型中表现出不同的活性,HER2表达的乳腺癌比胃癌或结直肠癌更敏感。一种可能的解释是每种肿瘤类型独特的HER2表达模式,HER2蛋白在胃癌中通常表现出比乳腺癌更异质的表达模式。分子亚型对ADC治疗反应的影响证据正在浮现。在DESTINY-Lung01试验的 interim报告中,T-DXd在HER2突变队列的确认客观缓解率(ORR)超过了HER2过表达队列。
4. 获得性耐药机制
除了上述与表达和分子谱相关的固有敏感性/耐药机制外,主要有三种提出的ADC获得性耐药机制:由于抗原表达下调或影响表位识别的转录后修饰导致的抗原丢失;细胞内运输通路的改变;以及载荷耐药,主要通过ATP结合盒转运蛋白的上调。
-04-
三、连接子化学与平台毒性
对于静脉注射的治疗抗体,存在多重障碍阻碍将足量载荷递送到有效治疗实体癌所需的剂量。这些障碍包括但不限于基质屏障(扩散跨间质流体空间对抗压力梯度阻碍大分子运输)和结合位点屏障(抗体成功结合靶抗原阻止其渗透肿瘤)。由于抗体在体内分布体积大、非肿瘤组织特异性摄取竞争以及肝肾代谢清除,99%系统给药的ADCs无法到达肿瘤。因此,虽然靶点介导的抗体摄取驱动抗肿瘤疗效从而降低最低有效剂量,但靶点非依赖性、载荷来源的脱靶、脱肿瘤毒性仍是ADC开发的关键问题。
研究分析了已获批和临床活跃ADCs的最大耐受剂量和/或推荐2期剂量,发现具有常见药物连接子的ADCs往往具有相似的最大耐受剂量和毒性谱,独立于靶点抗体;这被称为“平台毒性”。平台毒性的一个因素是循环中过早释放的未偶联载荷;较高的药物抗体比和可裂解连接子的使用增加了未偶联细胞毒性载荷扩散到循环的可能性。T-DXd和Sacituzumab Govitecan显示出的循环未偶联载荷剂量比携带不可裂解连接子的T-DM1高出10到100倍。与此观察一致,大多数携带可裂解连接子系统的ADCs治疗伴随中度至高度的嗜中性白血球减少症、脱发和胃肠道不良事件,这与释放载荷的毒性不矛盾。
除了连接子系统,偶联化学也部分导致了细胞毒性载荷在循环中的过早释放。构成许多目前获批或开发中ADCs的硫醇-马来酰亚胺化学,可通过逆Michael反应导致整个药物连接子从抗体上脱偶联。逆Michael反应据报道可在7天内以高达50%-75%的比例诱导ADC药物连接子脱偶联。脱偶联的药物连接子反过来迅速与含硫醇的血浆分子(主要是白蛋白)反应形成新偶联物。白蛋白具有长半衰期(平均血清半衰期三周),含药物连接子的白蛋白通过新生儿Fc受体结合的主动循环机制,可能导致直接肿瘤摄取并经逐渐代谢释放载荷。研究表明,引入高稳定性、定点偶联药物连接子修饰的ADCs,其循环半衰期改善,肿瘤摄取更高,血浆稳定性高,且常呈现更高的抗肿瘤活性。
-05-
四、下一代抗体策略
为解决肿瘤渗透和系统毒性问题,额外的努力包括使用下一代载体,如双特异性抗体和条件激活抗体。
1. 基于双特异性抗体的ADCs(BsADCs)
基于双特异性抗体的ADCs通过克服抗原下调和表达异质性相关的耐药,为增强传统ADC疗效提供了有前景的途径。某些BsADCs有望增强抗体内化和/或处理或缓解靶点毒性。目前有10种BsADCs处于临床开发中,其中2种(JSKN003和BL-B01D1)正在III期临床试验中测试。双表位抗体靶向同一靶抗原的两个独立表位,可诱导受体聚集和快速靶点内化。BL-B01D1是一种EGFR×HER3靶向的BsADC,由抗EGFR/HER3的双特异性抗体、组织蛋白酶B可裂解连接子和拓扑异构酶I抑制剂组成。BL-B01D1在经过大量治疗的晚期实体瘤中显示出初步的抗肿瘤活性和可接受的安全性。
2. 其他创新抗体
抗体片段和纳米抗体由于分子尺寸较小,表现出更快的血管通透性和更好的组织渗透,在实体瘤中分布更均匀。VHH偶联药物因其独特的药理优势,包括优越的实体瘤渗透性、增强的稳定性、相对较低的生产成本、易于基因工程改造、格式灵活性、低免疫原性和模块化,可能与传统ADCs竞争。主要缺点包括快速肾脏清除和肾脏滞留。快速清除可能削弱需要在血液中更持久存在的治疗疗效,肾脏滞留可能导致肾小球中载荷集中从而引起肾脏损害。Probodies是融合了自掩蔽部分或具有pH依赖性构象变化的抗原结合位点的IgG分子,旨在减少在正常组织中的结合,提高肿瘤特异性。
-06-
结语
抗体通过靶点介导摄取提供肿瘤特异性、延长细胞毒素循环半衰期以及提供如受体中和、信号通路抑制和免疫效应功能激活等额外机制,在ADC疗效中起关键作用。下一代ADCs有望克服靶点在肿瘤上毒性在非肿瘤上和有限肿瘤渗透的问题,这部分解释了平台毒性。靶点多样化是另一个研究热点,旨在扩大可能受益于这种创新治疗模式的患者群体。
虽然抗体靶点的识别传统上依赖于肿瘤与健康组织间mRNA的差异表达,但基因表达本身并非靶点表达的唯一决定因素,因为存在转录后和翻译后变化。作为替代,通过蛋白质组学方法识别细胞表面抗原可产生具有功能重要性及转化潜力的靶点。
ADCs在过去几十年的出现和发展是肿瘤学的重要进步:ADCs通过提供传统化疗无法达到的疗效水平,改变了多种癌症的治疗。抗体驱动共同递送的细胞毒性载荷的肿瘤摄取,并为提高这种创新治疗模式的肿瘤特异性提供了独特方式。抗体、连接子和载荷的独特组合影响ADC的整体表现;因此,在选择合适的细胞表面靶抗原时,需要从多面视角进行仔细考量。靶点多样化和抗体创新正在快速进展,ADC格局的指数级增长有望根除难以治疗的实体瘤。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
