引言
髓系细胞在癌症中扮演着多重角色,它们既通过血管生成、转移和免疫抑制促进肿瘤进展,又能刺激抗肿瘤免疫。传统上,这种双重功能被归因于细胞异质性,但越来越多的证据表明,髓系细胞可塑性才是癌症的一个更根本的特征。
-02-
一、髓系细胞可塑性的定义与类型
髓系细胞是一个庞大且多样化的群体,包括红细胞、巨核细胞、粒细胞(中性粒细胞、嗜酸性粒细胞和嗜碱性粒细胞)、单核细胞、巨噬细胞、肥大细胞以及树突状细胞(DCs)的髓系亚群。在癌症中,巨噬细胞、单核细胞和粒细胞是免疫调节、肿瘤进展和治疗反应的核心。髓系分化具有高度适应性,这种特性被称为髓系可塑性。在癌症背景下,细胞可塑性在两个相互关联的层面上运作:分化可塑性和功能可塑性。
1. 分化可塑性
分化可塑性是指髓系前体细胞及部分成熟细胞扩增并跨越谱系界限改变命运的能力。在实体瘤中,这表现为粒细胞-巨噬细胞前体(GMPs)的扩增和髓系生成的增加。例如,单核细胞根据微环境信号的不同,倾向于分化为巨噬细胞而非DCs;在病理条件下,淋巴样和单核细胞前体可分化为粒细胞;反之,在紧急髓系生成期间,中性粒细胞定向的前体细胞也可分化为单核细胞。
2. 功能可塑性
功能可塑性是指髓系细胞在不发生谱系身份改变的情况下,其活性发生重大转变。在癌症中,经典的、具有宿主保护功能的细胞可以被重编程为一种病理状态,这种状态的细胞会抑制免疫、促进血管生成并协助肿瘤细胞侵袭。处于这种病理激活状态的细胞被称为髓源性抑制细胞,包括多形核MDSC(PMN-MDSC)和单核细胞MDSC(M-MDSC)亚群,它们具有独特的转录谱、表型特征和功能活性。
-03-
二、癌症中髓系可塑性的调控机制
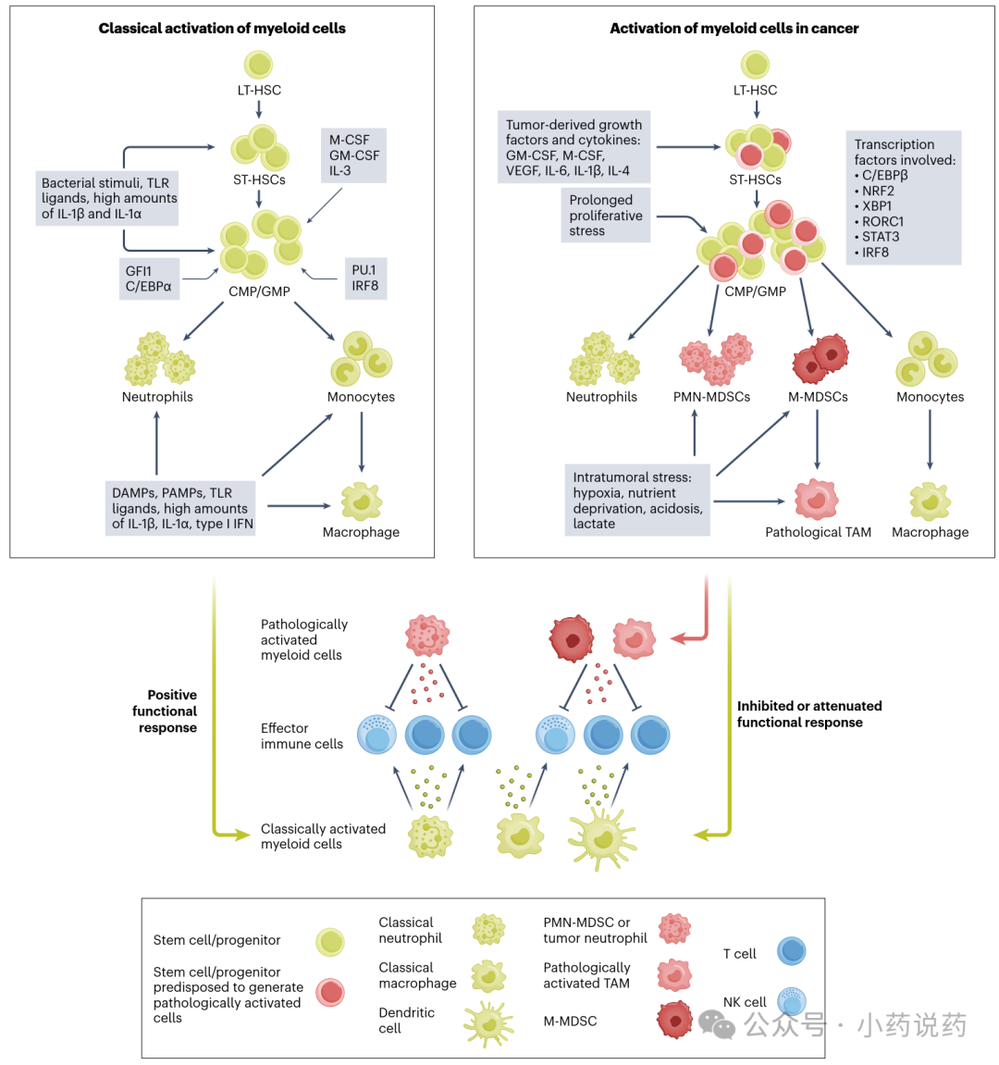
1. 髓系生成的重编程
在急性感染期间,病原体衍生的信号会触发强烈的髓系生成,以迅速扩增髓系细胞保护宿主。而在癌症中,肿瘤衍生的信号驱动适度但持久的髓系生成。这种持续的压力启动了PMN-MDSCs和M-MDSCs的生成,随后M-MDSCs分化为免疫抑制性的肿瘤相关巨噬细胞。近期研究表明,这种重编程始于造血干细胞(HSC)阶段的早期变化。
在GMP阶段,正常的嗜中性粒细胞定向以IRF8下调、GFI1表达和C/EBPα上调为特征。GFI1抑制IRF8和EGR1,阻断单核细胞程序同时激活嗜中性粒细胞基因。在癌症中,GMPs中IRF8和视网膜母细胞瘤蛋白水平的降低使嗜中性粒细胞偏向PMN-MDSCs。IL-1家族细胞因子介导癌症相关的髓系生成并使前体细胞偏向免疫抑制命运。例如,IL-1β促进乳腺癌模型和患者中的粒细胞生成,而阻断IL-1β可部分逆转这种效应并减少小鼠模型中的转移。
2. 肿瘤微环境(TME)的塑造作用
髓系细胞在癌症中的功能状态取决于TME中的许多因素,包括细胞因子环境、缺氧、肿瘤类型和分期。中性粒细胞是功能可塑性的典型例子。虽然PMN-MDSCs的功能状态通常与癌症患者的不良临床预后和对治疗的反应降低有关,但在特定条件下,中性粒细胞也可以促进抗肿瘤效应。例如,在小鼠肉瘤模型中,肿瘤诱导前消耗中性粒细胞与非常规T细胞缺乏激活有关,这对防止肉瘤发展至关重要。在大多数情况下,中性粒细胞的抗肿瘤效应是在治疗干预后观察到的。
单核细胞和巨噬细胞也表现出功能二分法。虽然在癌症早期阶段存在促进抗肿瘤反应并是治疗反应所需的亚群,但也存在免疫抑制和促肿瘤的亚群。研究表明,巨噬细胞的功能比转录簇或基于生物标志物的亚群更具定义性,这意味着定位而非特定表型决定了巨噬细胞的功能。触发受体2(TREM2)已被确定为小鼠癌症模型和人类癌症中免疫抑制性TAMs的表型和功能标志物。
3. 对癌症治疗的反应
髓系细胞可塑性不仅取决于肿瘤演变,还取决于治疗类型。这在分析免疫检查点抑制剂(ICIs)等免疫治疗药物后的肿瘤浸润髓系细胞时尤为明显。抗CD40或抗PD-1治疗可诱导表达高水平L-选择素(CD62L)的特定中性粒细胞亚群在小鼠体内积累。这些细胞刺激DCs产生IL-12,并在体外对癌细胞表现出细胞毒性活性。抗CTLA4和抗OX40治疗抗体的组合已被证明能诱导一种抗肿瘤中性粒细胞亚群,其特征是增强的激活特征,包括IL-1β和干扰素的产生及反应性。
DNA损伤反应(DDR)抑制剂对TME中髓系细胞的调节作用也日益明显。聚腺苷二磷酸核糖聚合酶(PARP)抑制剂奥拉帕利已被证明能重塑TME中的巨噬细胞浸润,主要促进促炎性巨噬细胞表型。耗竭免疫抑制性巨噬细胞可增强奥拉帕利在小鼠中的疗效。另一种DDR抑制剂——共济失调毛细血管扩张症和RAD3相关蛋白(ATR)抑制剂cerasertib,通过显著减少M-MDSCs和TAMs并消除PMN-MDSCs的免疫抑制活性,重塑了肿瘤内的髓系细胞区室。布鲁顿酪氨酸激酶(BTK)抑制剂依鲁替尼对单核细胞和TAM表型及功能产生细微影响,并在体内耗竭MDSCs,从而改善ICIs和CAR-T细胞疗法的疗效。
-04-
三、髓系细胞可塑性的治疗靶向策略
1. 巨噬细胞和M-MDSC的重编程
针对M-MDSCs和TAMs关键调节因子的治疗药物已在多种癌症中进行了测试。靶向CSF1R–CSF1轴是研究最广泛的策略,包括小分子CSF1R抑制剂(如培西达替尼)和抗CSF1R抗体等。尽管这些治疗在CSF1驱动的疾病——腱鞘巨细胞瘤中产生了明确的临床疗效,但在实体瘤中的总体结果令人失望。CSF1R抑制在临床上减少了TAM/M-MDSC含量,耗竭了CSF1R依赖的库普弗细胞并调节了肝酶,表明靶点接合。有限的临床获益可能反映了多种因素,包括因肝毒性导致的剂量限制,这减少了通路抑制,PMN-MDSCs的代偿性扩增以及抗肿瘤TAM亚群的附带耗竭。
靶向单核细胞趋化因子受体CCR2的早期研究也结果不一。在胰腺癌中,CCR2抑制剂PF-04136309与FOLFIRINOX联合是可耐受的并显示出令人鼓舞的活性,而与吉西他滨联合白蛋白紫杉醇联用则无益处且耐受性降低。TREM2阻断剂(如PY314抗体)正用于重编程肿瘤相关髓系表型。TREM2在胶质母细胞瘤中尤为相关,支持免疫抑制性髓系状态。然而,在三阴性乳腺癌和卵巢癌中的发现表明,TREM2表达可以标记抑制性和抗肿瘤髓系群,且叶酸受体2(FOLR2)阳性的髓系细胞在某些情况下可能代表更主要的抑制性亚群。
2. 中性粒细胞和PMN-MDSC的靶向
靶向中性粒细胞和PMN-MDSCs面临独特的挑战,主要因为缺乏可操作的机制来直接调节这些群体。大多数临床努力使用CXCR2配体中和抗体和小分子拮抗剂。抗IL-8抗体(BMS-986253)与免疫疗法联合测试降低了血清IL-8水平,但未显示疗效信号。CXCR2小分子抑制剂已在多种联合方案中进行了探索。AZD5069在去势抵抗性前列腺癌患者亚群中产生了令人鼓舞的信号,但在胰腺癌或头颈癌中未显示明确的临床活性。SX-682在免疫治疗后转移性黑色素瘤的II期研究中显示出有希望的效果后,正在多项II期试验中研究。
3. 靶向细胞内通路
MDSC分化受多个信号节点影响,其中两个已从临床前研究进入临床试验:磷酸肌醇3-激酶γ(PI3Kγ)和JAK-STAT信号传导。PI3Kγ抑制剂eganelisib/IPI-549在头颈鳞状细胞癌、三阴性乳腺癌、肾细胞癌和非小细胞肺癌中进行了评估,主要与ICIs和化疗联合。转录特征表明,eganelisib-阿替利珠单抗联合重塑了TME,改变了表达CXCL9的TAMs与SPPI+TAMs的比例,并产生了更均匀的外周免疫细胞激活。
JAK抑制剂鲁索替尼在霍奇金淋巴瘤的I期试验中显示出有希望的活性,增强了ICI反应。除了T细胞调节外,该治疗还调整了外周中性粒细胞与淋巴细胞比率。另一种靶向JAK–STAT的方法使用STAT3反义寡核苷酸danvatirsen下调巨噬细胞和M-MDSCs中的STAT3。Danvatirsen主要被巨噬细胞、调节性T细胞和内皮细胞摄取,而非肿瘤细胞,提供了对抑制性巨噬细胞的选择性。
4. 靶向免疫抑制代谢物
精氨酸酶在髓系细胞中过表达,其增强的精氨酸转化为尿素和鸟氨酸被认为限制T细胞和自然杀伤(NK)细胞功能。在一项Ib期试验中,精氨酸酶抑制剂INCB001158与帕博利珠单抗联合调节了外周精氨酸水平,但在头颈鳞状细胞癌和胆道癌中未观察到临床活性。吲哚胺2,3-双加氧酶(IDO)将色氨酸转化为犬尿氨酸。色氨酸耗竭损害T和NK细胞功能,而犬尿氨酸激活芳烃受体和一般控制非抑制性2(GCN2)激酶。多种IDO抑制剂试验结果为阴性,突显了通路冗余,这可能包括色氨酸2,3-双加氧酶(TDO)表达补偿IDO阻断。
-05-
三、面临的挑战与未来方向
1. 冗余性与毒性
为什么多种针对髓系细胞的策略未能产生一致的临床获益?证据表明,广泛的细胞和信号冗余削弱了治疗效果。解决这一问题的方法包括同时靶向多个髓系细胞群体,如将CSF1R抑制剂与CXCR2拮抗剂联合靶向PMN-MDSCs,或在TAMs中上调C/EBPα并抑制PMN-MDSCs中的脂肪酸转运蛋白2(FATP2)。然而,这些方法带来相当大的靶向脱靶毒性风险,可能导致毒性并限制有效剂量。髓系定向疗法不太可能显示出有意义的单药活性,其最大益处预期来自与其他治疗的联合。
2. 选择性与精准治疗
最有希望的策略是靶向选择性与病理性髓系细胞相关的分子和通路。这种方法可以减少毒性,同时保留抗肿瘤的、经典激活的TAMs、单核细胞和中性粒细胞。例如,病理性髓系细胞上内质网应激相关的DR5上调、PMN-MDSCs而非经典多形核中性粒细胞中FATP2的表达,以及PMN-MDSCs上CD300LD的表达。最终目标是将癌症中的髓系细胞从病理激活的促肿瘤细胞转变为抗肿瘤的经典激活细胞。
3. 疾病阶段与治疗时机
髓系细胞在肿瘤演变的不同阶段具有不同的作用。在患有确定疾病的患者和携带肿瘤的小鼠中,髓系细胞主要是免疫抑制和促肿瘤的。然而,在肿瘤负荷非常低的情况下——特别是在有效的免疫治疗后——正常的髓系细胞可能是有益的,并可能发挥抗肿瘤活性。因此,临床试验中常用的连续给药模式可能忽略了髓系细胞反应的时间复杂性。阐明中性粒细胞和其他髓系亚群何时最相关将是优化治疗时机和完善患者选择的关键。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
