引言
上皮-间质转化(EMT)是癌症细胞可塑性的核心驱动力,它赋予肿瘤细胞侵袭、免疫逃避、治疗抵抗和转移的能力。EMT并非一个二元开关,而是一个包含瞬时、可逆状态的连续谱系,这些状态赋予肿瘤细胞独特的功能特性。近期技术进步揭示了不同肿瘤背景下EMT状态的意外多样性,这对疾病进展和治疗反应具有重要意义。
-02-
一、EMT概述
1. EMT的本质与生理病理背景
EMT是后生动物中广泛存在的过程,使上皮细胞能够获得间质特征,包括前后极性、运动能力和抗细胞死亡能力。该过程最初在原肠胚形成和神经嵴迁移的背景下被描述,此后被证实广泛参与从器官发生和组织修复到纤维化和癌症等多种生理和病理过程。EMT并不总是完全转化为间质状态,也不完全消除上皮特征,特别是在体内,它涉及上皮细胞向更具可塑性和迁移性状态的有序、部分重编程。
在胚胎发育中,经历EMT的细胞获得迁移特性,并在精确发育线索的引导下参与中胚层、内胚层、神经嵴衍生物和其他谱系的形成。在成年期,瞬时EMT激活在组织修复中具有关键作用。当慢性激活时,EMT变得病理化,促进组织结构破坏、细胞去分化、基质重塑和炎症,导致纤维化发生。下图展示了非转化上皮细胞在不同条件下的两种EMT程序:胚胎期的侵袭性EMT和成体响应损伤的炎症性EMT。
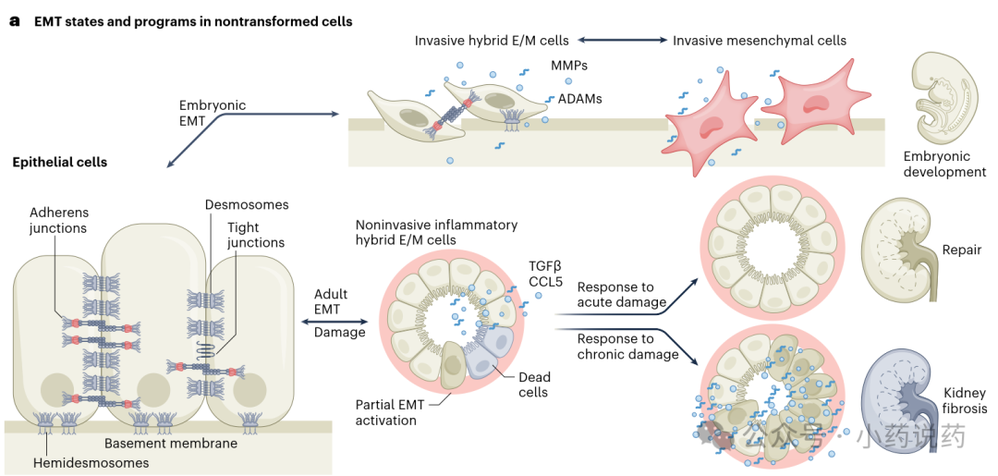
2. 核心调控机制
EMT程序的核心是一组转录因子,最著名的是SNAIL、TWIST、ZEB和PRRX家族成员。这些EMT转录因子抑制上皮基因的转录并激活间质程序,重塑细胞骨架,改变细胞-基质相互作用并破坏细胞-细胞粘附。
EMT-TF的表达由多种信号通路诱导,包括由转化生长因子-β(TGFβ)或WNT受体、Notch或受体酪氨酸激酶触发的通路。环境因素如缺氧和机械力,或细胞内信号如对DNA损伤的反应、氧化应激或代谢重编程也能诱导其表达。下图展示了EMT的激活机制,包括外部信号通路、环境因素和细胞内信号的汇聚。
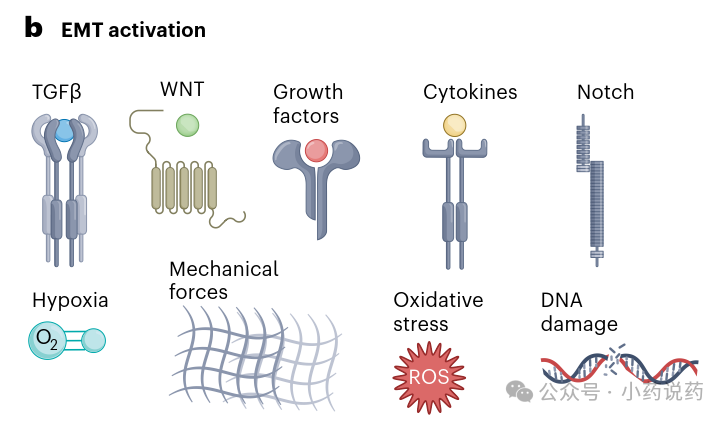
此外,EMT还受到转录后调控,包括通过miR-200家族和miR-34等microRNA、可变剪接以及与染色质修饰物的相互作用。对不同发育和癌症模型中EMT进程的系统分析揭示了EMT-TF的刻板顺序激活:SNAIL1作为先驱调控因子抑制上皮特征,而TWIST和PRRX1等更强效的间质诱导因子通常在EMT后期被招募,诱导侵袭特性。下图形象地展示了这种EMT-TF的顺序招募过程,箭头指示方向,线条宽度表示激活或抑制强度。
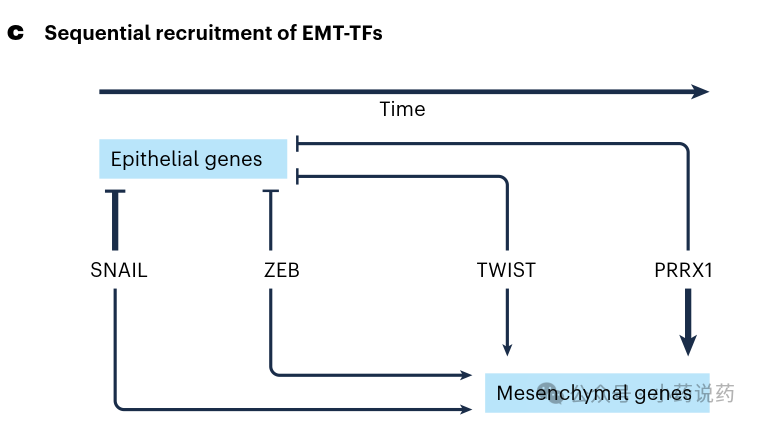
3. EMT作为多维连续谱
EMT更准确地被描述为由不同调控模块控制的多维细胞状态连续谱。细胞可以采用部分EMT配置,同时表达上皮和间质标志物并显示杂合表型。允许单细胞分辨率的技术发展使这些杂合状态的特征化更好,它们在EMT景观中可以是稳定或亚稳态的。EMT通常是可逆的,细胞经历间质-上皮转化(MET)。细胞在整个历史中可以参与连续的EMT/MET循环,MET的成功需要EMT-TF的下调。
EMT日益被认为是细胞可塑性的驱动力,即细胞适应其身份和行为以响应内在或环境线索的能力,这被认为是癌症的一个标志。EMT通过解锁末端转录程序赋予分化细胞可塑性,无论是在癌症中还是在组织修复或退化中。与依赖于不可逆突变的遗传进化不同,表型可塑性使细胞在选择性压力下迅速转换,增强细胞适应性。
-03-
二、EMT在癌症进展中的作用
1. EMT在肿瘤起始中的作用
自20世纪80年代发现第一个癌基因以来,癌症的起始和进化一直与突变紧密相连。然而,过去十年的研究表明,突变本身不足以触发肿瘤起始。我们的身体可以被理解为一个巨大的克隆镶嵌体,我们在几个组织中携带大量具有癌症相关突变的克隆。致癌物通过扩增具有预先存在驱动突变的克隆来促进肿瘤发生,而不一定直接引起突变。
克隆扩增不足以形成肿瘤,细胞需要绕过额外的瓶颈,如癌基因诱导的衰老或免疫清除。EMT的激活可以赋予癌细胞肿瘤起始能力,同时赋予对凋亡或癌基因诱导的衰老的抵抗力。SNAIL1作为EMT激活的先驱调控因子,在从非转化到转化细胞的过渡中起关键作用。通过多模态单细胞测序,在BRCA突变的乳腺癌中识别出一种肿瘤前状态,其特征是在缺乏驱动突变的情况下存在深刻的表观基因组失调,这种状态由SNAIL1激活和部分EMT标记,充当非转化和转化细胞之间的桥梁。
EMT激活可能作为一个早期的“状态设定”事件,与癌基因突变合作,并在某些情况下先于突变,创造一个有利于肿瘤发生程序稳定的允许性细胞景观。下图展示了肿瘤发生的多阶段过程,从遗传镶嵌到克隆生长、细胞丢失,最终肿瘤启动,其中EMT激活和肿瘤干细胞特性是关键环节。
此外,EMT诱导的染色质重塑在非常早期阶段增加基因组不稳定性,影响随后的进化轨迹。
环境因素也与癌症风险增加相关并触发EMT。例如,尼古丁在小鼠肺纤维化模型中通过激活STAT3–BDNF–TRKB信号通路导致TWIST激活。空气污染中的颗粒物质通过激活ETS-1和NF-κB诱导肺癌细胞系的EMT样状态。肥胖和动情周期等全身状况也与EMT激活有关。
2. 原发肿瘤中的EMT异质性
肿瘤表现出高度的肿瘤内异质性(ITH),这被认为源于遗传差异。然而,遗传异质性本身不能完全解释转移行为,因为除了原发肿瘤中已有的突变外,未发现转移特异性驱动突变。细胞可塑性产生了ITH的额外层面,即遗传相同的细胞采用不同的转录程序。
EMT在部分肿瘤细胞中的激活构成了这种功能异质性来源,长期与增加的侵袭特性相关。单细胞RNA测序揭示了多种癌症类型中EMT状态的存在,确认了其在体内动物模型和癌症患者中的激活。值得注意的是,中间EMT状态与增加的转移潜力相关。在乳腺癌中,仅占肿瘤细胞约1.5%的罕见基底/干细胞样EMT群体表现出不成比例的高转移能力。
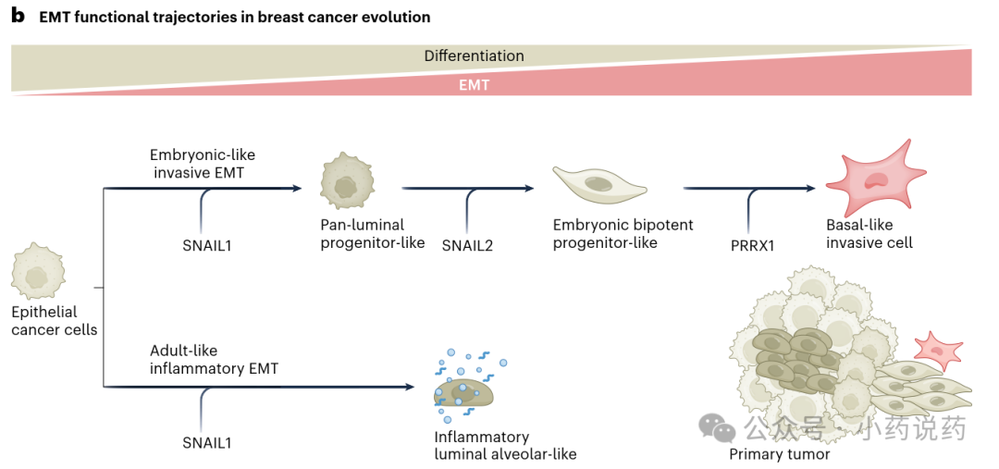
EMT驱动的异质性在体内表现为沿上皮-间质谱系分布的一系列细胞可塑状态。上图展示了乳腺癌进化中的EMT功能轨迹:上皮癌细胞经SNAIL1调控去分化,形成两种不同的EMT路径。一条是“胚胎样轨迹”,细胞继续去分化获得祖细胞样表型,最终在PRRX1作用下成为基底样侵袭性细胞;另一条是“成体样炎症轨迹”,细胞被重编程为与抗肿瘤免疫浸润相关的炎症样状态。这两种群体在同一肿瘤内占据不同的空间位置:侵袭性程序细胞富集在肿瘤-基质界面,而炎症程序细胞位于肿瘤内部。
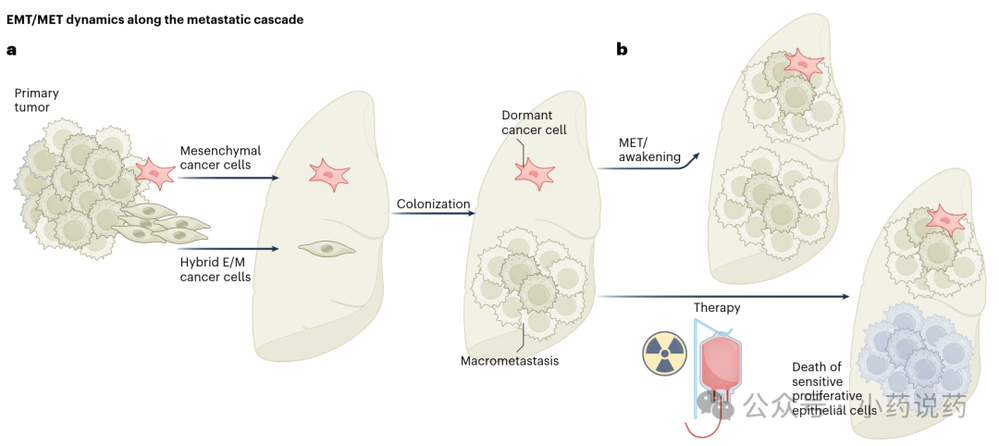
功能分析表明,耗竭PRRX1不仅显著减少转移负担,还导致向炎症EMT程序转变,伴随抗肿瘤巨噬细胞浸润增加。这表明两种EMT程序是可塑且相互依赖的,功能上相互拮抗:侵袭程序促肿瘤,而炎症程序发挥抗肿瘤作用。下图展示了EMT在转移级联反应中的动态变化,杂合型和间质型癌细胞离开原发灶,杂合型细胞定植能力更强,而间质型细胞常处于休眠状态。
3. EMT与转移
一旦癌细胞激活EMT并获得侵袭特性,它们可以渗入血液循环,成为循环肿瘤细胞。CTCs可以作为单个细胞或集群存在,后者显示出更高的转移潜力。CTCs存在于杂合EMT状态,同时表达上皮和间质标志物,并与增强的肿瘤起始能力、可塑性和治疗抵抗相关。
虽然EMT⁺细胞可在已建立的转移灶中发现,但大多数转移细胞是EMT⁻,反映了仅使用两个标志物解释完整EMT谱系的局限性,或MET/上皮样状态是转移定植所必需的。整合单细胞RNA测序与CRISPR谱系追踪的研究证实,转移主要源于原发肿瘤中激活EMT的克隆,特别是晚期杂合EMT状态的克隆。
完全间质状态虽然具有更高的侵袭能力,但在实验性转移测定中转移潜力较低,而杂合EMT表型显示出增加的转移潜力。低表达或下调EMT-TF被确定为某些模型中转移的必要步骤,支持了MET或EMT的部分逆转是有效转移生长所需的观点。谱系追踪研究表明,很少有转移源于经历MET的高度间质克隆;相反,转移克隆起源于具有中间EMT激活的小群体。
同时,散播细胞可以进入非增殖状态,通常称为休眠。休眠癌细胞通常显示间质状态,与高度间质癌细胞转移潜力低的研究结果一致。EMT激活和休眠程序在原发肿瘤内已协调,例如PRRX1赋予侵袭能力的同时诱导细胞周期停滞和休眠相关基因表达。
4. EMT与转移微环境的相互作用
成功的转移定植需要间质癌细胞至少部分重新获得上皮特征。微环境信号在转移位点诱导强烈EMT激活可能削弱其增强的转移潜力。下图展示了EMT-肿瘤微环境在转移位的相互作用。
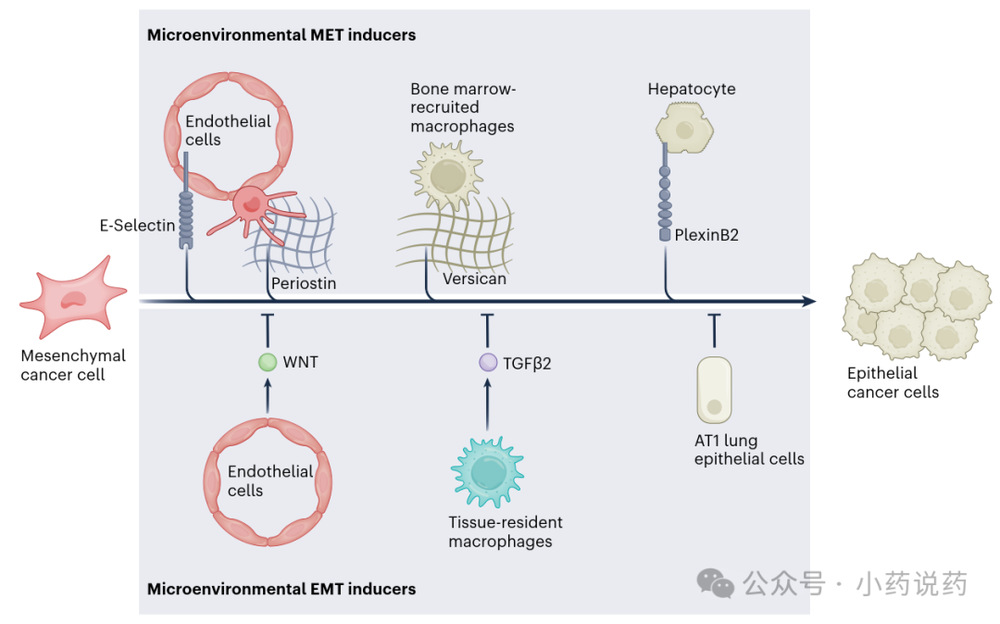
血管周微环境是散播癌细胞遇到的第一个微环境。内皮细胞表达的E-选择素通过结合表面糖蛋白促进乳腺癌细胞骨转移定植中的MET。肺内皮细胞的WNT信号反应性被确定为散播癌细胞休眠的关键决定因素。血管生成活动的程度在此背景下至关重要,内皮细胞通过血栓调节蛋白-1分泌促进休眠,而尖端细胞分泌TGFβ1和骨膜蛋白促进肿瘤生长。
髓系细胞也调节上皮/间质可塑性。组织驻留巨噬细胞分泌的TGFβ2可通过TGFβR3信号维持散播癌细胞的休眠状态。招募的巨噬细胞沉积的聚集蛋白通过下调磷酸化SMAD2促进肺部MET,增强转移生长。癌细胞与非转化上皮细胞的相互作用也有重要作用,如与AT1⁺肺上皮细胞相互作用诱导SFRP2表达,激活促生存、非增殖的部分EMT样程序。此外,肝细胞表达的PlexinB2与癌细胞分泌的信号素结合,诱导MET并驱动转移定植。
-04-
三、EMT与免疫监视
EMT状态对免疫监视和免疫治疗反应有重要影响。EMT特征在人类数据集中一直与免疫抑制相关。下图展示了EMT在免疫抑制中的细胞自主和非自主作用。
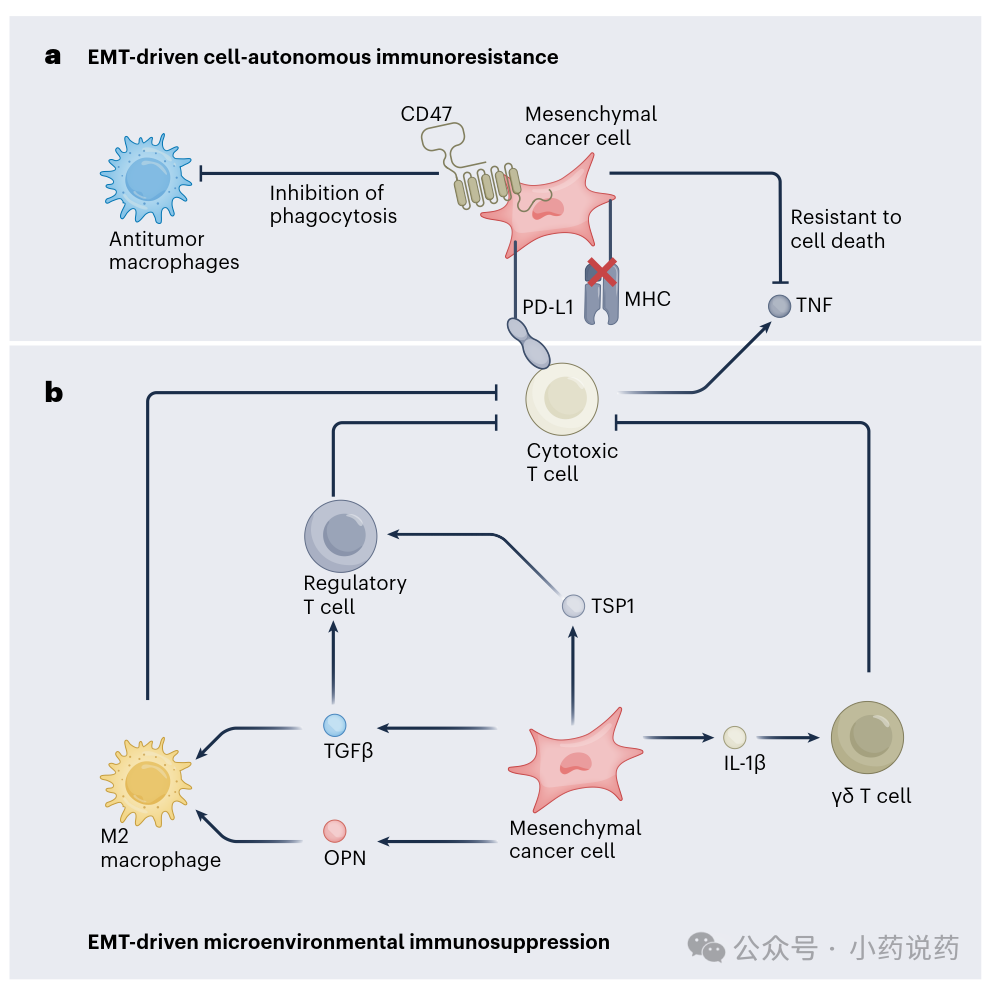
EMT-TFs SNAIL1和ZEB1直接激活CD47表达,这是一个抑制巨噬细胞吞噬的“别吃我”信号。这些转录因子还诱导免疫检查点配体如PD-L1的表达,直接损害T细胞功能。图5a展示了EMT驱动的细胞自主免疫抵抗机制,如CD47和PD-L1的上调。
另一个关键机制是抗原呈递的抑制,可通过下调MHC或免疫蛋白酶体的改变实现。TCF4被证明抑制抗原呈递机制表达同时诱导EMT,导致黑色素瘤去分化。间质状态的内在特征也使癌细胞对免疫介导的杀伤更具抵抗力,如EMT赋予对TNF等促死亡信号的抵抗力。E-钙粘蛋白的伴随丧失可能损害与T细胞有效免疫突触的形成。
EMT不仅赋予癌细胞免疫抵抗力,还促进免疫抑制性肿瘤微环境的建立。SNAIL1激活通过TSP1分泌增强调节性T细胞的招募,抑制细胞毒性CD8⁺ T细胞活动。高SNAIL1表达的间质癌细胞分泌TGFβ1、OPN和巨噬细胞集落刺激因子等免疫调节因子,生成富含M2巨噬细胞和调节性T细胞、耗竭细胞毒性CD8⁺ T细胞的抑制性微环境。图5b详细描绘了间质癌细胞通过分泌多种因子诱导免疫抑制微环境的机制。值得注意的是,一小部分间质细胞足以建立这种免疫抑制环境,保护邻近非EMT癌细胞免受免疫攻击。
-05-
四、新兴治疗策略
由于EMT是转移级联的核心步骤,许多团队尝试抑制或调节它以期预防或治愈转移。EMT赋予对标准化疗、放疗和免疫治疗的抵抗力。有效的EMT靶向不仅可能减少转移,还可能增强现有药物疗效。
1. 直接靶向EMT主调控因子
EMT-TFs长期被认为是“不可成药”的,大多数抗EMT策略未包含专门设计的分子。然而,蛋白降解剂,包括分子胶水和蛋白水解靶向嵌合体(PROTACs),通过将蛋白拉近E3泛素连接酶诱导泛素化和降解,可能为靶向EMT-TFs提供有效方法。下图展示了PROTAC降解特定EMT-TFs从而预防或减弱EMT的机制。
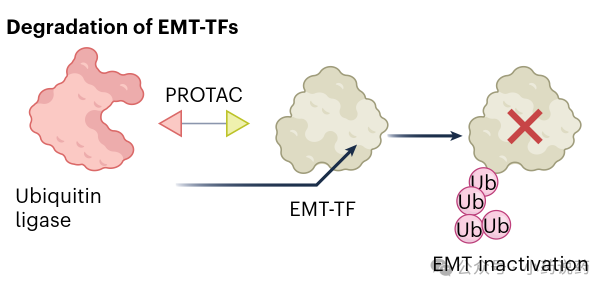
转录因子化学诱导邻近剂(TCIPs)通过将近邻的致癌转录因子重定向至具有相反活性的表观遗传调节因子,重编程其活性。下图展示了分子胶诱导EMT-TF与表观遗传调节因子结合,导致转录重编程的机制。
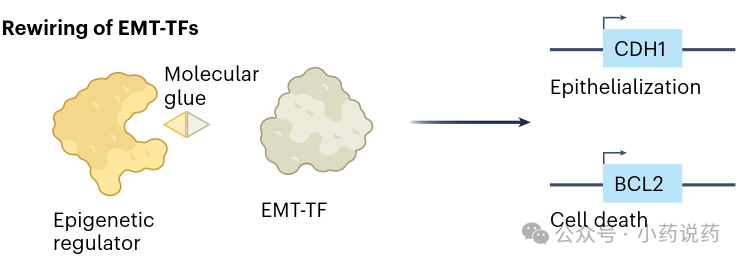
2. 利用间质状态的获得性脆弱性
EMT程序不仅赋予细胞运动和抗死亡能力,还引入了新的脆弱性。
铁死亡是一种非凋亡性细胞死亡程序,依赖于细胞内铁。间质细胞由于细胞内铁浓度高于上皮细胞,表现出对铁死亡的增加敏感性。ZEB1激活合成多不饱和脂肪酸的酶并下调合成单不饱和脂肪酸的酶,增加脂质过氧化敏感性。下图展示了利用GPX4抑制剂等铁死亡诱导剂选择性消除经历EMT细胞的机制。
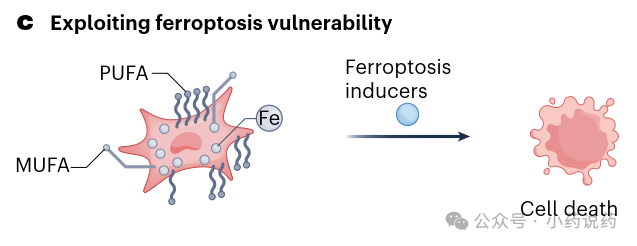
癌细胞重编程是另一种策略。间质癌细胞具有可塑性,可产生不同细胞谱系。将癌细胞转化为不分裂的脂肪细胞可减少侵袭和转移。下图描绘了通过腺病毒介导将分化细胞重编程为惰性细胞类型的过程。
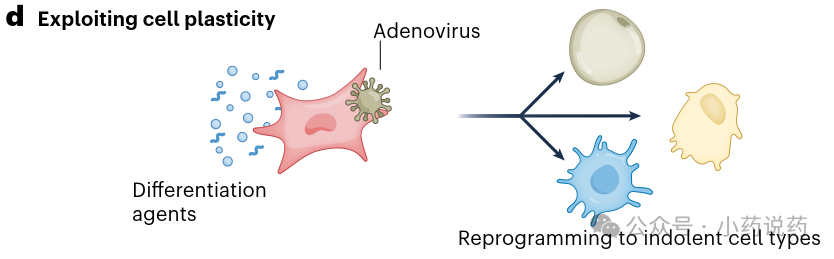
3. 利用EMT程序的可塑性和相互依赖性
肿瘤部署至少两种截然不同但相互依赖的EMT程序。由于成人样EMT与促炎反应和抗肿瘤髓系细胞招募相关,促进这种EMT类型可能比完全抑制EMT产生更高的治疗益处。抑制侵袭性EMT(如通过Prrx1基因缺失)可增强炎症程序,提供双重优势:减少散播和增加抗肿瘤免疫浸润。下图展示了通过调节EMT程序,如抑制侵袭轨迹并促进炎症轨迹,从而改变肿瘤微环境的策略。
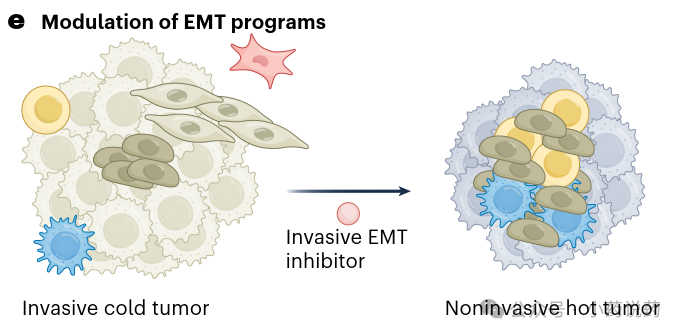
4. 免疫治疗与逻辑门控CAR T细胞
免疫疗法,特别是免疫检查点阻断,已改变多种实体瘤的治疗。然而,EMT异质性极大影响免疫治疗反应。在皮肤鳞状细胞癌中,沿EMT谱系不同阶段的细胞激活不同的T细胞检查点:上皮样细胞主要参与PD-1–PD-L1轴,而杂合和间质细胞激活CTLA-4–CD80和TIGIT–CD155。
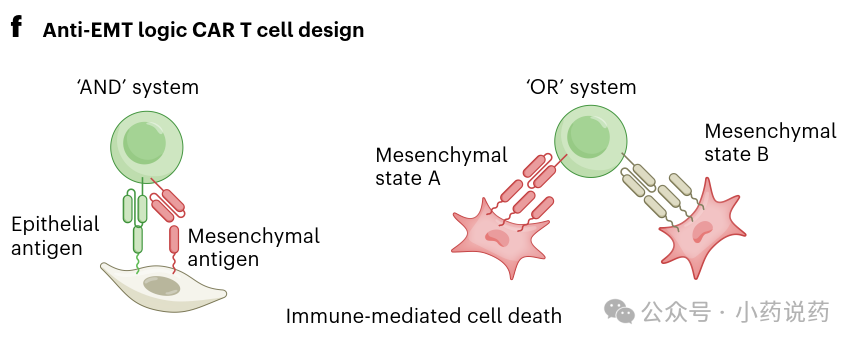
逻辑门控CAR T细胞提供了选择性靶向EMT⁺细胞的前景。‘AND’门需要同一细胞上存在两个抗原才触发细胞毒性。设计特异性靶向同时表达上皮和间质标志物的细胞的CARs,可摧毁杂合上皮/间质细胞。‘OR’门CAR设计使同一细胞能独立识别多种抗原,适合应对肿瘤群体内的抗原异质性。下图展示了抗EMT逻辑CAR T细胞设计,包括AND系统和OR系统的示意图。
5. 合理设计联合疗法
单独靶向EMT临床获益可能有限,但与EMT赋予抵抗力的疗法联合具有更大前景。合理设计的联合策略,包括时间和顺序,至关重要。
EMT赋予细胞对多种细胞毒性药物的抵抗力,EMT抑制增强多肿瘤类型的化疗疗效。EMT通过ZEB1–USP7–CHK1轴更有效地修复DNA损伤,促进放疗抵抗。下图展示了联合策略的多样性,包括与化疗、放疗、免疫疗法及靶向特定状态的药物(如铁死亡诱导剂)的结合。
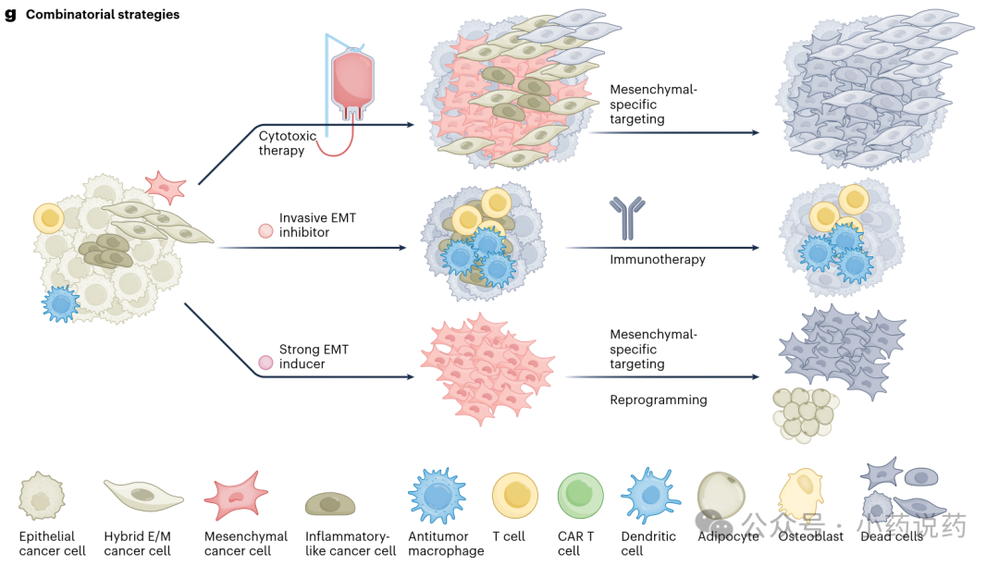
此外,将肿瘤驱动至均质稳定的间质状态可能使其转移性降低,并更易受特异性间质靶向(包括铁死亡或靶向间质抗原的CAR T细胞)影响。药物给药的时间可能至关重要,因为细胞可塑性在治疗期间可能进化。一种策略是使用标准疗法消除敏感克隆,随后使用EMT导向药物根除耐药间质亚群。
-06-
结语
EMT是肿瘤可塑性的关键驱动力,调节侵袭、免疫逃避、治疗抵抗和转移能力。EMT涵盖一个连续谱系,其中杂合状态主导转移定植,而完全间质状态有利于休眠和生存。这些动态与肿瘤微环境紧密相连,可诱导EMT或在其逆转中发挥作用。EMT异质性使生物标志物解释复杂化并影响治疗反应,强调了EMT知情临床策略的必要性。治疗努力正从全局EMT抑制转向利用间质脆弱性或利用可塑性进行重编程,并结合合理的治疗顺序。未来的挑战包括更好地理解EMT在癌症起始中的作用、其在未经治疗与经治疗肿瘤中的功能异质性影响、其与休眠的关系,以及如何将这种复杂性整合到临床决策中。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
