▎Armstrong
2026年5月8日,安进在Clinicaltrials.gov网站上注册了GIPR抗体偶联GLP-1新药AMG 133(Maridebart Cafraglutide)用于GLP-1治疗后的维持治疗三期临床试验MARITIME-SWITCH。
该三期临床计划入组300例受试者,预计2028年1月完成。

该三期临床入组标准为BMI≥25(非30以上的肥胖标准)且GLP-1治疗后减重幅度超过10%的人群。

从主要终点和次要疗效终点来看,该三期临床的目标是通过AMG 133来保持GLP-1的减重效果,即控制反弹。
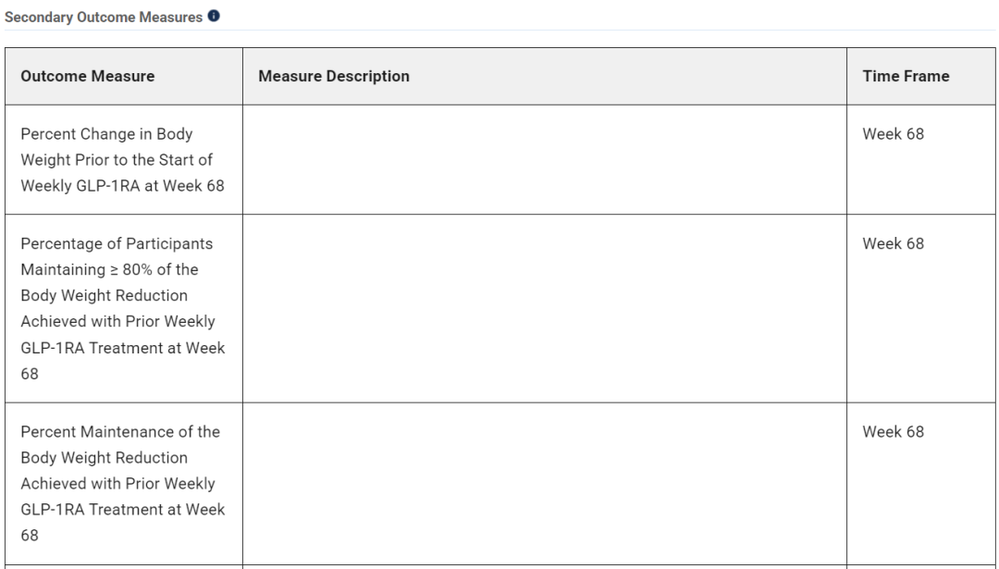
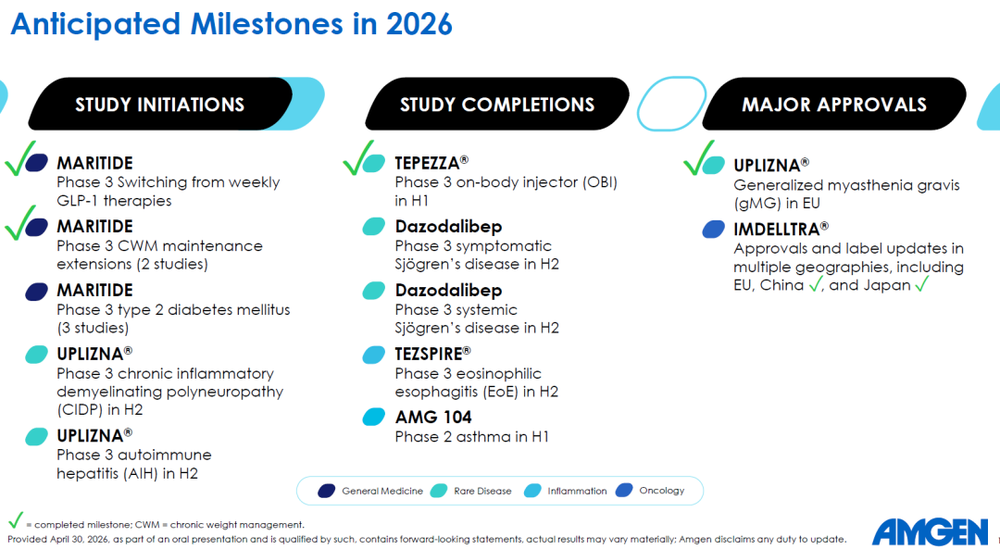
安进在一季度财报中已经明确指出,还将启动两项长期体重维持治疗的三期临床。可见,安进已经将AMG 133的一个应用场景重点锁定在维持治疗上。
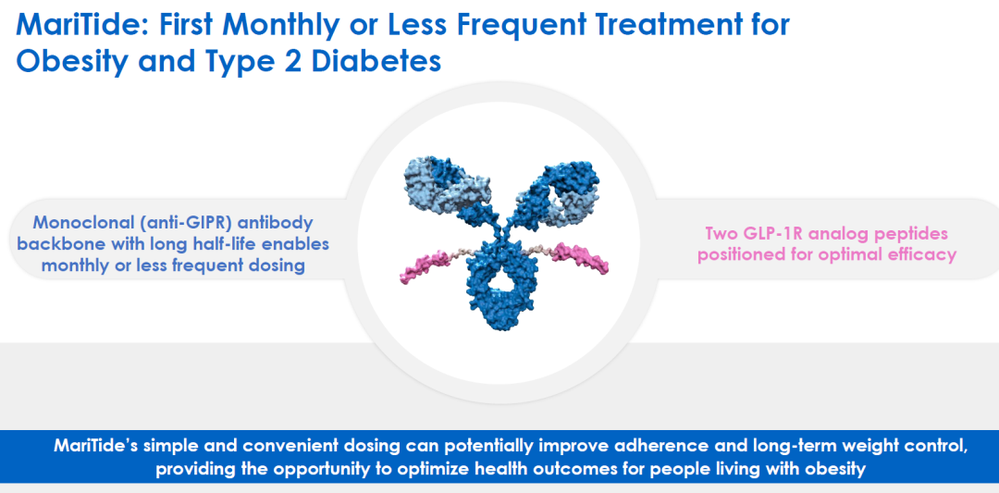
不同于替尔泊肽等采用GIP激动剂,AMG 133为首创的GIPR拮抗剂抗体偶联GLP-1,作用机制刚好相反。
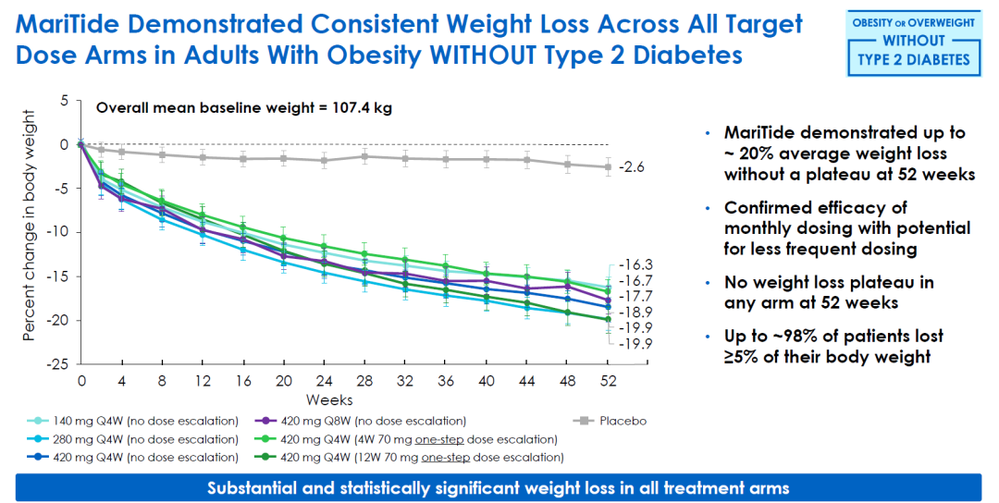
AMG133在二期临床中表现出相当于替尔泊肽的疗效,且只需要每个月给药一次。
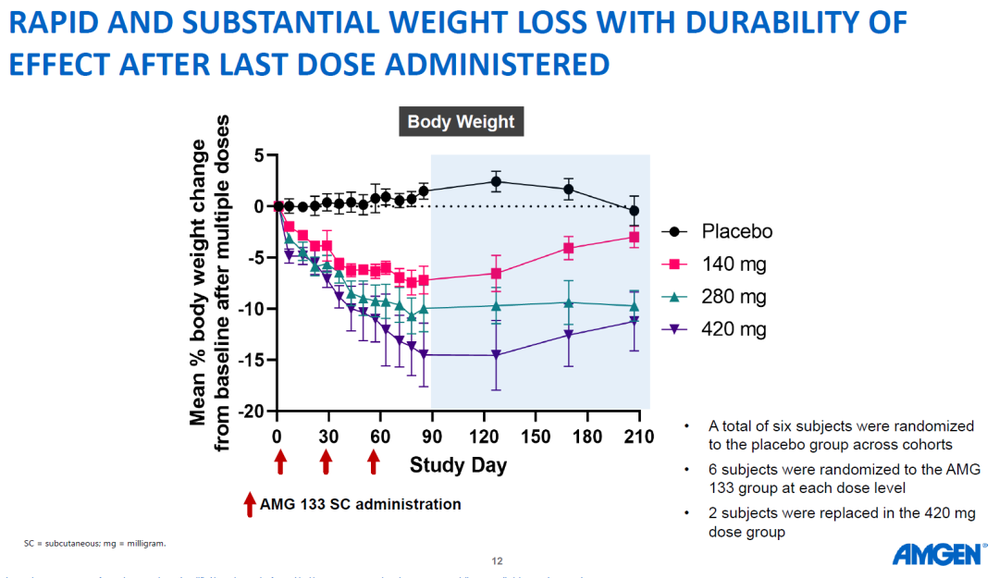
从一期临床披露的数据来看,AMG 133停药后反弹很小,完全不同于其他GLP-1单靶点或GLP-1/GIP双靶点激动剂类产品,这应该也是安进重点推进维持治疗控制反弹的核心原因。
总结
随着司美格鲁肽、替尔泊肽、Orforglipron等在减重领域的广泛应用,其胃肠道副作用、停药反弹的痛点也成为真实的临床需求。AMG 133耐受性较好,且给药频率更低,同时不易反弹,成为维持治疗场景下的重要优势。

Armstrong技术全梳理系列
和铂医药技术全梳理; 荣昌生物技术全梳理; 再鼎医药技术全梳理; 药明生物技术全梳理; 恒瑞医药技术全梳理; 豪森药业技术全梳理; 正大天晴技术全梳理; 吉凯基因技术全梳理; 基石药业技术全梳理; 百济神州技术全梳理; 百济神州技术全梳理第2版; 信达生物技术全梳理; 信达生物技术全梳理第2版; 中山康方技术全梳理; 复宏汉霖技术全梳理; 先声药业技术全梳理; 君实生物技术全梳理; 嘉和生物技术全梳理; 志道生物技术全梳理; 道尔生物技术全梳理; 尚健生物技术全梳理; 康宁杰瑞技术全梳理; 科望医药技术全梳理; 岸迈生物技术全梳理; 礼进生物技术全梳理; 康桥资本技术全梳理; 余国良的抗体药布局; 荃信生物技术全梳理; 安源医药技术全梳理; 三生国健技术全梳理; 仁会生物技术全梳理; 乐普生物技术全梳理; 同润生物技术全梳理; 宜明昂科技术全梳理; 派格生物技术全梳理; 迈威生物技术全梳理; Momenta技术全梳理; NGM技术全梳理; 普米斯生物技术全梳理; 普米斯生物技术全梳理2.0; 三叶草生物技术全梳理; 泽璟制药抗体药全梳理; 恒瑞医药抗体药全梳理; 齐鲁制药抗体药全梳理; 石药集团抗体药全梳理; 豪森药业抗体药全梳理; 华海药业抗体药全梳理; 科伦药业抗体药全梳理; 百奥泰技术全梳理; 凡恩世技术全梳理。