新锐Biotech艾科联AACR亮相:CD3/41BB/CDH17数据优异,开启下一代TCE
2026年4月22日
CD3双抗在众多交易的簇拥下,成为大火赛道。但单纯的CD3双抗,还是被认为可能存在杀伤能力不足,T细胞激活持久性相对较差。所以,二代CD3始终在不断被开发,开发的主要方向,加上共刺激信号,如CD28,41BB,CD2等。从CAR-T的设计来看,这一思路有其合理性。第一代 CAR 在 T 细胞内仅包含一个CD3ζ结构域,负责细胞内的信号传导,但由于缺少共刺激域,该类CAR-T 细胞具有寿命短、细胞毒性低等缺陷。第二代CAR-T具有 1 个独特的 4-1BB 或 CD28 分子共刺激结构域,增强了来自TCR-CD3 复合物的“信号”, T 细胞增殖能力和杀伤毒性提升。目前上市的CAR-T主要为二代CAR-T。CD3/41BB/TAA,其实就是一个将CAR-T内置信号外置的过程,而这一过程最重要的就是找到其最大的TAA依赖激活的安全窗口。如今对于CD3双抗和41BB双抗的设计均为依赖TAA的T细胞激活,以实现对肿瘤细胞的精准杀伤。其实,罗氏已经做了很好的临床探索,目前数据优异。
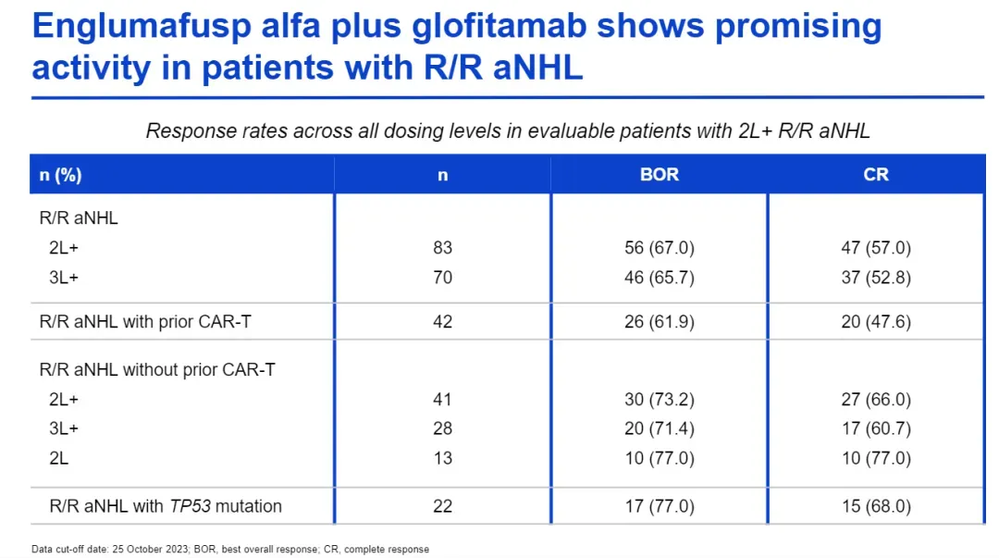
罗氏正在开展1期临床试验中评估englumafusp alfa(CD19/41BB)与CD20×CD3双特异性抗体格菲妥单抗(glofitamab)联用,治疗复发/难治性非霍奇金淋巴瘤(r/r NHL)患者。
初步研究数据表明,该联合疗法在侵袭性r/r NHL(r/r aNHL)患者中显示出良好的抗肿瘤活性,最佳客观缓解率(BoR)为67.0%,完全缓解(CR)率为57.0%;二线治疗r/r侵袭性NHL患者的BOR为77.0%,CR率为77.0%。此外,联合治疗具有与格菲妥单抗单药相当的安全性和细胞因子释放综合征(CRS)情况。
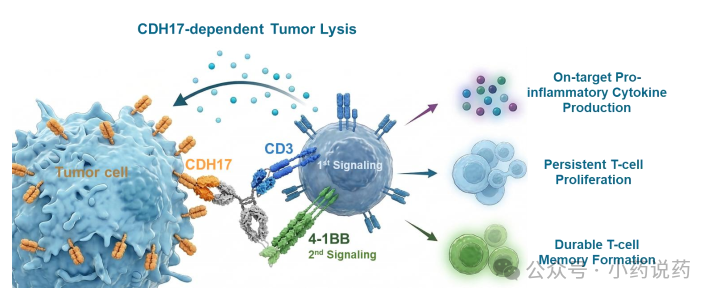
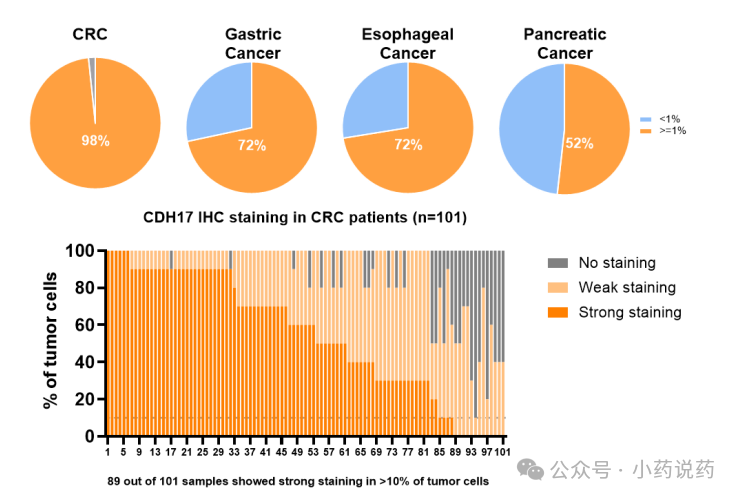
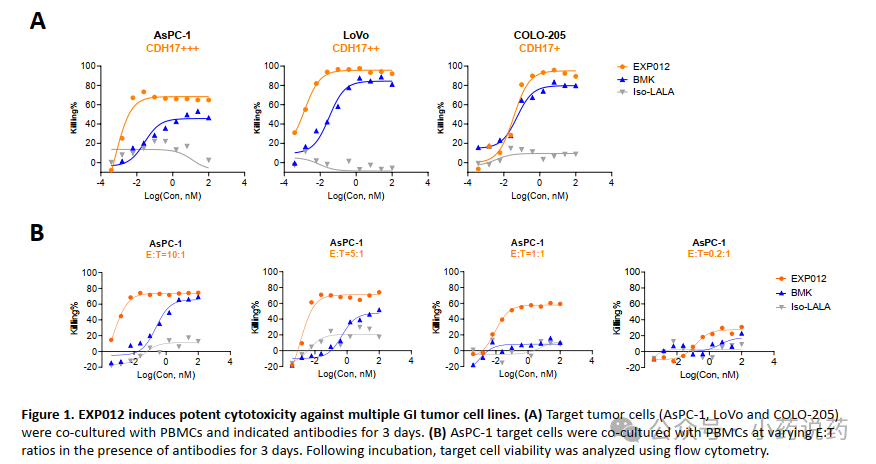
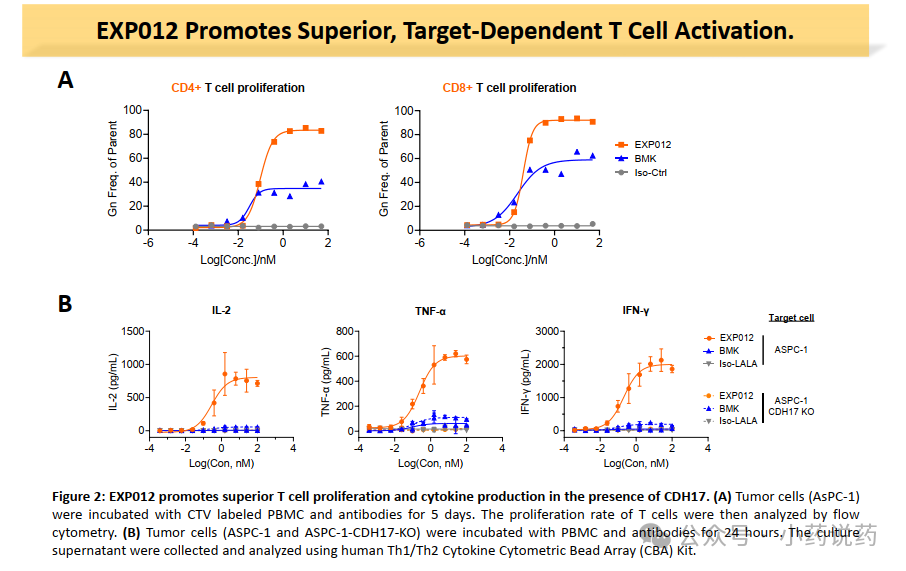
以上数据也给予该类药物一定的数据支撑和科学支撑。CLDN18.2/4-1BB的双特异性抗体Givastomig联合纳武利尤单抗及mFOLFOX6化疗方案,在HER2阴性转移性胃癌一线治疗中的应用潜力。初步结果显示,Givastomig联合治疗方案显示出令人鼓舞的初步抗肿瘤活性和可管理的安全性,中位PFS达16.9个月。而历史中位PFS仅8.3个月。Givastomig可同时结合肿瘤细胞表面的CLDN18.2与T细胞上的共刺激受体4-1BB,可在CLDN18.2表达的肿瘤微环境中通过4-1BB信号通路条件性激活T细胞。也是对41BB有效佐证。艾科联作为头部CD3/41BB下一代TCE公司,在该领域团队探索多年,平台具有优异的安全窗口,目前公司头部管线CD3/41BB/DLL3已经在临床阶段,临床进展顺利。2026年,艾科联在AACR公开旗下CD3/41BB/CDH17管线EXP012临床前数据。结构层面,41BB放置于C端,CD3和CDH17均为1价。CDH17作为大热靶点,在ADC领域已经产生多个重磅交易,而在CD3领域开发者为数不多。CDH17在结直肠癌,胃癌,胰腺癌等高度表达。EXP012对于肿瘤细胞相比于对照药物,具有更好的杀伤能力。
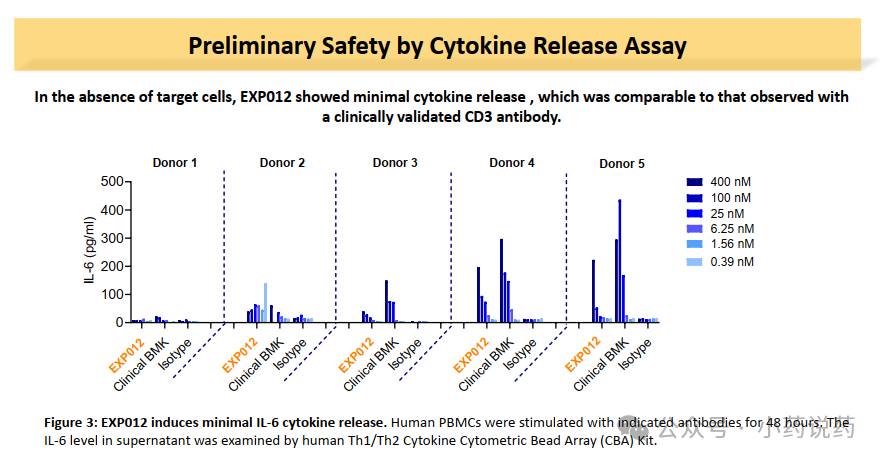
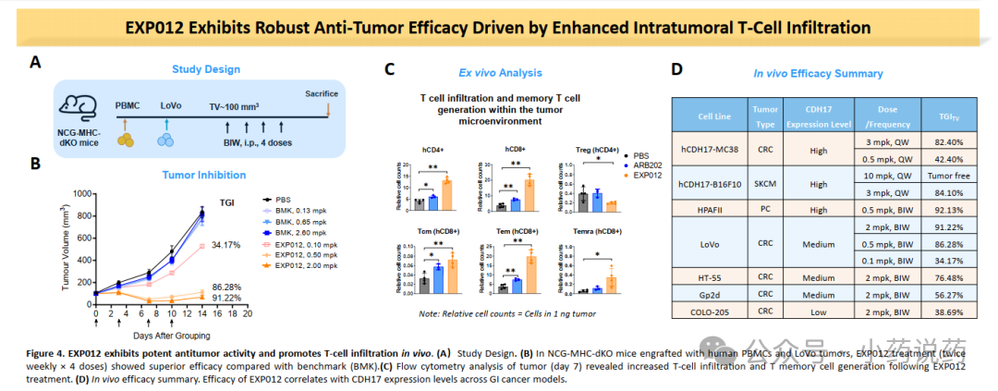
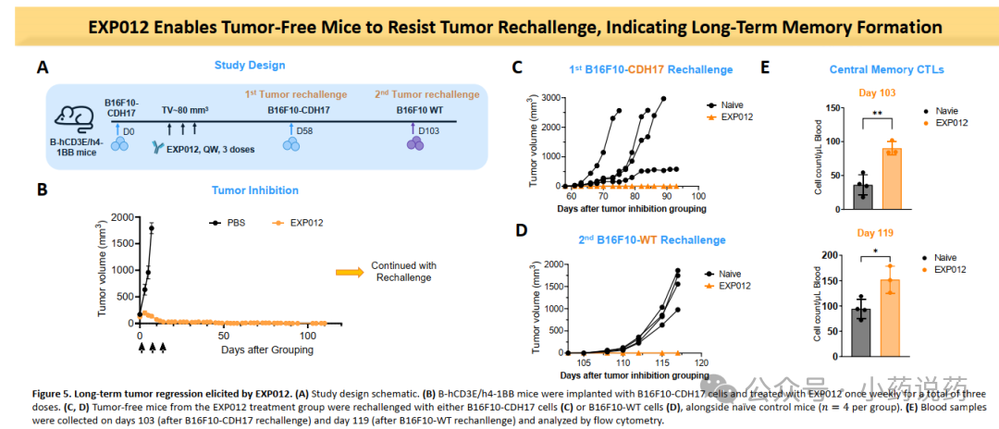
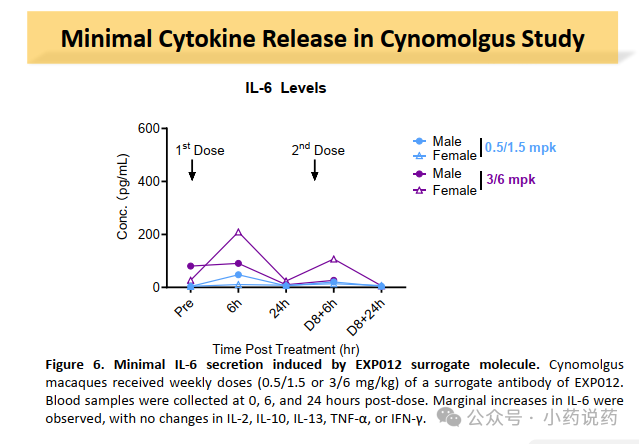
EXP012 展现了独特的肿瘤依赖性细胞因子释放与增殖机制。通过在肿瘤微环境中诱导 T 细胞的定向分化并建立免疫记忆,该分子能有效启动免疫级联反应,从而驱动强劲且持久的抗肿瘤免疫应答。在没有靶细胞的情况下,EXP012具有极少的细胞因子释放,与当前的临床验证的CD3双抗具有可比性,甚至更优。也就是说,41BB的加入并没有造成更严重的CRS的风险,这跟罗氏的研究具有一致性。EXP012表现出强效的抗肿瘤活性,主要由肿瘤内T细胞浸润增强所驱动。EXP012能够使已清除肿瘤的小鼠在再次肿瘤挑战时仍能抵抗肿瘤,表明其可诱导长期免疫记忆的形成。即便再次接种的肿瘤不表达CDH17也展现了优异的杀伤能力,Bystander Killing效应明显,对于实体瘤异质性的解决具有重大意义。最主要的是猴子方面数据,目前EXP012在猴子上能够给到6mpk,同时具有极少的CRS释放。证明了该平台的可靠性。未来临床剂量,肯定不需要这么高的剂量。具有良好的安全窗口的潜力。艾科联作为头部下一代TCE临床阶段公司,在不久的将来会陆续有多款TCE药物进入临床。而目前的数据展现了极为有利的前景。当下CD3多抗,已经在尝试同ADC的联用,所以未来CDH17 ADC也并不会成为CDH17 TCE的竞争对手,两者反而可以利用机制的互补进行联用或者序惯治疗。公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。