2025年6月19日,德睿智药宣布小分子GLP-1受体激动剂MDR-001的2b期临床取得成功,不同剂量组治疗24周减重8.2%-10.3%,绝对减重7.4-9.2kg,安慰剂组为2.4kg(p<0.00001)。同时,MDR-001在改善多个代谢和心血管疾病相关参数表现出色,包括腰围、血脂、血压等指标,有望带来全面临床获益。
安全性方面,MDR-001试验期间无药物治疗相关SAE,研究入组20%肝功能异常和转氨酶升高的受试者,各组均未观察到转氨酶升高的趋势,且相比于安慰剂组,MDR-001治疗组的转氨酶较基线具有明显降低。此外,心脏安全性良好,未观察到心率升高的风险,仅有2例(0.8%)因TEAE终止治疗,远低于同类药物15-50%的终止率。

辉瑞、礼来为小分子GLP-1受体激动剂开发的先驱,引领了整个赛道的发展。
2023年6月,辉瑞放弃开发小分子GLP-1受体激动剂Lotiglipron,原因是其在早期临床中出现的转氨酶升高的安全性信号,而这一问题当时在第一代的Danuglipron中则没有发现。

2025年4月,辉瑞宣布终止开发每日一次小分子GLP-1受体激动剂Danuglipron,因1例患者经历严重肝损伤,停药后缓解,经过考虑后辉瑞决定终止开发Danuglipron。

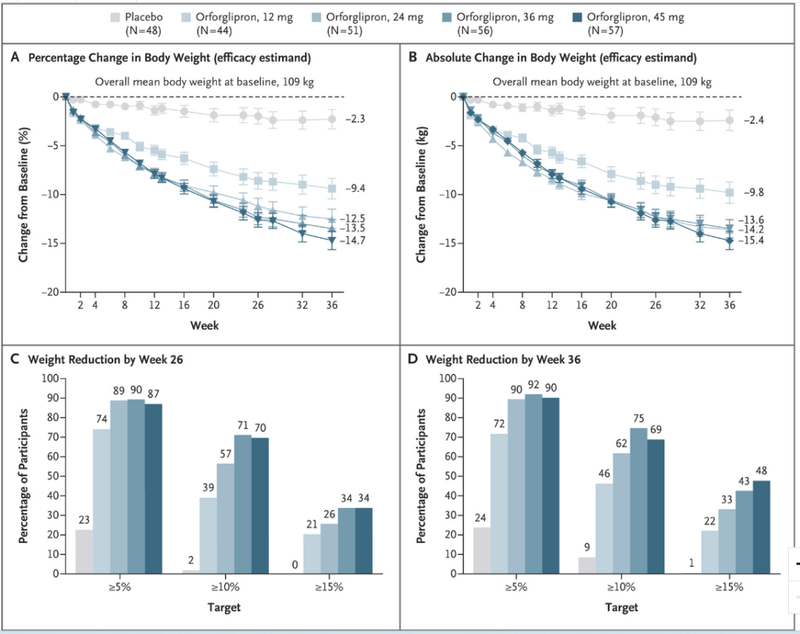
礼来的Orforglipron则在今年宣布糖尿病三期临床成功。

礼来Orforglipron在安全性方面与注射类GLP-1药物相当,无患者达到Hy's law标准的肝损伤。

Orforglipron治疗期间,ALT、AST均值有所下降。



Orforglipron在减重二期临床中,治疗36周减重幅度为12.5%-14.7%(安慰剂2.3%)。
国内主要竞品中,恒瑞医药HRS-7535在今年ADA会议上公布了及那种二期临床数据,治疗26周减重2.99-9.36%,安慰剂组为-2.5%。安全性方面,未观察到肝酶升高趋势。


华东医药HDM1002的1b期临床数据在今年ADA会议上公布,治疗4周减重6.8%、5.1%、4.9%,未观察到肝酶升高相关AE。

闻泰/箕星药业VCT220的减重二期临床数据在今年ADA会议上公布,治疗16周减重5.8-9.5%,安慰剂组为1.6%。安全性方面,未发现肝脏毒性相关安全性信号。


总结
小分子GLP-1的先驱,辉瑞因肝脏毒性而终止开发,礼来则率先在三期临床撞线,且ALT、AST均有降低趋势。国产竞品中,恒瑞医药、闻泰医药、华东医药已经推进到三期临床,德睿智药此次2b期临床表现出优异的疗效与安全性,很快也将推进到三期临床。对于关键的肝脏安全性,几家企业均未披露具体数据,恒瑞医药的描述是“未观察到肝酶升高趋势”,闻泰医药的描述是“未发现肝脏毒性相关安全性信号”,华东医药的描述为“未报告肝酶升高相关AE”(较早期数据,1b期治疗4周数据)。德睿智药则描述“转氨酶较基线明显降低”。MDR-001有望成为小分子GLP-1赛道又一个有力竞争者。

Armstrong技术全梳理系列
和铂医药技术全梳理; 荣昌生物技术全梳理; 再鼎医药技术全梳理; 药明生物技术全梳理; 恒瑞医药技术全梳理; 豪森药业技术全梳理; 正大天晴技术全梳理; 吉凯基因技术全梳理; 基石药业技术全梳理; 百济神州技术全梳理; 百济神州技术全梳理第2版; 信达生物技术全梳理; 信达生物技术全梳理第2版; 中山康方技术全梳理; 复宏汉霖技术全梳理; 先声药业技术全梳理; 君实生物技术全梳理; 嘉和生物技术全梳理; 志道生物技术全梳理; 道尔生物技术全梳理; 尚健生物技术全梳理; 康宁杰瑞技术全梳理; 科望医药技术全梳理; 岸迈生物技术全梳理; 礼进生物技术全梳理; 康桥资本技术全梳理; 余国良的抗体药布局; 荃信生物技术全梳理; 安源医药技术全梳理; 三生国健技术全梳理; 仁会生物技术全梳理; 乐普生物技术全梳理; 同润生物技术全梳理; 宜明昂科技术全梳理; 派格生物技术全梳理; 迈威生物技术全梳理; Momenta技术全梳理; NGM技术全梳理; 普米斯生物技术全梳理; 普米斯生物技术全梳理2.0; 三叶草生物技术全梳理; 泽璟制药抗体药全梳理; 恒瑞医药抗体药全梳理; 齐鲁制药抗体药全梳理; 石药集团抗体药全梳理; 豪森药业抗体药全梳理; 华海药业抗体药全梳理; 科伦药业抗体药全梳理; 百奥泰技术全梳理; 凡恩世技术全梳理。