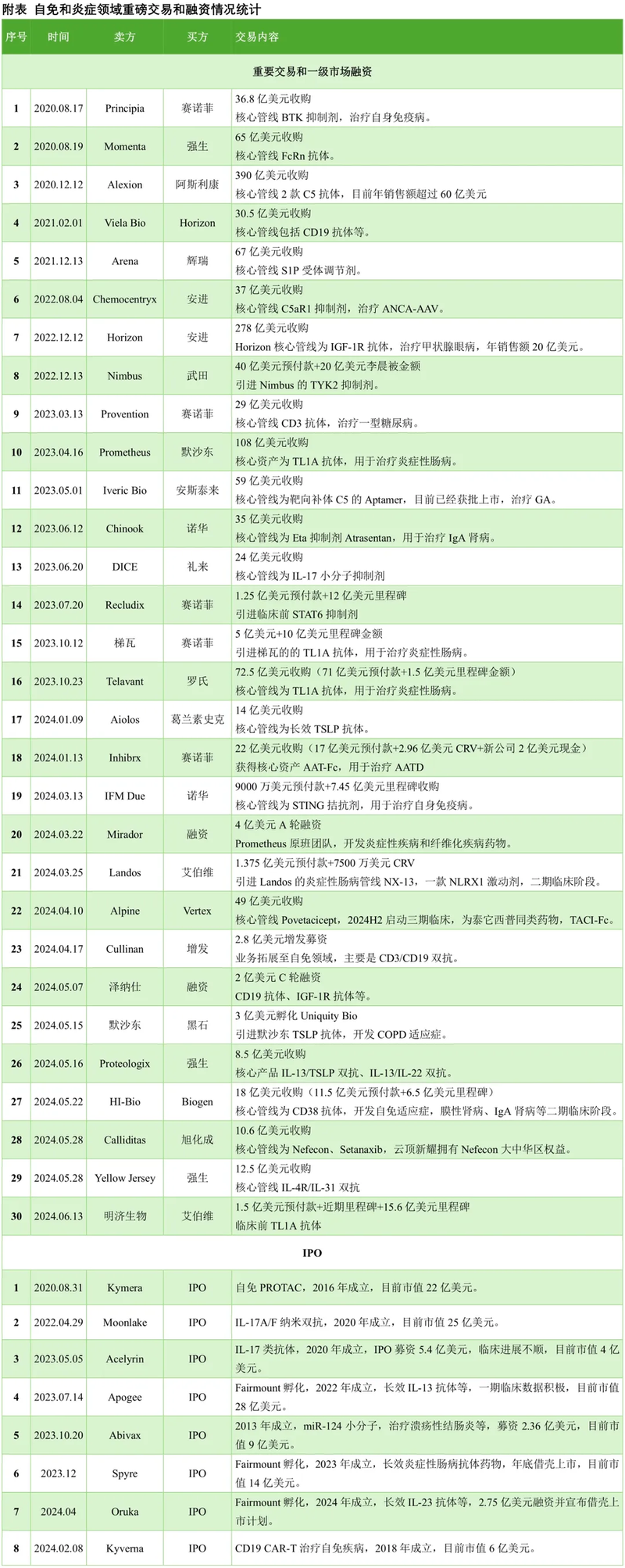
2024年6月22日,武田在ISTH年会上公开了CD38抗体Mezagitamab(TAK-079)治疗原发免疫性血小板减少症(ITP)的2b期临床数据。武田同时宣布计划下半年启动三期临床试验。

疗效方面,600mg Mezagitamab治疗组81.8%的患者达到血小板完全响应,90.9%的患者达到有临床意义的血小板响应,100%的患者达到止血血小板响应。
该2b期临床分为两个部分,Part A中25例患者分为3组,分别接受100mg、300mg、安慰剂治疗。Part B中16例患者分为2组,分别接受600mg Mezagitamab或安慰剂治疗,每周给药一次,连续给药8周,继续随访8周。

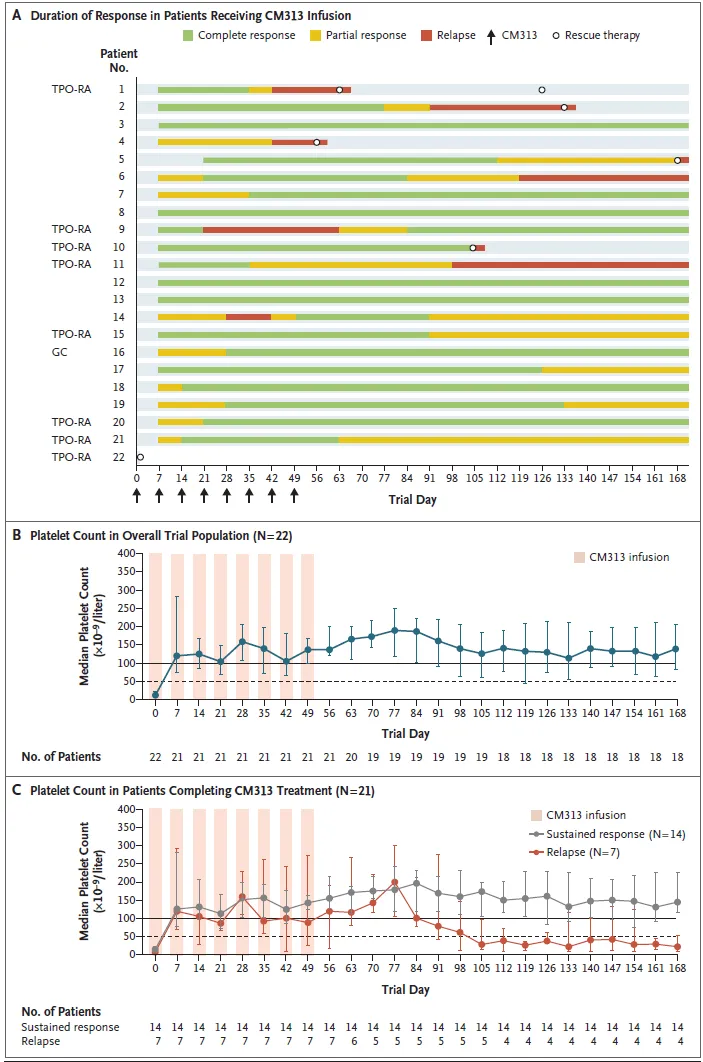
2024年6月19日,新英格兰医学期刊发表了康诺亚CD38抗体CM313治疗原发免疫性血小板减少症(ITP)的1/2期临床数据。该研究入组22例ITP患者,除1例患者首次给药后脱落,其余21例患者均完成了8 次给药和16周的随访。在疗效上,95.5%的患者(21/22)在首次接受CM313给药后 8周内达到血小板计数≥50 × 10^9/L,血小板计数持续≥50 × 10^9 /L的中位累积时间为23周,至首次血小板计数≥50 × 10^9 /L的中位时间为1周,至首次血小板计数≥30 × 10^9 /L且较基线增加≥2倍的中位时间为1周,持久血小板响应率为63.6%(14/22)。21例患者在整个研究期间达到总体缓解(完全或部分缓解),其中20例患者达到完全缓解。基线时,68.2%患者(15/22)报告出现出血症状。在第8周,出现出血症状的患者比例降至4.8%(1/21)。大多数因CM313治疗后血小板计数恢复正常或安全水平而停用伴随药物。总之,CM313在95.5%的既往接受过多种治疗的ITP患者中表现出快速且持续的疗效反应。

总结
近两年来,欧美资本市场上自免交易异常火热,许多B细胞的肿瘤靶点也纷纷转向自免赛道,并不断取得临床进展。今年5月,HI-Bio被Biogen以18亿美元收购,其核心管线就是CD38抗体,用于自免疾病。如今康诺亚、武田的CD38抗体ITP临床数据相继取得初步突破,ITP或将成为CD38成功拓展的首个自免适应症。