▎Armstrong
近期,DLL4/VEGF双抗ES104(Tovecimig)在胆道癌的关键性临床试验中取得成功,达到主要终点,有望成为胆道癌二线治疗的新标准,为这一高度未满足的临床领域带来新的希望。
胆道癌是一种高度恶性的消化系统肿瘤,具有进展快、诊断晚、预后差等特点。全球胆道癌发病率约为3/10万,根据最新的GLOBOCAN数据,全球胆道系统相关癌症的新发病例总数大约为 27–29 万例/年,且呈逐年上升趋势。在中国,胆道癌发病率明显高于欧美地区,每年新增胆道癌患者约为55,700人【1】。大多数胆道癌患者确诊时已处于晚期,当前标准治疗手段对其控制效果有限。一线治疗以免疫联合化疗为主,客观缓解率不足30%,虽然免疫检查点抑制剂能够改善生存,但整体获益仍有限;70-80%的患者在一线治疗失败后会进入二线治疗阶段。二线治疗中,仅有FOLFOX化疗方案作为标准,其客观缓解率仅5%,中位生存期约为半年;真正具有明确靶点突变可使用靶向治疗的患者仅占比不超过20%。因此,二线晚期胆道癌二线治疗尤其缺乏有效手段,亟需机制新颖、疗效确切的新型药物。
在ES104的胆道癌关键性临床试验中,Compass采取随机、对照设计,入组168例晚期胆道癌患者,主要终点为ORR,关键次要终点包括PFS、OS、DOR等。
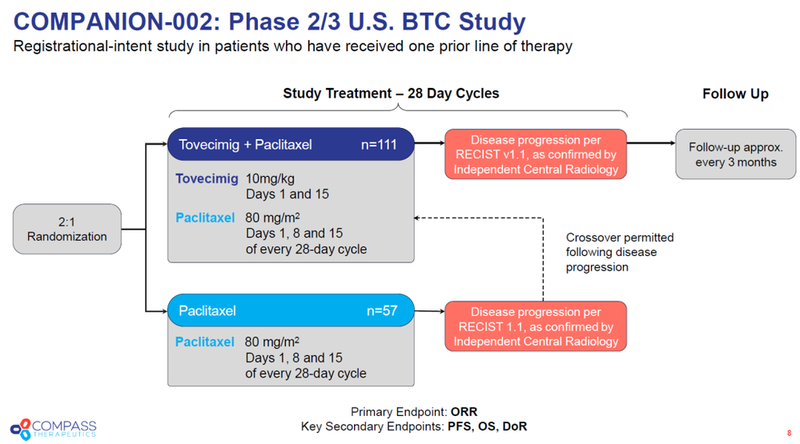
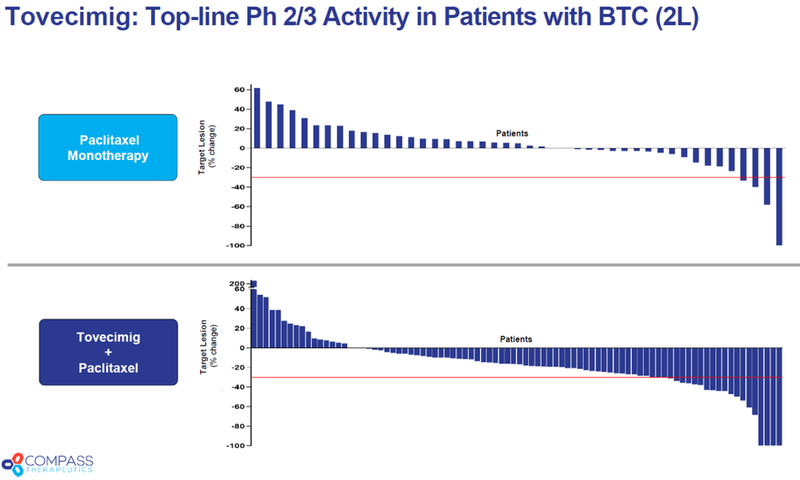
ES104联合紫杉醇治疗组相比于紫杉醇对照组,ORR分别为17.1%、5.3%,p值为0.031,ORR提高到3倍以上,展示出优异疗效。两组BOR为PD的比例差异显著,紫杉醇组42.1%的患者其最佳疗效为疾病进展,而ES104联合治疗组仅16.2%的患者为疾病进展,提示PFS曲线在治疗早期即已出现分离,预示着PFS将获得显著获益。此外,ES104更早的2期单臂研究中,BTC二线或三线的患者经ES104联合紫杉醇治疗后中位PFS和中位OS分别达到9.4个月和12.5个月,远超化疗PFS 3-4个月,OS半年的历史数据。

从瀑布图上可以看到,联合治疗组有4名患者达到100%缩瘤,靶病灶完全消退,获益明显。在疗效显著提高的情况下,ES104安全性表现也与已获批的同类药物类似。ES104有望成为全球胆道癌二线治疗的标准疗法。
Stifel在其近期的研究报告中指出,Tovecimig当前在客观缓解率方面已取得统计学显著性,这一结果使得后续对无进展生存期数据的正式统计分析成为可能。在当前缺乏有效治疗选择的疾病背景下,结合Tovecimig在疾病进展数据中表现出的差异性优势等方面的评估,Stifel将Tovecimig在二线胆道癌适应症中的成功概率(POS)由原先的75%上调至85%。
适应症拓展方面,ES104在结直肠癌单药临床试验中也显示出积极的临床获益。
ES104在胆道癌、结直肠癌的临床进展,其意义远超本身,意味着DLL4/VEGF有望成为新一代的血管抑制基石药物,对于胃癌、胶质母细胞瘤、肝癌、卵巢癌、肾癌等多个瘤种都有拓展可能。
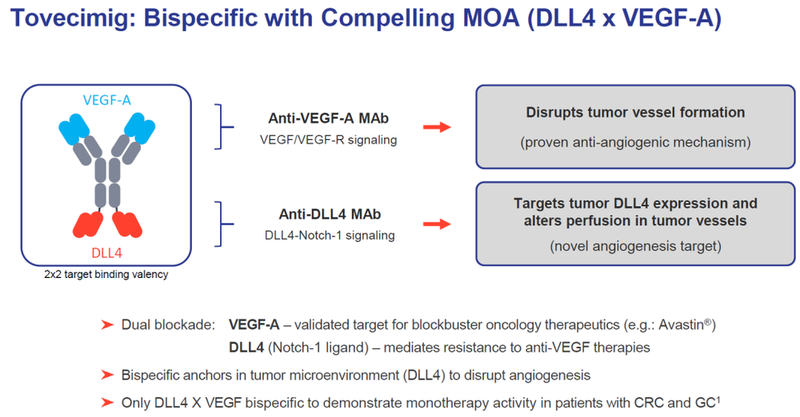
在血管抑制方面,最经典的治疗方案包括贝伐珠单抗、小分子VEGF受体抑制剂等,虽已广泛应用于多种肿瘤治疗中,但其疗效常因耐药性而受限。更重要的是,血管抑制这一机制也开始取得迭代突破。ES104采用对称的2+2设计,靶向DLL4和VEGF两个关键血管生成通路,其中,DLL4-Notch1 通路被认为是VEGF单抗产生耐药的关键机制。通过同步阻断这两大路径,ES104有望克服传统血管抑制疗法的局限性,成为血管生成抑制领域的新一代“基石”药物。
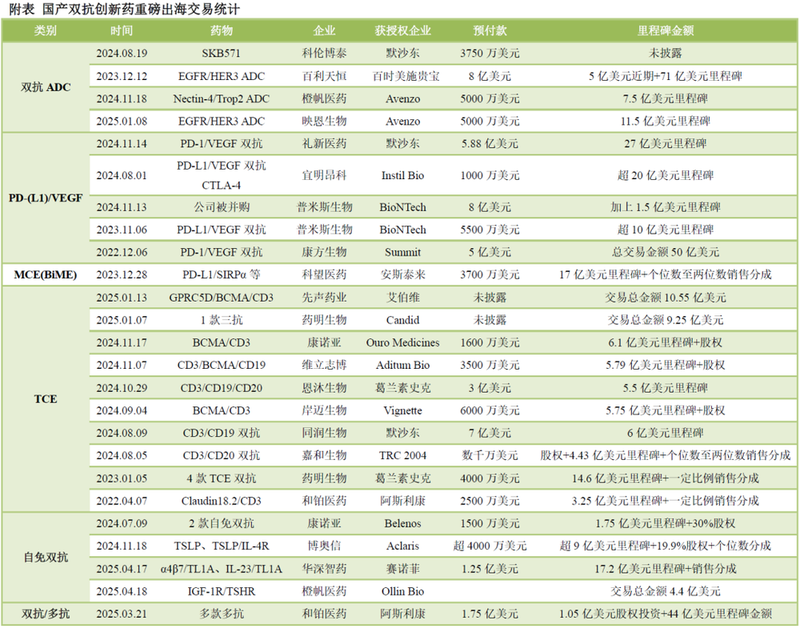
DLL4/VEGF双抗的成功,也提示我们新的抗体药物形式近年来快速发展,PD-1/VEGF为代表的肿瘤免疫双抗,EGFR/cMET为代表的TAA双抗,DLL3/CD3为代表的实体瘤TCE,DXd-ADC为代表的三代ADC取得一系列临床突破。以双抗为例,多款TCE、PD-1/VEGF双抗、自免双抗密集完成高额出海授权交易,新的赛道如MCE(Myeloid Cell Engager),也出现科望医药PD-L1/SIRPα双抗更创新的双抗新药。
双抗本质上是不同靶点作用机制的有机组合,肿瘤免疫、TAA靶向、血管抑制等为肿瘤治疗中最重要的几类机制。PD-1/VEGF双抗的成功正是源于肿瘤免疫与血管抑制机制的有效结合,也引起了整个行业的广泛关注和布局。
在双抗领域的布局,科望医药走在了更前沿,其拥有DLL4/VEGF双抗ES104的大中华区权益,正积极推进胆道癌在大中华区的商业化进程,同时布局多个瘤种的临床探索。此外,其自主研发的MCE包括多款基于BiME平台的双抗、两款TL1A/X双抗等,将持续加热双抗赛道。
总结
默沙东和BMS的PD-1+小分子VEGF抑制剂 ,康方生物PD-1/VEGF双抗一再验证了免疫治疗+血管抑制的应用前景,免疫治疗、血管抑制、化疗、放疗成为肿瘤治疗的最重要基石。免疫治疗的迭代主要是新靶点组合,化疗的迭代主要是ADC,放疗的迭代主要是靶向核药。相比之下,血管抑制的迭代仍有很大空间,DLL4/VEGF双抗有望成为血管抑制的新一代基石药物,后续可以与化疗、ADC、免疫治疗多种治疗机制开展联合治疗的探索,不断扩展其临床应用空间。
参考文献
[1] Zheng R, Zhang S, Zeng H, et al. Cancer incidence and mortality in China, 2016. J Natl Cancer Cent 2022;2:1-9.

Armstrong技术全梳理系列
和铂医药技术全梳理; 荣昌生物技术全梳理; 再鼎医药技术全梳理; 药明生物技术全梳理; 恒瑞医药技术全梳理; 豪森药业技术全梳理; 正大天晴技术全梳理; 吉凯基因技术全梳理; 基石药业技术全梳理; 百济神州技术全梳理; 百济神州技术全梳理第2版; 信达生物技术全梳理; 信达生物技术全梳理第2版; 中山康方技术全梳理; 复宏汉霖技术全梳理; 先声药业技术全梳理; 君实生物技术全梳理; 嘉和生物技术全梳理; 志道生物技术全梳理; 道尔生物技术全梳理; 尚健生物技术全梳理; 康宁杰瑞技术全梳理; 科望医药技术全梳理; 科望医药技术全梳理2.0; 岸迈生物技术全梳理; 礼进生物技术全梳理; 康桥资本技术全梳理; 余国良的抗体药布局; 荃信生物技术全梳理; 安源医药技术全梳理; 三生国健技术全梳理; 仁会生物技术全梳理; 乐普生物技术全梳理; 同润生物技术全梳理; 宜明昂科技术全梳理; 派格生物技术全梳理; 迈威生物技术全梳理; Momenta技术全梳理; NGM技术全梳理; 普米斯生物技术全梳理; 普米斯生物技术全梳理2.0; 三叶草生物技术全梳理; 泽璟制药抗体药全梳理; 恒瑞医药抗体药全梳理; 齐鲁制药抗体药全梳理; 石药集团抗体药全梳理; 豪森药业抗体药全梳理; 华海药业抗体药全梳理; 科伦药业抗体药全梳理; 百奥泰技术全梳理; 凡恩世技术全梳理。