解析全球首个获批的BCMA × CD3 双抗--Teclistamab
2025年8月9日
Teclistamab(商品名:TECVAYLI®),是首个用于治疗复发或难治性多发性骨髓瘤(RRMM)成年患者的现成皮下注射双特异性BCMA×CD3 T细胞接合剂,患者此前至少接受过4种治疗方案,包括一种蛋白酶体抑制剂(PI)、一种免疫调节剂和一种抗CD38单克隆抗体。
![图片]()
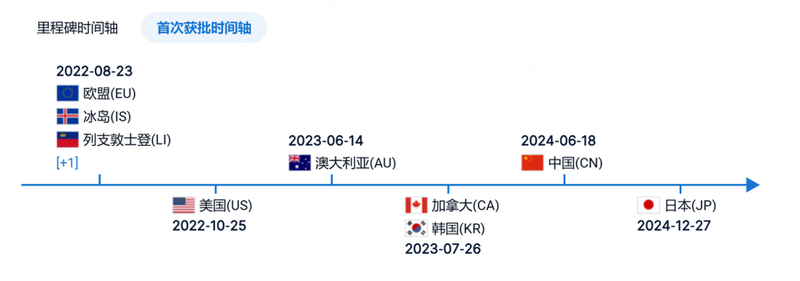
该药已于2022年获美国FDA批准上市,首次获批的时间线见下图。图片来源于智慧芽
多发性骨髓瘤是一种源于浆细胞(一种负责抗体生成的免疫细胞)的恶性肿瘤。在该疾病中,骨髓内异常增殖的浆细胞会大量分泌单克隆免疫球蛋白(通常称为M蛋白)。这些异常蛋白不仅会抑制正常血细胞的生成,还可能引发:(1)异常浆细胞在骨髓内过度增殖,会破坏骨组织,导致骨痛、骨折以及高钙血症;(2)过量的M蛋白可能在肾脏沉积,引发肾功能障碍甚至肾衰竭;(3)血液学异常:例如贫血和免疫功能低下,这会增加感染的风险。尽管目前多发性骨髓瘤仍无法完全治愈,但借助化疗、蛋白酶体抑制剂、免疫调节剂、单克隆抗体等多种治疗手段,能够有效控制病情,显著延长患者的生存期并提升生活质量。然而,随着治疗的推进,患者可能会对多种治疗方案产生耐药性,这使得病情的持续控制变得更加复杂且充满挑战。
Teclistamab(特立妥单抗)
![图片]()
药物类型:双特异性T细胞结合器
靶点:BCMA(B细胞成熟抗原)和CD3(T细胞表面抗原)
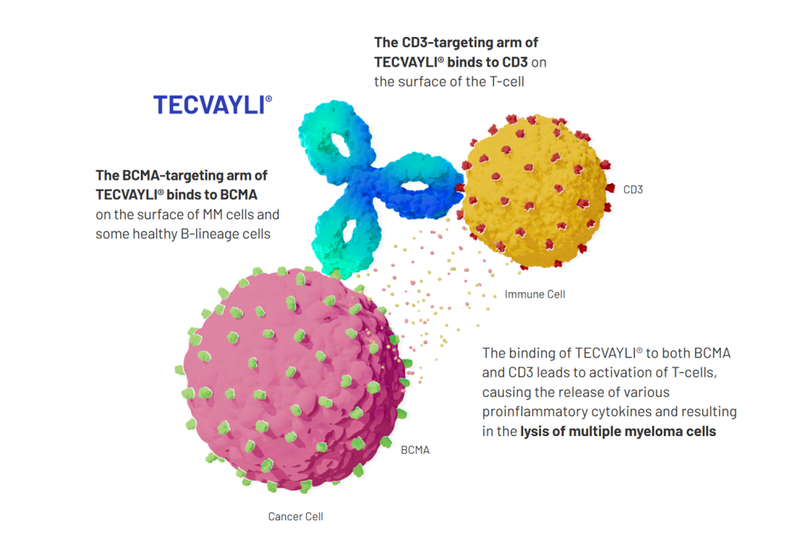
[知识扩展:BCMA(B-cell maturation antigen)即B细胞成熟抗原,是一种细胞表面受体,主要在浆细胞和多发性骨髓瘤细胞上表达。它属于肿瘤坏死因子受体(TNFR)超家族,参与调控B细胞的分化以及浆细胞的存活和功能维持。在多发性骨髓瘤患者中,BCMA在恶性浆细胞上高度表达,因此成为了一个极具前景的治疗靶点。针对BCMA的疗法(如CAR-T细胞治疗、双特异性抗体和抗体药物偶联物)已显示出显著的抗肿瘤活性,为患者提供了新的治疗选择。CD3是一组在T细胞表面表达的蛋白复合体,是T细胞受体(TCR)复合物的重要组成部分,其主要功能包括:(1)当T细胞受体识别抗原呈递分子(MHC)上呈现的抗原时,CD3分子介导信号传递,激活T细胞,从而引发一系列免疫反应;(2)CD3在T细胞的发育和成熟过程中起着关键作用,确保T细胞能够正确识别抗原并响应免疫刺激。通过靶向CD3,药物可以有效招募和激活T细胞,实现对病变细胞的精准靶向杀伤,从而为癌症等疾病的治疗提供了新的手段,例如各类T细胞接合剂(TCE)。]作用机制:通过同时结合BCMA(在多发性骨髓瘤细胞表面高表达)和CD3(T细胞表面标志物),激活T细胞杀伤肿瘤细胞(见下图)。
原研机构:Janssen Research & Development LLC
Teclistamab的分子结构
Teclistamab采用了全长IgG4抗体的结构形式,其生产和开发是基于杨森生物科技公司与Genmab签订的DuoBody®技术平台许可协议。这一协议确保了两个不同靶点结合域能够正确组装并保持稳定,既满足了双特异性抗体的需求,又具备了良好的体内半衰期和药代动力学特性。
[知识拓展:IgG4是免疫球蛋白G(IgG)的四个亚型之一,其结构与其他IgG亚型类似,由两条重链和两条轻链组成。但其铰链区(hinge region)较为灵活,且存在独特的“半抗体交换”现象,即两种不同来源的IgG4分子可能交换半边,从而形成混合型抗体。与IgG1相比,IgG4的Fc区与Fcγ受体(FcγRs)和补体蛋白C1q的结合能力较弱,因此在体内引起的抗体依赖细胞毒性作用(ADCC)和补体依赖细胞毒性作用(CDC)明显降低。这一特性使其在需要减少炎症反应或免疫副作用的治疗中更具优势。由于其较低的效应功能,IgG4格式的抗体常被用于构建双特异性抗体和T细胞接合体。这可以确保在靶向激活T细胞的同时,不会引发过强的Fc介导的免疫效应,从而提高治疗的安全性和有效性。关于Duomab技术平台的详细介绍可以查阅之前发表的文章内容:技术梳理系列 | Genmab的Duomab平台]
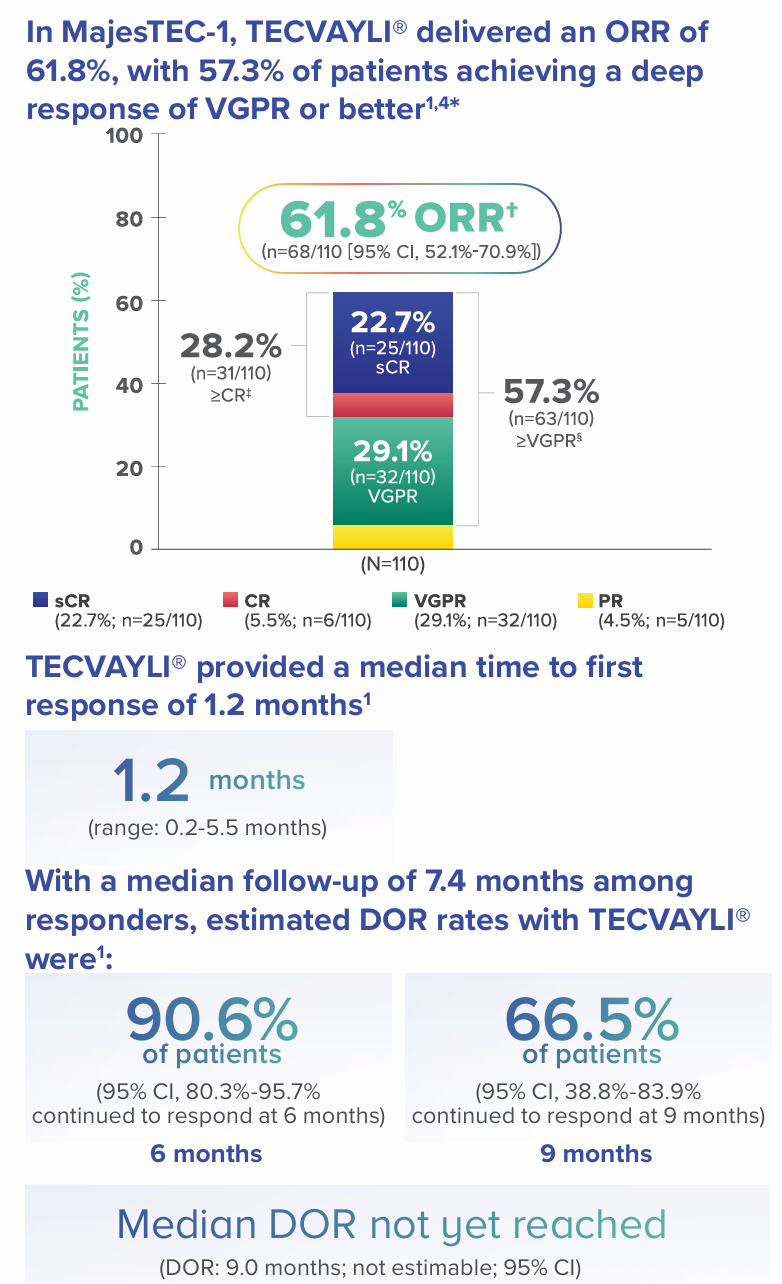
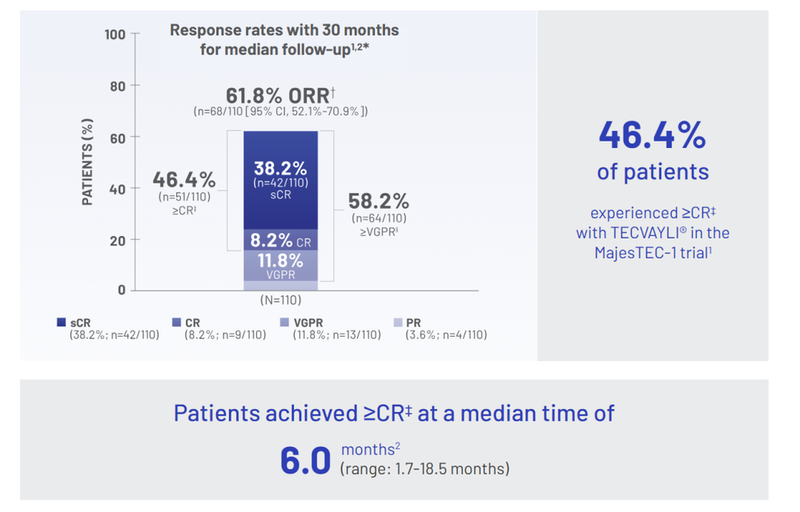
MajesTEC-1研究是一项关键的1/2期临床试验,旨在评估Teclistamab在复发或难治性多发性骨髓瘤(RRMM)患者中的疗效和安全性。该研究是一项单臂、开放标签、多中心、剂量递增研究。主要终点为总缓解率(ORR),即患者在治疗后肿瘤缩小或消失的比例;次要终点包括缓解持续时间(DOR)、无进展生存期(PFS)、总生存期(OS)等。在该研究中,Teclistamab的总缓解率(ORR):61.8%,其中 57.3% 的患者实现了极佳部分缓解(VGPR)或更深程度的反应。TECVAYLI® 在复发/难治性多发性骨髓瘤(RRMM)患者中展现了较高的疗效。其他关键数据如下:- 首次缓解的中位时间:1.2个月(范围:0.2-5.5个月)
这表明Teclistamab在 患者中具有快速起效、高深度缓解率,并且缓解持续时间较长的特点。
Teclistamab在 30 个月的中位随访期后,仍显示出较高的缓解率,具体数据如下:这表明,在更长时间的随访中,Teclistamab依然能维持较高的缓解率,并且深度缓解(sCR 和 CR)的患者比例较先前数据有所提升,显示出该疗法在复发/难治性多发性骨髓瘤(RRMM)患者中的持续疗效。
Teclistamab的安全性
![图片]()
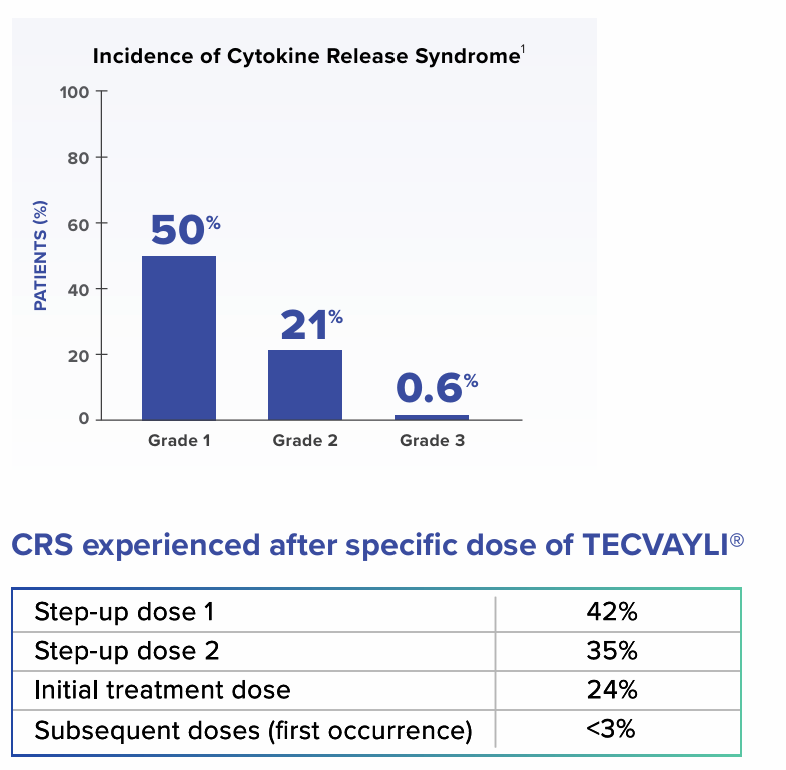
使用Teclistamab可能会引发严重的不良反应,其中最为关键的是细胞因子释放综合征(CRS)和神经毒性。CRS是一种可能危及生命甚至导致死亡的严重反应,因此在治疗过程中,建议采用逐步加量(Step-up dosing)方案来降低CRS的发生风险。如果患者出现CRS症状,应立即暂停Teclistamab的使用,直至症状缓解,并根据CRS的严重程度来决定是否需要永久停药。
关于细胞因子释放综合征(CRS):在临床试验中,接受推荐剂量Teclistamab的患者中,有72%出现了CRS,其中1级CRS占50%,2级占21%,3级占0.6%。此外,33%的患者经历了复发性CRS。大多数患者在首次逐步加量(Step-up dose 1,42%)、第二次逐步加量(Step-up dose 2,35%)或初始治疗剂量(24%)后出现CRS,而在后续剂量中首次发生CRS的概率低于3%。CRS的中位起病时间为2天(范围:1至6天),中位持续时间为2天(范围:1至9天)。CRS的临床症状包括但不限于发热、低氧血症、寒战、低血压、窦性心动过速、头痛以及肝酶(AST和ALT)升高。此外,Teclistamab还可能引发免疫效应细胞相关神经毒性综合征(ICANS)以及其他严重的神经毒性反应。在治疗期间,医护人员需要密切监测患者是否出现神经毒性的相关症状,如头痛、意识混乱、言语障碍等。一旦发现这些症状,应立即暂停Teclistamab的治疗,并根据患者的病情严重程度调整用药方案,以确保患者的安全和治疗的有效性。
核心专利
标题:Bcma/cd3 and gprdc5d/cd3 bispecific antibodies for use in cancer therapy
专利号:IL278654A0(申请日:2019年5月15日)
蛋白序列:包含4条关键蛋白序列
![图片]()
![图片]()
图片来源于智慧芽
总结
Teclistamab作为全球首个靶向BCMA x CD3的双特异性抗体,已在多国获批用于多发性骨髓瘤,并在难治性/复发性适应症中展现显著疗效。其联合疗法和特殊审评路径(如中国的附条件批准)进一步扩展了临床应用前景。参考资料来源于:https://www.tecvaylihcp.com/discover-science/以及智慧芽数据库