一、 引言:构建心脏数字孪生的几何基石
在精准医疗和计算生物力学的前沿领域,构建患者特异性的“心脏数字孪生”已成为心血管疾病诊断与治疗规划的核心愿景。数字孪生不仅仅是心脏的三维图像,它是一个集成了结构、功能、电生理和力学特性的动态计算模型。要实现这一目标,第一步也是最关键的一步,便是心脏形状重建——即从临床医学影像(如MRI)中提取精确的三维解剖几何。
然而,这一过程面临着严峻的现实挑战。传统的三维重建往往依赖于高密度的体素扫描,但在临床实践中,为了减少患者的扫描时间或受限于小动物成像的技术条件,医生通常只能获取稀疏的平面轮廓数据。传统的重建方法,如基于样条的插值或统计形状模型,在处理稀疏数据时往往力不从心。前者在高曲率区域容易产生伪影,后者则受限于预定义的人群先验,难以捕捉个体特异的病理重构(如心室瘤或局部室壁瘤样扩张)。
为了解决这一痛点,本文提出了“神经MRI”。这是一种基于神经场的重建框架,它不依赖于人群统计数据,而是通过学习连续的隐式形状表示,直接从稀疏的短轴和长轴MRI切片中恢复高分辨率的心脏几何。这项研究不仅在技术上实现了从“局部插值”到“全局隐式表示”的跨越,更为在稀疏数据限制下的生物力学建模提供了鲁棒的解决方案。
二、核心创新:神经场与分级采样
“神经MRI”的核心在于它如何重新定义“形状”。不同于传统的网格模型,该框架将心脏形状表示为一个连续的隐式函数。具体而言,它使用一个多层感知机来学习一个从三维空间坐标(x,y,z)到占据值(占据概率)的映射。如果一个点位于心脏内部,网络输出1;如果在外部,输出0;如果恰好在边界上,则输出0.5。
为了在稀疏数据下训练这一神经网络,研究团队设计了一套精密的分级采样策略:
1、数据输入:系统输入的是从有限元模拟和活体实验中获得的稀疏短轴和长轴平面轮廓。
2、分级优化:训练过程被分为6个预定义的细化等级(Level 0-5)。在每个等级中,网络进行120次迭代训练。这种从粗到精的策略使得模型能够先捕捉心脏的整体拓扑结构,再逐步学习心肌壁的精细几何特征。
3、损失函数设计:模型优化采用了复合损失函数,结合了二元交叉熵(用于确保预测点集与真实轮廓的准确性)和Eikonal铰链损失(用于强制执行符号距离函数属性,保证表面的平滑性)。
这种架构的优势在于,它利用了所有输入平面的全局空间上下文。即使在某些切片缺失的区域(如心尖或基底部),神经场也能利用全局几何信息进行合理的推断,而不是简单地在两个相邻切片之间画一条直线。
三、实验设计:从硅基模拟到活体验证
为了严格验证“神经MRI”的有效性,研究团队构建了互补的“硅基”与“活体”数据集。这种双重验证策略不仅提供了已知的“金标准”用于量化误差,也证明了模型在真实生物噪声下的鲁棒性。
1、在硅基数据集(有限元模拟):
研究团队利用有限元分析生成了500个双心室(左室和右室)的几何形状。这些模型模拟了真实的心脏解剖结构,包括复杂的肌纤维取向和跨壁的机械各向异性。通过将“神经MRI”重建的结果与这些已知的精确模型对比,研究人员能够量化其在处理复杂几何(如右室不规则的非凸轮廓)时的误差来源。
2、在体内数据集(活体成像):
该数据集包含两部分:
●小鼠成像:对5只野生型小鼠进行了高分辨率的多平面MRI扫描。
●人类患者:回顾性收集了3名患者的短轴和长轴MRI数据。
这些数据经过超分辨率重建和分割,生成了真实的稀疏切片样本,用于测试模型在临床实际条件下的表现。
四、结果评估:几何保真度的突破
研究结果通过Chamfer距离、Hausdorff距离以及高斯曲率误差等多个维度进行了评估,数据有力地支持了该框架的有效性。
1、整体几何匹配度
在所有测试案例中,重建的网格与参考几何形状高度吻合。特别是在体内数据集中,由于采用了更密集的多平面采样协议,模型表现出了亚毫米级的精度(平均误差低于0.1mm)。这证明了在数据条件允许的情况下,“神经MRI”能够生成满足生物力学仿真要求的高质量网格。
2、稀疏条件下的鲁棒性
更具意义的是在稀疏采样条件下的表现。在有限元数据集(模拟稀疏条件)中,尽管整体误差高于体内数据集,但“神经MRI”在解剖学上最具挑战性的区域——左室心尖和基底部——的表现显著优于传统的局部插值方法。
●对比传统方法:传统的样条插值往往会在心尖处产生“截断伪影”或在基底部因切片间距过大而产生扭曲。“神经MRI”利用全局神经场的特性,有效地平滑了这些过渡区域,生成了更符合生理学预期的流线型几何。

3、曲率与形态特征的保持
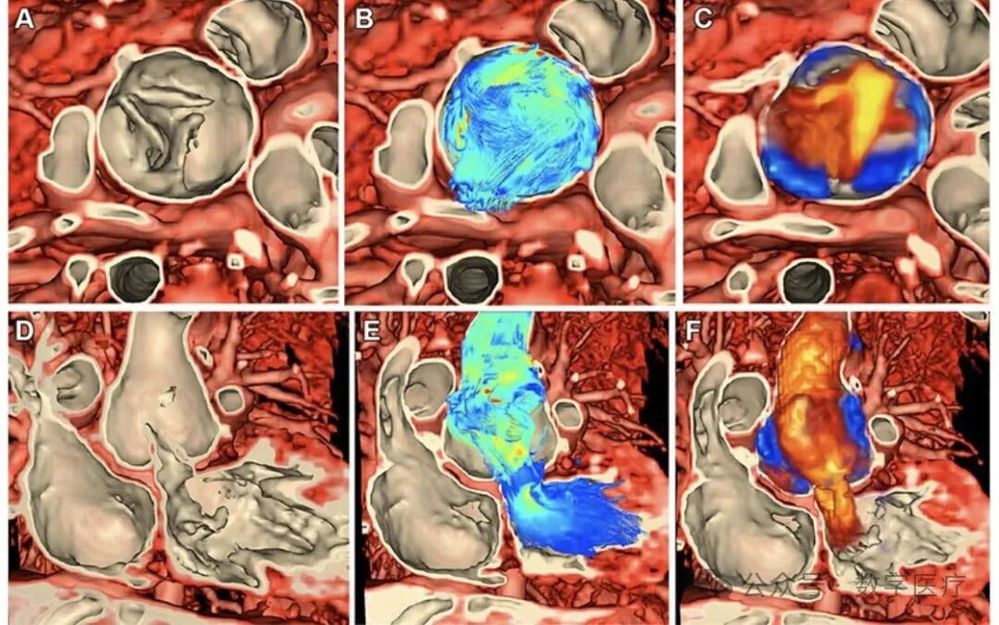
心脏的力学功能高度依赖于其局部曲率。研究发现,虽然稀疏采样会导致右室等高曲率区域的重建误差相对集中,但随着训练等级的提升(从Level 1到Level 5),模型对局部曲率的捕捉能力显著增强。热力图显示,“神经MRI”生成的左室和右室内心内膜表面的曲率分布与真实情况高度相似。
4、动态时序重建
该框架还被扩展应用于心动周期的时序重建。研究团队独立处理了舒张末期和收缩末期等多个时间点。结果显示,尽管在收缩期(体积最小、曲率最大)误差略有增加,但模型依然能够稳定地重建出心脏从舒张到收缩的形态演变,为构建动态的四维心脏数字孪生奠定了基础。
五、深度分析:为何神经场是未来的方向?
这篇文不仅展示了算法的优越性,更深刻地探讨了神经场技术对心脏计算模型的长远意义。
1、摆脱“人口统计学”的枷锁
传统的统计形状模型受限于训练数据的人口平均值。这意味着,如果遇到一个解剖结构罕见的患者(例如严重的右室扩张),统计形状模型可能会强行将其“拉回”平均形状,从而丢失关键的病理特征。“神经MRI”是一种基于病例的个性化学习,它不依赖于先验的形状空间,而是直接从该患者的稀疏切片中学习,这极大地保留了病理重构的特异性。
2、为生物力学仿真提供高质量网格
数字孪生的最终目的是计算仿真。有限元分析对网格质量极其敏感,劣质的网格(如高纵横比或负体积)会导致仿真崩溃。“神经MRI”输出的隐式场通过行进立方体算法提取的等值面,天生具有良好的正则性和平滑度,这为后续的力学模拟提供了理想的初始网格,减少了繁琐的后处理步骤。
3、解决“数据稀疏”的临床现实
在临床和小动物成像中,“时间就是分辨率”。“神经MRI”证明了我们不需要通过延长患者在磁共振机器内的痛苦时间来换取高密度扫描。通过AI的“超分辨率”能力,我们可以从快速、稀疏的临床扫描中,推断出完整的三维结构。这对于儿科成像或无法长时间屏气的患者具有巨大的临床转化价值。
六、局限与展望
尽管成果显著,作者在讨论部分保持了科学家的严谨,指出了当前的局限:
1、时间连贯性缺失:目前的框架是逐帧处理的,没有显式地强制心脏周期各时间点之间的运动一致性。未来的工作将引入循环神经网络或转换模型来学习动态的心脏运动模式。
2、右室重建的挑战:右室复杂的肌小梁结构和非凸几何使得其在稀疏采样下仍比左室更难重建。
3、样本量限制:尽管在小鼠和少量人类案例中表现良好,但仍需更大规模的临床数据验证。
七、结语
本研究是一项连接临床影像与计算生物力学的桥梁式工作。“神经MRI”框架的成功表明,隐式神经表示正在成为医学图像重建的下一代范式。
它不仅解决了从稀疏数据重建心脏几何的工程难题,更重要的是,它为构建真正个性化、高保真的心脏数字孪生提供了可行的路径。在未来,医生或许不再需要等待漫长的高分辨率扫描,只需通过一次快速的常规MRI,AI便能即时生成患者心脏的完整数字副本,用于模拟手术方案、预测药物反应或评估心力衰竭的风险。这项研究将我们带入了这一愿景的现实一步,标志着心脏医疗从“影像观察”向“数字计算”转型的关键里程碑。


The pain of self-discipline will never be as great as the pain of regret. 宁受律己须臾之苦,莫品余生追悔之痛。早上好!
