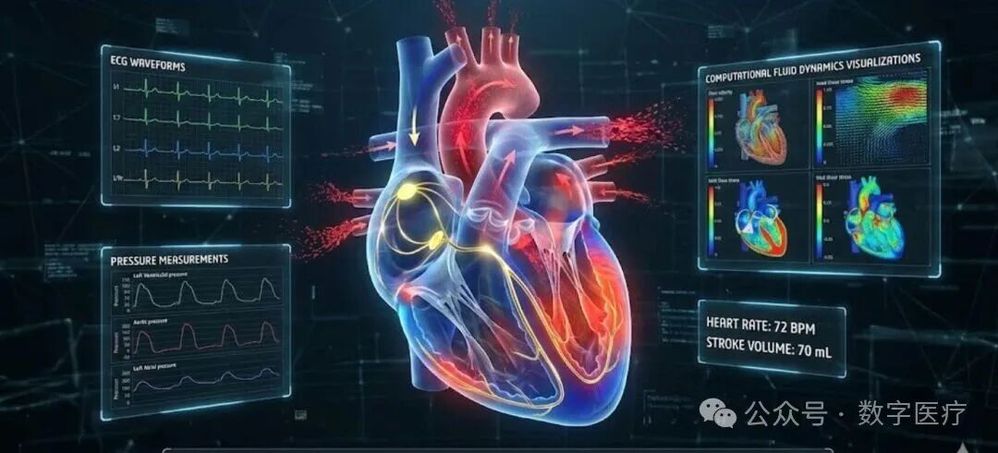
一、引言:医疗AI的“最后一公里”难题
在2026年的今天,尽管“数字孪生”的概念在工业界已相对成熟,但在心血管医学领域,它依然面临着巨大的挑战。现有的计算流体力学(CFD)模型虽然能模拟血流,但往往是“死”的——它们基于通用的几何形状和假设的边界条件,缺乏与特定患者实时数据的交互。
这篇文章的核心贡献在于,它明确指出:数字孪生不仅仅是物理系统的复制品,而是一个动态更新、具有预测能力并能指导决策的双向闭环系统。在冠状动脉疾病(CAD)的背景下,这个系统必须解决一个关键矛盾:临床数据的稀缺性与病理机制的复杂性之间的矛盾。
冠状动脉疾病是西方世界致死率最高的疾病之一。目前的临床评估主要依赖血流储备分数(FFR),但这通常需要侵入性导管检查。而另一个关键指标——壁剪切应力(WSS),被公认为是斑块形成和发展的重要生物力学标志物,但它无法直接通过现有设备测量。本文提出,通过数学手段,将可测量的速度数据(如超声)与不可测量的壁剪切应力联系起来,是构建冠状动脉疾病数字孪生的关键突破口。
二、核心架构:P2D与D2P的双向闭环
本文构建了一个包含五个组件的数字孪生框架:患者(数据源)、采集设备、P2D(物理到数字)、D2P(数字到物理)、临床医生。其中,P2D(数据同化)和D2P(决策合成)是数学挑战最密集的环节。
1、P2D:物理到数字(如何让模型“像”你)
这一步的目标是个性化。即利用患者的稀疏、带噪的观测数据(如超声多普勒速度),修正通用的纳维-斯托克斯方程模型,从而推断出无法直接测量的壁剪切应力。
2、D2P:数字到物理(如何预测未来)
这一步的目标是合成。即利用校准后的模型,预测疾病在未来的发展趋势(如斑块增长),并结合概率图模型(PGM),在不确定性下为医生提供最优的治疗建议(如是否需要植入支架)。
三、技术攻坚:P2D阶段的三种数学武器
本文详细探讨了三种将“数据”融入“物理模型”的数学方法,旨在解决壁剪切应力的快速、精准估算问题。
1、变分降阶模型数据同化
这是最经典的“最优控制”思路。
●原理:将边界条件(如进出口压力)视为控制变量。通过调整这些变量,最小化模型计算出的速度与超声实测速度之间的误差。
●挑战与对策:直接求解流体力学方程(全阶模型)计算成本极高,无法满足临床实时性要求。因此,作者引入了降阶模型。
●核心机制:利用POD(本征正交分解)从大量全阶模型数据中提取“特征基”,将高维的流体方程投影到低维空间(加勒金降阶模型)。这使得在“离线阶段”训练模型,在“在线阶段”秒级响应成为可能。
●意义:这种方法证明了,在非侵入性数据(超声)的帮助下,我们可以反向推演出导致这些血流模式的生物力学环境(壁剪切应力)。
2、连续降阶模型数据同化
这是受气象学启发的“连续松弛”方法。
●原理:不需要复杂的优化迭代。直接在流体方程中加入一个“松弛项”(µ(IH(u)−IH(v))),这个项的作用就像一个弹簧,当模型模拟值偏离观测数据时,就把它“拉”回来。
●优势:数学证明,只要观测数据足够,这种方法能保证模拟结果指数级收敛于真实解。
●本文的创新点:作者首次将这种“连续同化”思想应用到了降阶模型中(即CDA-降阶模型)。这解决了传统降阶模型在“解析度不足”或“数据稀缺”情况下容易发散的问题。本文指出,这种方法在处理冠状动脉这种复杂的几何形状和高雷诺数流动时,具有极高的鲁棒性。
3、基于物理信息神经网络的数据同化
这是当下最热门的“科学机器学习”路径。
●原理:训练一个神经网络,使其不仅满足观测数据,还要满足纳维-斯托克斯方程的残差为零。
●突破:文章展示了初步的未发表数据(DeepXDE库),表明引入数据同化后的PINN(DA-PINN)在速度和压力场的重构精度上远超传统PINN(误差从7%降至0.2%左右)。
●潜力:PINN天然适合处理不规则几何和边界条件,且无需网格生成,这为处理患者特异性的冠状动脉复杂解剖结构提供了巨大的想象空间。
四、决策升级:D2P阶段的智能推演
当数字孪生体通过P2D阶段成功构建后,它不仅仅是一个“镜子”,更是一个“预言家”。文章在D2P阶段提出了两个关键的数学升级方向:
1、带“记忆”的概率图模型
传统的决策模型往往是马尔可夫性的(即下一时刻只与当前时刻有关)。但在CAD治疗中,历史趋势至关重要。
●创新:文章提出引入多步马尔可夫链。即未来的状态不仅取决于现在的WSS值,还取决于过去k个时间步的WSS变化率。
●临床意义:一个患者虽然当前风险评分不高,但如果斑块增长率突然飙升,其治疗策略应与一个长期稳定高风险的患者截然不同。这种“带记忆”的模型能更敏锐地捕捉到这种急性变化。
2、多保真度融合
临床数据是分层的:既有高频低质的可穿戴设备数据(如智能手表),也有低频高质的影像数据(如CT/MRI)。
●策略:本文提出构建一个分层的图网络,将不同保真度的数据源整合在一起。利用低阶模型(如0D/1D电路模拟)处理大量低质数据,利用高阶模型(3D CFD)处理关键的高质数据,并在非线性流形空间中进行融合。
●价值:这解决了单一模型无法兼顾计算效率与精度的矛盾,使得数字孪生系统能够全天候、多维度地监控患者状态。

五、深度解析:为什么这是心血管医学的未来?
这篇文章不仅仅是一堆复杂的数学公式,它揭示了心血管医学从“经验主义”向“计算主义”转型的必然逻辑。
1、填补了“不可测”的空白
目前的医疗设备无法直接给血管壁“测应力”。这篇文章通过数学同化,成功地将“可测的速度”映射到了“不可测的应力”。这意味着,未来医生可能只需要做一个无创的超声检查,就能通过后台的数学模型,精准获知患者血管内壁的受力情况,从而在斑块破裂前进行干预。
2、解决了“个性化”的算力瓶颈
过去,为每个患者定制一个CFD模型需要数天甚至数周的计算时间。通过本文中提到的降阶模型和数据同化结合,计算时间被压缩到了临床可接受的范围内(如15分钟内)。这使得“千人千面”的精准医疗在经济和技术上变得可行。
3、引入了“动态决策”的概念
传统的临床决策往往是静态的(基于一次检查结果)。本文提出的D2P框架,将治疗变成了一个动态优化过程。它模拟了疾病在不同治疗方案下的未来演化,让医生能“预演”治疗结果,从而选择最优解。
六、行业启示与挑战
基于本文的结论,我们可以预见以下行业变革:
1、从“影像诊断”到“计算诊断”的范式转移
未来的医学影像报告可能不再仅仅是“发现斑块”,而是会包含由数字孪生系统计算出的“生物力学风险图谱”。 壁剪切应力指标有望成为继血流储备分数之后,评估心血管风险的下一个金标准。
2、数学与临床的深度融合
本文最后强调,构建数字孪生不仅是工程师的任务,更是数学家的任务。未来的临床科室可能需要配备“计算数学专家”,或者像本文作者呼吁的那样,建立标准化的多中心数据协议,以训练更强大的数学模型。
3、依然存在的挑战
尽管前景广阔,本文也诚实地指出了当前面临的挑战:
●几何重构:如何从医学影像中快速、自动地提取冠状动脉的几何形状依然是一个难点(特别是对于植入了支架的血管)。
●软组织力学:目前的模型主要关注流体(血液),未来需要更深入地耦合血管壁的生物力学响应(流固耦合)。
●严格的验证、确认与不确定度量化:数字孪生的临床可信度是其应用的基石。由于缺乏直接测量的“金标准”(如体内真实的WSS分布),建立一套严格的验证与不确定度量化流程至关重要。这包括利用体模实验、动物模型以及多中心临床数据来评估模型的预测误差。

七、结语
这篇文章为2026年的精准医疗提供了一份极具分量的“施工图纸”。
它告诉我们,数字孪生在心血管领域的落地,不靠单纯的算力堆砌,而靠数学智慧的注入。通过将数据同化(DA)作为连接现实与虚拟的桥梁,将降阶模型作为实现实时计算的引擎,这篇文章成功地将冠状动脉疾病的治疗从“事后补救”推向了“事前预测”。
这不仅是数学家的胜利,更是患者的福音。它预示着,在不久的将来,我们每个人或许都能拥有一个在计算机中跳动的“数字心脏”,它将提前预警风险,为生命争取最宝贵的窗口期。
如需要《冠状动脉疾病的数字孪生:一条数学路径》(英文,共22页),请在本微信公众号中赞赏(点喜欢或稀罕作者后按本公众号设定打赏)后,发来email地址索取。



Self-respect is knowing your worth without needing validation from anyone else. It's choosing peace over proving a point and walking away from what disrespects your value. When you respect yourself, you set the standard for how others treat you. Never shrink yourself to fit where you're not appreciated. 自尊,是深知自身的价值,而无需他人的认同来证明。它是在纷争中选择安宁,而非执意争辩;是在尊严受损之处,转身离去的从容。当你真正尊重自己,也就为他人如何对待你立下了标高。切莫为求被接纳,而委屈自己去契合那不珍惜你的所在。早上好!
