引言
抗体药物偶联物(ADC)技术的进步和新抗原靶点的识别,正将ADC重新定位为转移性去势抵抗性前列腺癌的一种有前景的治疗平台。ADC是一类新型生物治疗药物,将单克隆抗体的特异性与小分子载荷的细胞毒性相结合。这些抗体靶向主要在癌细胞上过表达的细胞表面抗原,通过连接子与载荷相连,连接子设计有不同的循环稳定性,以响应细胞内触发因素或在靶点位的抗体降解而释放载荷。ADC的作用机制涉及抗体-抗原结合、内吞、内体-溶酶体融合、溶酶体降解以及细胞毒性载荷的释放。
目前,ADC采用三类主要的细胞毒性载荷:微管破坏剂(如maytansinoids、tubulysin和auristatin)抑制微管聚合;喜树碱衍生物(如伊立替康、拓扑替康、甲磺酸依沙替康、deruxtecan)抑制拓扑异构酶I(TOPI);以及DNA烷化剂(如吡咯并苯并二氮杂卓和杜卡霉素)导致DNA交联,最终诱导凋亡。选择载荷时的重要考虑因素包括足够的效力、稳定性、功能基团可修饰性、诱导旁观者杀伤效应的能力以及水溶性。
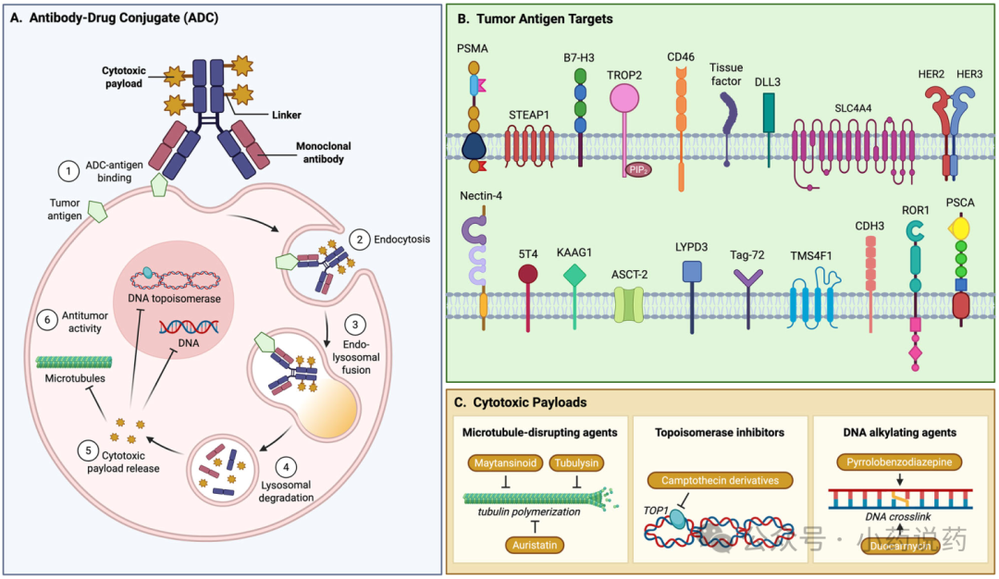
前列腺癌中潜在的抗原靶点非常丰富,包括PSMA、STEAP1、B7H3、TROP2、CD46、组织因子、DLL3、SLC44A4、HER2、HER3、Nectin-4、5T4、KAAG1、ASCT-2、LYPD3、Tag-72、TMS4F1、CDH3、ROR1和PSCA。以下将详细阐述针对这些靶点的ADC临床进展。
-02-
一、前列腺特异性膜抗原(PSMA)
PSMA是一种主要在前列腺细胞中发现的跨膜蛋白,其表达随着前列腺恶性肿瘤的进展而增加,特别是在雄激素剥夺疗法(ADT)后表达上调,使其成为治疗CRPC的重要靶点。PSMA具有内化信号,抗体-PSMA复合物可通过网格蛋白包被的小窝内化进入内体区室,有利于ADC载荷释放。
多项PSMA靶向ADC已进入临床开发。MLN2704是首个完成I期临床试验的PSMA-ADC,载荷为DM1,在23名mCRPC患者中显示出剂量依赖性药代动力学和一定的抗肿瘤活性,但随后的I/II期试验发现其二硫键连接子不稳定导致显著神经毒性,最终被终止。PSMA ADC(MMAE载荷)在I期试验中显示出初步活性,但在II期试验中因过早解偶联导致的脱靶毒性(≥3级神经毒性24%)而停止开发。MEDI3726(PBD载荷)也因抗体重链-轻链解离导致的脱靶效应而停止开发。
目前,ARX517(载荷为AS269)正在进行首个人体I期试验APEX-01,采用稳定的肟偶联技术,在剂量递增阶段显示出可控的安全性和初步疗效。尽管许多PSMA靶向ADC因疗效和毒性问题未能成功,但PSMA仍是一个重要靶点,特别是随着PSMA-PET和177Lu-PSMA-617的成功,进一步优化连接子技术可能改善PSMA-ADC的前景。
-03-
二、B7H3
B7H3是前列腺癌ADC的另一个有前景靶点,在前列腺肿瘤细胞中过表达,与疾病扩散和不良预后相关。Vobramitamab duocarmazine(MGC018,Duocarmycin载荷)在临床试验中显示出一定的抗肿瘤活性,但因高剂量调整率和致命不良事件而停止开发。
Ifinatamab deruxtecan(I-DXd,DXd载荷)在晚期实体瘤患者的I/II期试验中显示出可控的安全性和令人鼓舞的抗肿瘤活性,在mCRPC患者中客观缓解率较高,展示了TOPI抑制剂载荷在CRPC中的潜力。YL201(TOPI抑制剂载荷TMALIN®)在晚期实体瘤中显示出总体有前景的抗肿瘤活性,但血液学毒性较常见。DB-1311/BNT324(专有TOPI抑制剂载荷)已被FDA授予快速通道资格,初步数据显示疗效令人鼓舞且安全性可控。此外,HS-20093、MHB088C和MGC026等B7H3靶向ADC也在临床开发中。
-04-
三、STEAP1
-05-
四、TROP2
Trop2促进前列腺癌生长、转移和治疗耐药,其表达与不良结局有关,也可能在神经内分泌分化表型中起作用。Sacituzumab govitecan(SG,SN-38载荷)在mCRPC的II期研究中未观察到PSA50反应。ESG401(SN-38载荷)在预治疗实体瘤中显示出良好安全性特征和有前景的抗肿瘤活性。Datopotamab deruxtecan(Dato-DXd,DxD载荷)在多种实体瘤中显示出有意义的临床活性,目前正在评估其在包括mCRPC在内的实体瘤中的应用。MHB036C也是一种正在研究的TROP2靶向ADC。
-06-
五、CD46
CD46在晚期前列腺癌中高表达。FOR46(MMAE载荷)在I期研究中显示出可接受的安全性特征和临床活性,部分患者达到PSA50下降和肿瘤缩小。临床前模型显示恩扎卢胺可增加CD46表达,支持FOR46与恩扎卢胺联合使用的试验。
-07-
六、组织因子(TF)
TF在前列腺癌中富集,与疾病进展和预后不良有关。XB002(auristatin载荷zovodotin)在I期试验中耐受性良好,但因无法与现有TF靶向ADC竞争而被终止。Tisotumab vedotin(MMAE载荷)已获批用于宫颈癌,在实体瘤(包括CRPC)的试验已完成,但未报告CRPC特定数据。
-08-
七、Delta样配体3(DLL3)
DLL3在具有神经内分泌特征的CRPC和新生神经内分泌前列腺癌(NEPC)中表达。Rovalpituzumab tesirine(Rova-T,PBD载荷)因毒性、疗效有限和缺乏生存获益而停止开发,但DLL3仍是NEPC的相关靶点,Tarlatamab等DLL3靶向药物显示出有前景的活性。
-09-
八、其它靶点
SLC44A4:ASG-5ME(MMAE载荷)因显著毒性和有限抗肿瘤活性而停止开发。
HER2:虽然缺乏前列腺癌特定数据,但基于乳腺癌的成功,HER2靶向ADC(如T-DXd)在HER2表达的NEPC病例报告中显示出实质性反应。A166也在临床研究中。
HER3:HER3在致死性前列腺癌中频繁过表达。HER3-DXd和DB-1310正在开发中,并在临床前模型中显示出活性。
Nectin-4:Enfortumab vedotin(EV,MMAE载荷)在重度预治疗难治性mCRPC患者中显示出有前景的疗效和可控的安全性。LY4101174和LY4052031等下一代ADC也在开发中。
5T4:TUB-030(exatecan载荷)正在进行I/II期试验。
KAAG1:ADCT-901(PBD载荷)已完成I期试验。
ASCT2:MEDI7247(PBD载荷)已完成I期试验。
LYPD3:Lupartumab amadotin(auristatin载荷)因招募不足而终止。
TAG-72:TGW101(MMAE载荷)正在研究中。
TM4SF1:AGX101(maytansinoid载荷)正在研究中。
ROR1:CS5001(PBD载荷)在I期试验中显示出有前景的抗肿瘤活性。
P-cadherin (CDH3):BC3195(MMAE载荷)是唯一在临床试验中的CDH3靶向ADC。
PSCA:虽无ADC在临床开发,但临床前数据显示首个基于全人源抗PSCA抗体的ADC在异种移植模型中有效。
-10-
结语
随着肿瘤学领域继续朝着个性化和有针对性的方法发展,ADC有望成为前列腺癌的治疗策略。这里回顾了一些最相关的细胞毒性有效载荷,分子靶标和ADC,这些已经证明在前列腺癌中具有治疗潜力。这些ADC将有效的微管干扰物,拓扑异构酶抑制剂和DNA烷基化剂结合到靶向前列腺癌细胞表面过表达的抗原的抗体中,包括PSMA,B7H3,STEAP1,TROP2,CD46,TF,DLL3,SLC44A4,HER2,HER3,Nectin-4,5T4,KAAG1,ASCT2,LYPD3,Tag-72,TM4SF1,CDH3,ROR1和PSCA。然而,由于安全性和特异性问题,尚未批准ADC用于治疗前列腺癌。因此,需要进一步的开发和创新,既要改进现有的ADC,又要开发具有最佳目标,连接器和/或有效载荷的新型ADC。随着ADC技术在前列腺癌领域的不断进步,ADC为改善临床结果和提高患者的生活质量提供了新的希望。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
