▎Armstrong
2026年2月23日,和铂医药宣布将新一代CTLA-4抗体HBM4003大中华区外全球权益授权Solstice Oncology,后者支付逾1.05亿美元前期对价,包括5000万美元首付款,500万美元近期付款以及价值逾5000万美元的公司股权。此外,和铂医药还将获得最高11亿美元的里程碑付款,以及分级销售分成。Solstice Oncology为一家多个头部风险投资机构联合创立的临床阶段生物技术公司,此次合作为NewCo模式。

CTLA-4为肿瘤免疫领域重要靶点之一,获批在PD-1之前,不过首个上市的Yervoy由于毒性大,在临床上的应用受到很大限制。HBM4003为和铂医药自主研发的新一代CTLA-4抗体,采用了全新设计,对CTLA-4具有更高亲和力,同时采用重链抗体形式。临床前研究数据表明,HBM4003肿瘤组织渗透性更好,Fc通过工程化改造增强ADCC活性,可以更高效清除肿瘤微环境的Treg。
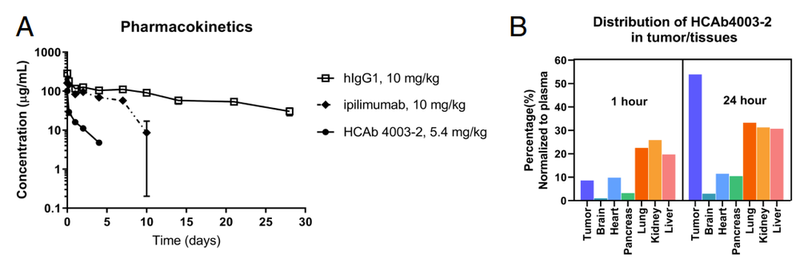
此外,HBM4003血浆中药物半衰期则更短,从而安全性有显著提升,扩大了治疗窗。HBM4003已经在临床中观察到更好的安全性特征,同时在结肠癌、肝癌和神经内分泌瘤等多个瘤种观察到明显疗效,有望充分释放CTLA-4靶点的价值。
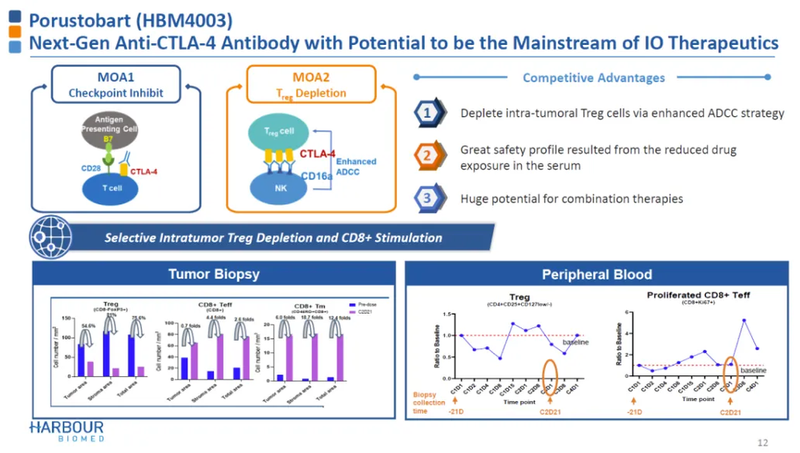
和铂医药HBM4003此次合作创造了CTLA-4抗体BD出海的新纪录,也为CTLA-4老靶点焕发新生机的重要尝试。
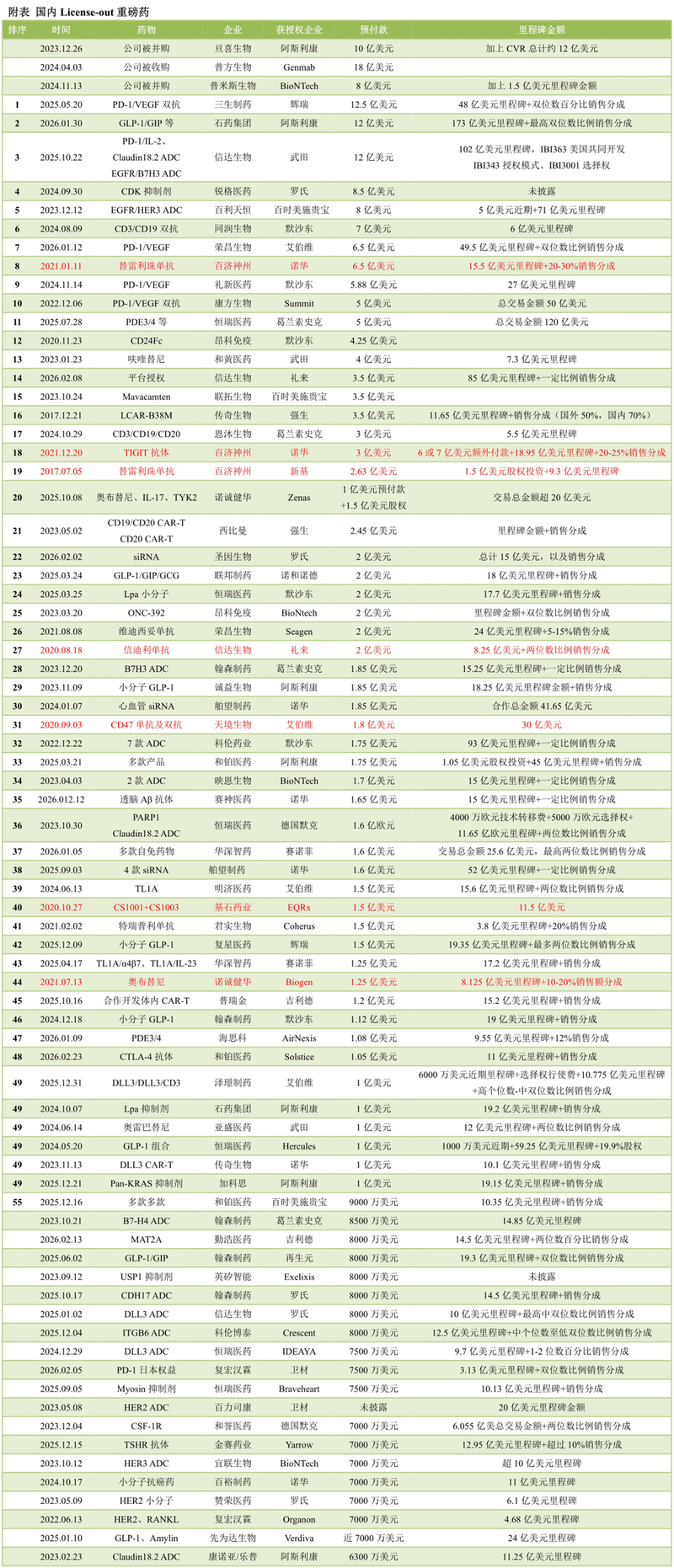
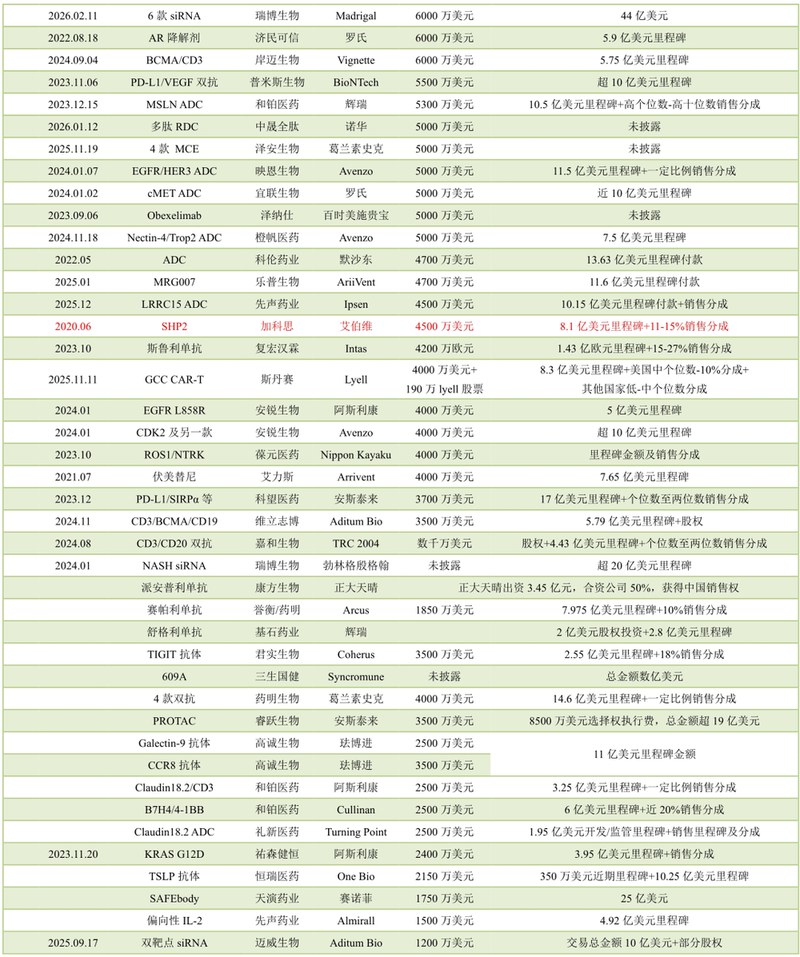
IO领域,和铂医药进行了全方位的迭代产品布局,除了新一代CTLA-4抗体外,和铂医药还开发了DCCE的PD-L1/CD40双抗,以及PD-1/VEGF大热之后的PD-1/VEGF/未披露靶点三抗迭代分子,整合IO、抗血管、肿瘤间质多种机制,旨在达到延长OS这一最终目标,同时进一步改善安全性以实现迭代标准疗法的目标。

总结
Treg在免疫系统中扮演重要角色,CTLA-4靶点已经完成POC,但仍需要解决第一代CTLA-4抗体毒性大的问题,HBM4003为代表的新一代CTLA-4抗体针对性的做了差异化设计,最大限度规避毒性问题,强化肿瘤组织渗透性和疗效,有望最大化释放CTLA-4靶点的价值。
2025年的诺贝尔生理学或医学奖被授予Treg发现者及其开关Foxp3的发现者,Treg在外周免疫耐受中扮演核心角色,其转化研究的潜力仍有待继续深挖。HBM4003通过更高效的Treg清除,实现有效性与安全性的更佳平衡。此次NewCo出海将加速HBM4003的全球临床开发,为IO迭代研发注入新的动能。

和铂医药连续达成重磅BD出海合作,仅MNC中就有阿斯利康、艾伯维、百时美施贵宝、辉瑞、大塚制药等,累计对外合作总金额超过120亿美元。更重要的是,和铂医药的BD合作覆盖范围极为广泛,既有双抗/多抗这样的迭代产品和技术,也有此次合作的全新作用机制的新一代CTLA-4抗体,充分体现了和铂医药同时深耕工程化和biology的深厚积累。

Armstrong技术全梳理系列
和铂医药技术全梳理; 荣昌生物技术全梳理; 再鼎医药技术全梳理; 药明生物技术全梳理; 恒瑞医药技术全梳理; 豪森药业技术全梳理; 正大天晴技术全梳理; 吉凯基因技术全梳理; 基石药业技术全梳理; 百济神州技术全梳理; 百济神州技术全梳理第2版; 信达生物技术全梳理; 信达生物技术全梳理第2版; 中山康方技术全梳理; 复宏汉霖技术全梳理; 先声药业技术全梳理; 君实生物技术全梳理; 嘉和生物技术全梳理; 志道生物技术全梳理; 道尔生物技术全梳理; 尚健生物技术全梳理; 康宁杰瑞技术全梳理; 科望医药技术全梳理; 岸迈生物技术全梳理; 礼进生物技术全梳理; 康桥资本技术全梳理; 余国良的抗体药布局; 荃信生物技术全梳理; 安源医药技术全梳理; 三生国健技术全梳理; 仁会生物技术全梳理; 乐普生物技术全梳理; 同润生物技术全梳理; 宜明昂科技术全梳理; 派格生物技术全梳理; 迈威生物技术全梳理; Momenta技术全梳理; NGM技术全梳理; 普米斯生物技术全梳理; 普米斯生物技术全梳理2.0; 三叶草生物技术全梳理; 泽璟制药抗体药全梳理; 恒瑞医药抗体药全梳理; 齐鲁制药抗体药全梳理; 石药集团抗体药全梳理; 豪森药业抗体药全梳理; 华海药业抗体药全梳理; 科伦药业抗体药全梳理; 百奥泰技术全梳理; 凡恩世技术全梳理。