
近日,专注于肿瘤靶向核药(放射性药物)研发的Aktis Oncology完成首次公开募股(IPO),以每股18.00美元的发行价,在纳斯达克全球精选市场挂牌交易(股票代码:AKTS),预计总募资额达3.645亿美元。此前,Aktis已通过四轮融资募集3.31亿美元,吸引了Janus Henderson Investors、RA Capital Management等知名医疗健康投资机构。
2024年5月,Aktis与礼来达成战略合作,共同开发针对实体瘤的放射性药物。根据协议,Aktis将获得6000万美元的预付款,以及高达11亿美元的里程碑付款和销售版税。此外,礼来还将进行一笔未披露金额的股权投资。
合作达成后,礼来将获得Aktis针对其选定靶点研发的放射性药物的全球开发、生产和商业化权利。Aktis将保留全部七条自有管线的资产所有权,其中包括针对Nectin-4的临床阶段项目。
这家成立于2020年的Biotech,深耕靶向α放射性粒子疗法领域,凭借专有的微型蛋白放射性偶联物(RDC)平台,拥有AKY-1189(靶向Nectin-4)和AKY-2519(靶向B7-H3)两大原研载体骨架,核心管线覆盖多种靶点高表达的实体瘤。
01
从药物研发到产融结合,Aktis团队多领域专家实现全链路把关
Aktis组建了一支由医疗健康行业专家组成的核心管理团队,团队成员在各自领域拥有长期从业经验。
该团队构建起药物研发、临床落地以及资本衔接的多领域架构,由总裁兼首席执行官Matthew Roden博士领衔,其兼具生物制药行业、医疗股票资本平台的管理背景,曾领导外部创新的研发团队处理累计价值超过1250亿美元的业务发展交易,还拥有免疫学和结构生物学的学术基础。
首席技术官Tyler Benedum博士牵头技术研发,拥有十六年从业经验,曾就职于礼来公司全资子公司Avid Radiopharmaceuticals(聚焦诊断放射药物研发),推进AMYVID和TAUVID(均为阿尔茨海默病PET诊断影像剂)上市与商业化授权;研发团队成员还包括首席医疗官Akos Czibere博士,其深耕药物开发领域近20年,成功领导多个全球实体肿瘤和血液恶性肿瘤注册项目,并推动ADC、双抗等多款疗法在全球多地获批;以及首席科学官Paul L.Feldman,其专注于新型肽治疗药物研发,曾独角兽企业Intarcia Therapeutics的管理团队任职。
在产业运营与资本管理层面,首席财务官Kyle Kuvalanka拥有超20年生物制药行业的高级领导经验,曾负责Syros Pharmaceuticals与Blueprint Medicines两家制药上市公司的财务与业务职能建设;首席运营官Shulamit Ron-Bigger博士则曾任百时美施贵宝研发与早期开发组织的战略与运营主管,具备战略开发与运营经验。
02
专有微型蛋白技术平台,与礼来达成平台型合作
放射性药物凭借其精准诊疗优势,在肿瘤治疗领域占据重要地位。Statifacts机构数据显示,2024年全球放射性药物市场规模已超67.4亿美元,预计到2034年将达到约144.4亿美元,2025年至2034年的复合年增长率为8.2%,其中癌症治疗是主要增长力。
但这个高潜力赛道仍面临着多重挑战,主要包括:监管要求严格、高生产成本、放射性物质安全处置困难,以及放射毒性控制要求高等;同时,传统放射性药物还存在靶点识别不精准的技术局限,进一步放大了正常组织损伤的可能性。
Aktis技术平台针对放射性药物领域的痛点,自主研发微型蛋白作为靶向载体,结合α放射性同位素构建靶向放射药物分子,该药物具备三大差异化技术优势:
■ 靶向载体设计独特
采用分子量远小于传统抗体蛋白的微型蛋白(<10kDa)作为靶向载体,经特异性修饰后,可定向识别肿瘤细胞表面的靶点糖蛋白,高效渗透并富集于肿瘤细胞内部,实现药物对肿瘤细胞的集中作用。此外,通过基因工程改造,该载体可加速患者体内残留药物的清除,降低全身同位素暴露风险。
■ 高能杀伤,射程精准可控。
靶向载体携带的α放射性同位素在衰变过程中,会释放强杀伤力的α粒子,能够直接破坏肿瘤细胞双链DNA,实现精准杀伤。同时,由于α粒子射程短且可控,可有效减少对周围正常组织的波及,进一步提升用药安全性。
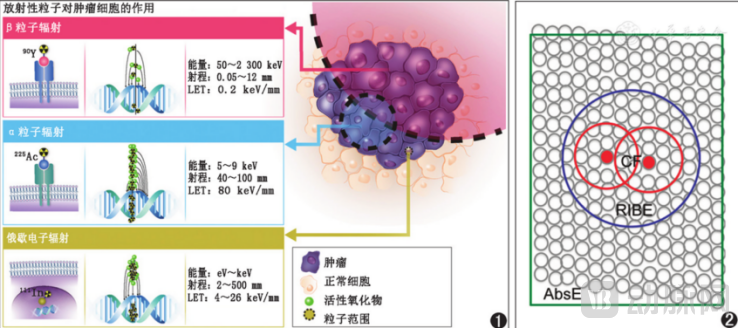 α粒子放射治疗原理(图源:《中华核医学与分子影像杂志》)
α粒子放射治疗原理(图源:《中华核医学与分子影像杂志》)
■ 诊疗一体化
基于诊疗一体化设计的药物,可与同位素68Ga和177Lu安全结合——先用68Ga标记进行PET成像诊断,通过影像工具准确定位肿瘤,并验证药物与靶点的结合情况;再以177Lu标记开展后续治疗,实现“诊断—治疗“的无缝衔接。这种可视化的治疗流程,能更精准地筛选出潜在获益人群。
值得关注的是,与礼来的合作中,Aktis并未出让任何现有管线资产,而是依托自有技术平台达成平台型合作,针对礼来选定的一组特定靶点上开展放射性药物(治疗+诊断)的研发。
03
双管线布局潜力靶点,覆盖多类实体瘤
依托微型蛋白技术平台,Aktis聚焦Nectin-4和B7-H3两大高潜力肿瘤靶点,通过偶联同位素225Ac,验证其两大核心靶向载体骨架。
Aktis管线进展(AKY-1189与AKY-2519)
■ AKY-1189:全球首款Nectin-4靶向微型蛋白载体
Nectin-4是一个经临床研究充分验证的优质靶点,能够促进肿瘤细胞增殖、迁移和侵袭;在成人健康组织中低表达,而在尿路上皮癌、乳腺癌、头颈部肿瘤等多种肿瘤中显著过表达。
当前,Nectin-4 ADC已形成梯度竞争——从市场布局看,海外已有安斯泰来的Enfortumab vedotin获批上市,礼来的两款ADC药物ETX-22与LY4052031也均处于Ⅰ期临床试验阶段;国内赛道同样活跃,迈威生物的9MW2821临床数据亮眼,该药已在宫颈癌领域启动单药Ⅲ期临床试验,并在三阴乳腺癌中开展与PD-1联合治疗的Ⅱ期临床试验,临床进展处于国内前列;百奥泰的BAT8007也于2023年启动Ⅰ期临床试验。
不过,靶向Nectin-4的治疗性放射性药物研发仍处于空白阶段。这正是Aktis的突围机会。
AKY-1189是Aktis研发的全球首款Nectin-4靶向微型蛋白载体,具有first in class潜力,经优化可作为放射性核素的靶向载体骨架,偶联225Ac、177Lu、68GA等核素形成完整放射性药物,精准靶向Nectin-4蛋白。
其核心产品[225Ac]-AKY-1189,于2025年4月获FDA临床试验许可,同年5月进入Ⅰb期临床试验,除用于转移性尿路上皮癌(MUC)的治疗外,还有望拓展至所有高表达Nectin-4的肿瘤。临床前研究数据显示,其在受试对象体内安全性良好,对正常组织器官无明显损伤,且未出现因药物蓄积而引起的慢性毒性反应。
■ AKY-2519:B7-H3靶向微型蛋白载体
免疫检查点糖蛋白B7-H3在正常细胞中低表达或不表达,而在多种恶性肿瘤细胞及肿瘤浸润性免疫细胞(如单核细胞、骨髓源性抑制细胞MDSC、巨噬细胞等)中高表达。该蛋白通过抑制免疫功能,可促进巨噬细胞极化、影响树突状细胞功能,从而调控抗肿瘤免疫应答,并且还能够介导肿瘤细胞的增殖、侵袭和转移,从而促进肿瘤生成。
当前针对携带B7-H3靶点的肿瘤细胞存在多种治疗方法,且路径开发持续传来利好消息,但均具有一定局限性。例如,单克隆抗体疗法用于治疗卵巢癌和非小细胞肺癌,但伴随有安全性问题,适用人群有限;纳米抗体疗法可治疗多种实体瘤,组织穿透能力却不足;双特异性抗体疗法可提升T细胞介导的肿瘤杀伤效应,同时存在诱发细胞因子风暴的风险;虽然CAR-T细胞疗法的肿瘤杀伤效果显著,但仍受肿瘤微环境抑制、抗原异质性等问题的制约。
基于自主研发的AKY-2519靶向载体骨架,Aktis推出[225Ac]-AKY-2519,目前处于临床前研究阶段,计划于2026年提交IND申请;适应症瞄准非小细胞肺癌、卵巢癌等B7-H3高表达的肿瘤,有望填补相关治疗空白。
不仅如此,对于放射性药物这类活性会随着时间衰减的特殊产品而言,临床阶段的规模化生产与“准时交付”同样是核心挑战。Aktis深度介入从生产到配送的全流程管理,以确保药物能以最佳活性状态送达临床研究中心。
从解决放射性药物安全与精准性的痛点,到聚焦热门靶点的稀缺靶向疗法,Aktis力求从高热度的放射药赛道突围,在竞争激烈的市场中,开辟一条兼具市场价值与行业影响力的差异化道路。
如果您想对接文章中提到的项目,或您的项目想被动脉网报道,或者发布融资新闻,请与我们联系;也可加入动脉网行业社群,结交更多志同道合的好友。


近
期
推
荐



