肿瘤类器官是一类新型的体外疾病模型。相较于传统实验应用的2D细胞系,肿瘤类器官拥有其无法比拟的3D异质性结构,能够继承患者的肿瘤表型。同时,肿瘤类器官避开了动物模型所面临的种属差异问题,大幅降低了实验成本及周期,提高临床一致性,在药物研发、个性化用药指导等多种应用中有着显著的优势。
器官芯片(Organoid-on-a-chip)则是微流控技术与类器官技术交叉融合发展的新兴技术。它在传统的类器官培养基础上,利用芯片平台实现了对培养环境的精准调控,可以进行高通量培养和精准模拟复杂的生理环境(如肿瘤微环境、呼吸道屏障等)。
具体而言,器官微流控芯片通过设计明确的培养室和精确控制连续流动,实现类器官的三维培养,有效提高类器官模型构建的成功率和药物筛选准确性,具有更高的可控性和仿生性,进而可实现动态持续监测、单一系统集成多种生物学功能、高通量药物筛选等。
成立于2023年7月的广州逸芯生命科学有限公司(后简称“逸芯生命科学”)是一家致力于体外工程化器官芯片全流程技术开发的公司,为罕见病,肿瘤等复杂疾病药物研发提供更加科学有效的体外疾病模型。在创始人、首席科学家刘杰教授的带领下,逸芯生命科学已实现培养材料、芯片功能、微流控培养系统等多点创新,推出应用于疾病机制探索和创新药物开发的器官微流控芯片产品。

刘杰,中山大学教授/博导,生物医学工程学院院长助理,美国耶鲁大学博士,中国生物材料学会再生医学材料分会委员、中国生物材料学会生物材料先进制造分会委员、逸芯生命科学创始人兼首席科学家。主持包括国家科技部重点研发、国家自然科学基金、广东省科技厅国际合作项目等20余项课题,在Nature Materials、Advanced Science、Biomaterials、ACS Nano等国际著名杂志发表研究论文80余篇;获授权专利10余项,已转化2项。研究方向包括:类器官与器官芯片;纳米材料用于药物递送和基因治疗;干细胞再生医学等。
医工交叉科学家团队,打造国际首个器官芯片全流程平台
药物开发和精准治疗的关键环节在于高通量构建合适的体外生理模型,但传统药物研发评价流程具有一定局限性。比如2D细胞培养难以模拟组织微环境、缺少体内模拟的动态条件;动物肿瘤模型难以实时监测药物与细胞的相互作用,难以满足新型细胞治疗、免疫治疗和基因治疗方法的有效性评价,以神经系统疾病药物开发为代表的模型匮乏。
人体组织和器官往往由具有特殊结构的功能单元构成,并且不同功能单元之间也存在着相互作用。而普通的三维模型往往难以实现这样多结构、多尺度、多组分微环境的模拟。类器官通过三维支架材料,具有干性的细胞可在仿生三维环境中增殖、诱导分化并与相邻细胞相互作用,形成结构功能与真实组织相似的体外模型。
因此,逸芯生命科学致力于开发药物研发新范式——器官芯片微生理系统,打造国际首个器官芯片全流程平台,通过器官芯片,实现高通量、快速、精准和智能的药物开发,实现升级版的干湿实验闭环结合,颠覆传统药物研发流程。
在逸芯生命科学深耕的器官微流控芯片中,微流控技术能够在体外进行精确的流体、机械力、结构和组分的调控。细胞可以培养在定制化的微环境中,在多组分的协同作用下,完成对组织和器官的功能的模拟,实现器官芯片的构建。此外,通过微流控装置设计,体系内还可施加仿生力学刺激,如流体剪切应力、循环应变、机械压缩等,这大大拓展了可调控的体外仿生病理生理微环境。
不过,微流控技术与类器官技术跨领域、跨学科的交叉融合给研发团队提出了很高要求——既需要拥有生物学知识、又需要具备医工交叉的研发经历,结合器官芯片应用场景,还需要具备药物临床前及临床研发经验。刘杰教授带领下,逸芯生命科学建立起一支具备医工交叉背景的科学家团队:研发团队来自耶鲁,中大,港科大等知名高校,具有微加工、组织工程、材料、生物学等交叉学科背景,完全匹配器官芯片研发体系。
推出国内首款新型类器官培养基质胶,建设产品级设计、加工和建模平台
在打造国际首个器官芯片全流程平台的大目标下,逸芯生命科学从类器官基质材料、个性化多功能芯片、动态微流控培养系统三大领域逐步攻克,逐步搭建起标准化、自动化的器官芯片微生理系统。
基质材料方面,逸芯生命科学团队创新性推出了国际首款可工程化应用的多功能新型类器官培养基质材料,目前已上市销售。此款国内首个新型类器官培养基质胶完全摒弃基于小鼠肿瘤提取的工艺制备基质胶,基于正常组织脱细胞工艺全新方案开发,来源广泛,成本低,源头可控,类器官培养效率高,凝胶强度高,并在实验中显示出良好的安全性及稳定性,有望解决海外基质胶垄断现状。

逸芯生命科学 国内首个新型类器官培养基质胶
与此同时,逸芯生命科学已推出自主研发的可稳定传代和高效扩增的类器官培养基套装20余种,涵盖常见肿瘤类器官以及鼻粘膜、子宫内膜、皮肤等正常组织器官模型,具有易用性高、类器官构建高效、稳定性强等优势,提供标准化的类器官培养解决方案。
器官芯片的产品化方面,逸芯生命科学基于其全流程平台研发出10余款高通量、功能化仿生的通用芯片,可实现动态和静态培养。根据客户不同应用场景及需求,可在2~3个月内高效率拓展专用芯片。此外,逸芯生命科学还聚焦鼻粘膜器官芯片、血管化器官芯片、皮肤器官芯片、肠器官芯片等体外模型的疾病领域,正在研发专用芯片。

逸芯生命科学 器官芯片解决方案
此外,逸芯生命科学正在建设基于全球首个鼻粘膜器官芯片构建药物递送开发平台、基于高通量免疫共培养器官芯片构建AI制药筛选平台等AI+器官芯片赋能平台。刘杰教授谈到,“基于高通量的器官芯片研发和产品化,我们会逐步构建起药物开发和筛选平台。在这一点上,器官芯片既会应用AI,赋能新分子的类器官干湿实验验证,未来也将反哺AI制药快速筛选药物管线的需求。在当前的AI制药赛道,整体数据体系来源于2D细胞,输入数据不精准、不完备,难以形成数据闭环。而器官芯片的高通量3D数据和干湿实验有效数据能够成为喂给AI药物筛选平台的迭代素材,未来,随着器官芯片的发展,基于3D数据的细胞形态学分析、动态数据监测、细胞间关联等病理学研究都将迎来更多突破。”
基于类器官培养基和通用器官芯片的创新,逸芯生命科学在药物开发和临床精准用药等领域可实现周期缩短5倍以上,成本降低90%。整体来看,逸芯生命科学将从器官芯片配套产品(如培养基、个性化培养试剂盒等)、器官芯片技术服务、AI+器官芯片新药发现三大解决方案入手,打造器官芯片全流程解决方案。成立不足1年,逸芯生命科学已开始实现产品商业化落地,与研发机构、药企、CRO等建立合作。
类器官培养基质材料创新的未来:3D生物打印生物墨水
提到标准化,刘杰教授认为临床专家共识与工程化上的标准化都至关重要:“通俗来说,工程标准化就是我们生物工程研发者从经验中总结的——如何能够尽可能让更少人参与到培养和制作类器官的过程中。我身边每个研发人员,培养模型过程中个体化的经验和操作习惯都会影响到最终结果,标准化和可及性就没法实现。假如我们构建一个体外类器官全流程的标准化、自动化装备或平台,这可能就会是下一个行业性的标准。”
从成立之初,逸芯生命科学就以工程化、标准化作为准则,开发自动化器官芯片工作站(集成化3D器官培养微球制备系统)也已列入研发日程之中。

逸芯生命科学 高通量水凝胶微球微球制备系统
更多的探索仍在持续。此前,刘杰教授团队首次提出将新型类器官培养基质胶(改性脱细胞细胞外基质材料)作为肿瘤类器官3D生物打印生物墨水应用,并开发高通量肿瘤类器官药物评价平台。
过往肿瘤类器官模型构建受到人工操作的制约,导致其在实验规模、结果可靠性等多个方面都面临着一定的挑战。3D生物打印技术有望取代人工操作,实现大规模、标准化、高一致性肿瘤类器官模型的构建。但现有的类器官培养材料(如Matrigel)较弱的机械性能无法满足3D生物打印的需要,而传统生物墨水(如海藻酸盐)无法为类器官提供最佳的生长环境。
实验中,新型类器官培养基质胶形成的水凝胶在流变学、力学等多方面的性能均显著优于Matrigel,其稳定性能够满足类器官长期培养的需求。利用生物墨水在低温下的可逆凝胶化特性,可以在低温平台上实现高通量、高精度、高可控性的3D生物打印,制备得到大量尺寸均一、结构完整的凝胶球体。
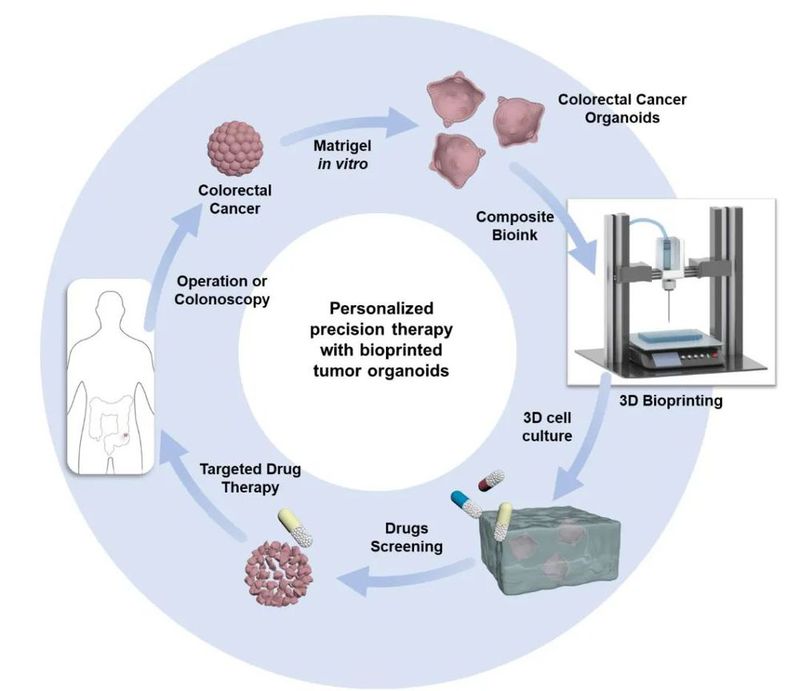
高通量结直肠癌类器官药物评价模型构建示意图
除去良好的3D生物打印性能,该生物墨水也兼具了优秀的结直肠癌类器官培养效果。刘杰教授团队将肿瘤类器官模型与高通量3D生物打印相结合,实现了高通量的结直肠癌类器官药物评价模型的构建。即使在经历3D生物打印过程后,其依然能够形成具有空间异质性的多细胞结构,这种结构与Matrigel中培养的类器官以及原始肿瘤组织相似,能够较好地反映患者肿瘤组织的空间特征。同时,其结直肠癌类器官能够表达多种结直肠癌标志性蛋白,特征精细再现有利于模拟患者对于广谱类药物、靶向药物等多种治疗药物的真实反应。
正如刘杰教授所说,结合生物材料、培养基、芯片设计创新,逸芯生命科学可以为客户、为未来的疾病研究提供更多的差异化的器官芯片模型。这将是个漫长而不断求索的过程,也是在合作中发现新机遇的共建之路。