“偶尔吃一顿好的,应该没事吧?”这是很多人在面对高脂美食时的自我安慰。
然而,来自哈佛大学的研究团队发表于Cell子刊 Immunity的一项最新研究可能要让我们重新审视这个想法了。
这项研究发现,高脂饮食通过扰乱肠道菌群,诱发炎症反应,并与3型天然淋巴细胞(ILC3)内的脂质堆积相互叠加,进一步压制其脂肪酸氧化能力,触发线粒体脂质过氧化,最终导致ILC3迅速死亡。并且,这一过程并不是肥胖“惹的祸”。
DOI:10.1016/j.immuni.2026.02.014.
ILC3减少,与肥胖无关,
与脂肪本身有关
在深入这项研究之前,我们先来了解3型天然淋巴细胞(ILC3)。它们通过分泌效应分子白介素-22(IL-22),作用于肠道上皮细胞,诱导抗菌肽的产生并增强肠道屏障功能,从而阻止有害细菌及毒素进入血液。
如果没有ILC3,肠道屏障就会像漏雨的屋顶,细菌和毒素四处渗漏,引发慢性低度炎症,这也是肥胖、糖尿病、脂肪肝甚至肠癌的温床。
既往研究提示,长期高脂饮食可能导致ILC3减少,但一直没弄明白:到底是肥胖本身“惹的祸”,还是脂肪直接对ILC3下了“毒手”? 这个“先有鸡还是先有蛋”的问题,在这项新研究中得到了清晰的解答。
研究团队使用了多种基因修饰小鼠,包括肥胖基因缺陷的ob/ob小鼠、缺乏T细胞和B细胞的Rag2敲除小鼠,以及肠道中没有微生物的无菌小鼠。
他们给小鼠喂食了猪油、棕榈油、橄榄油、葵花籽油和鱼油等多种脂肪来源的高脂饮食(60%或45%的热量来自脂肪),并设置了严格匹配的对照饮食(10%脂肪)。
研究者首先在肥胖和超重人群的肠道中观察到:ILC3的比例与身体质量指数(BMI)呈反比。也就是说,越胖的人,肠道ILC3比例越低。与
接着,他们在小鼠中观察到了类似的现象。无论小鼠是先天肥胖(ob/ob)还是后天饮食诱导的肥胖,喂高脂饮食,它们ILC3比例就会显著降低。
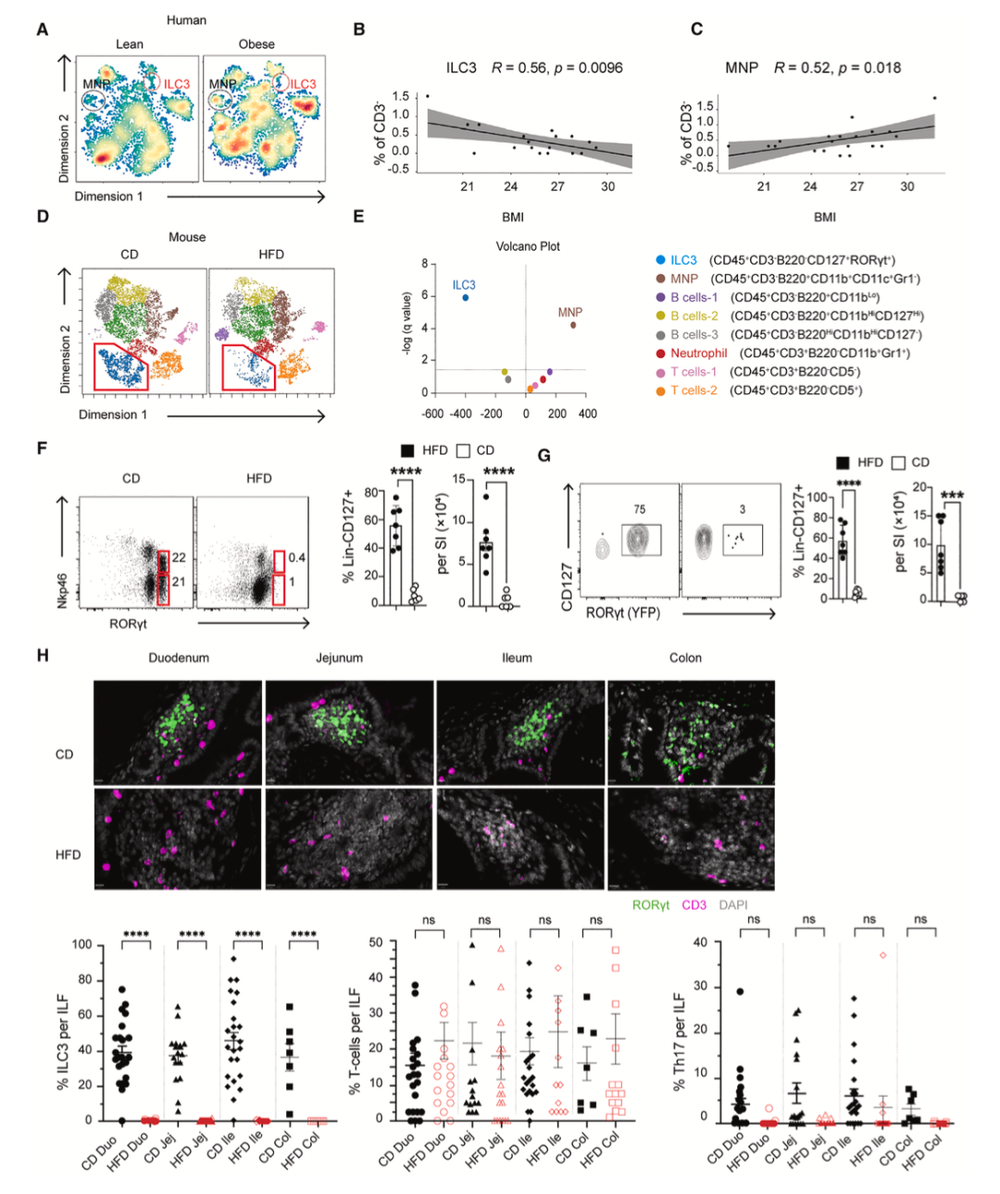
肥胖人群与小鼠的肠道ILC3数量显著减少
为了排除“吃得多”和“长胖”这两个因素的干扰,研究者还进行了配对喂养,他们让高脂饮食组的小鼠每天摄入的总热量与对照组完全一致,结果这组小鼠的体重并没有增加,但ILC3的数量照样减少了。
随后,他们用脂肪吸收抑制剂Orlistat来阻止脂肪吸收,结果发现:阻断脂肪吸收后,即使摄入高脂饮食,ILC3也能被保护下来。
这也意味着,是高脂饮食中的脂肪本身,而不是肥胖或热量过剩,导致了ILC3的死亡。
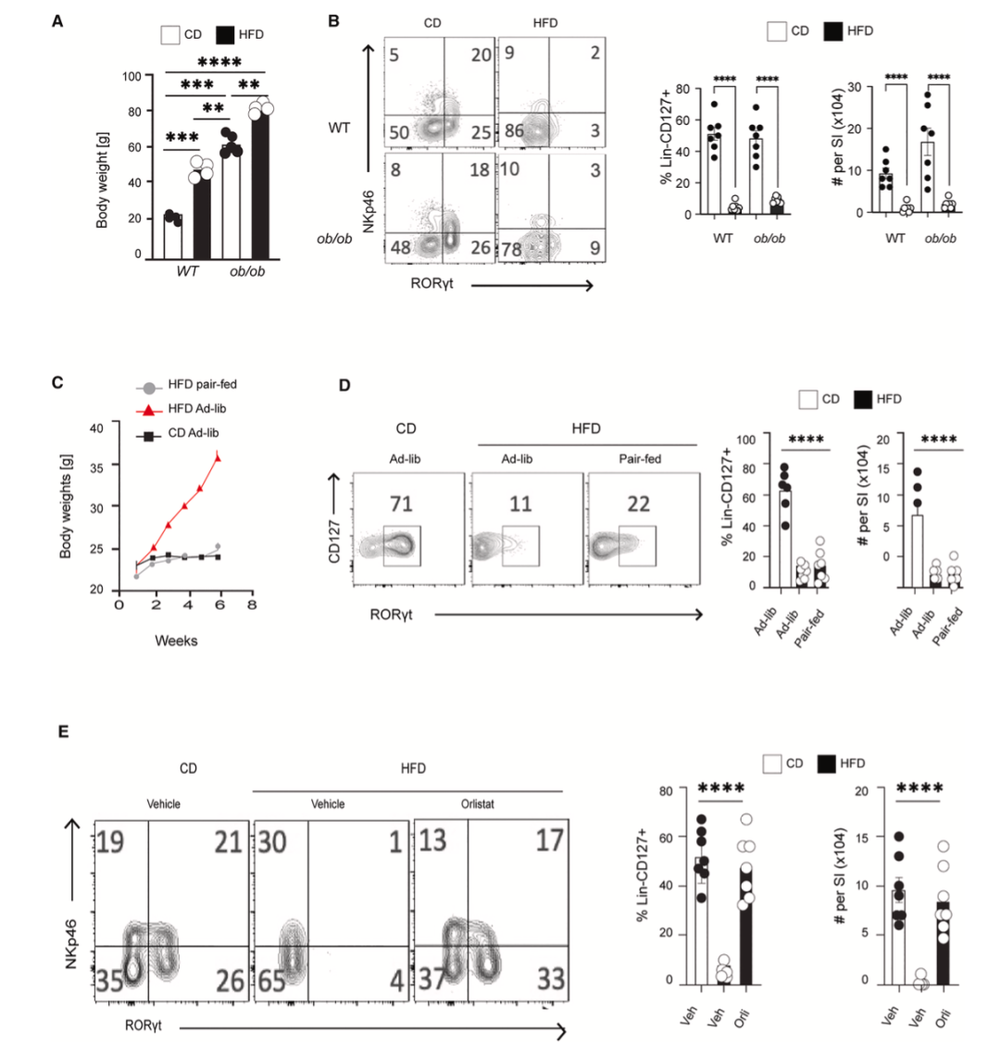
高脂饮食的吸收过程而非肥胖本身,导致肠道ILC3减少
只需24小时,
ILC3就开始死亡
在传统认知中,只有长期吃得油腻才会伤身。然而,研究者在小鼠摄入高脂饮食后的24小时时就检测到血液中细菌产物(PRR配体)水平显著升高,ILC3死亡的比例和数量开始显著增加,但此时它们的血糖耐受性还是正常的。
不过,短短1周后,所有肠段(十二指肠、空肠、回肠、结肠)的ILC3数量都大幅减少;到第4周,基本完全消失。
这意味着,一次放纵大餐,可能就足以让肠道免疫防线出现缺口。
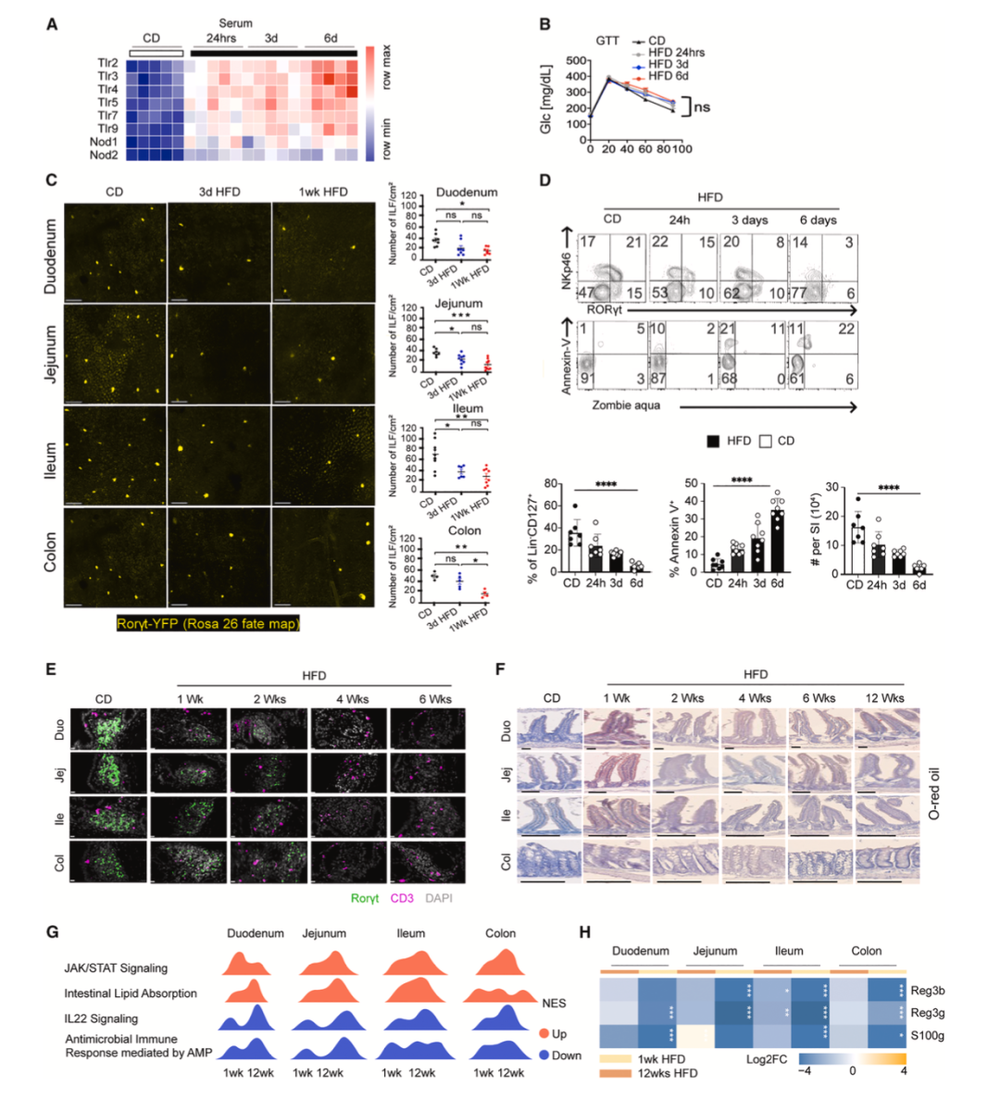
高脂饮食诱导 ILC3 细胞死亡,早期破坏肠道免疫屏障
那么,高脂饮食究竟是怎么杀死ILC3的呢?研究者揭开了其中的分子机制,可以用“两击模型”来概括。
第一击:ILC3大量吞噬脂肪,变成“胖子细胞”
ILC3比其他免疫细胞(T细胞、B细胞)更爱“吃油”。在摄入高脂饮食的小鼠肠道中,ILC3内部充满了脂滴。不过,仅仅有脂质堆积,并不会杀死ILC3。在无菌小鼠中,即使摄入高脂饮食,ILC3也能安然无恙地活着,尽管它们体内同样积累了大量脂肪。这说明:脂肪要“兴风作浪”,还需另一个信号的“助攻”。
第二击:菌群驱动的炎症,抑制了脂肪酸氧化
当高脂饮食破坏肠道屏障后,细菌产物(如脂多糖LPS、肽聚糖PGN)渗漏到肠壁,激活了单核吞噬细胞,这些细胞大量释放促炎因子(IL-1β、IL-23、TNF-α)。炎症信号又作用于ILC3,抑制了脂肪酸氧化(FAO)通路。
正常情况下,ILC3可以通过FAO把脂滴中的脂肪酸氧化分解掉。但当FAO被抑制后,脂质堆积在线粒体周围,在炎症刺激下产生大量的脂质过氧化物,导致线粒体膜完整性丧失,ILC3走向凋亡。
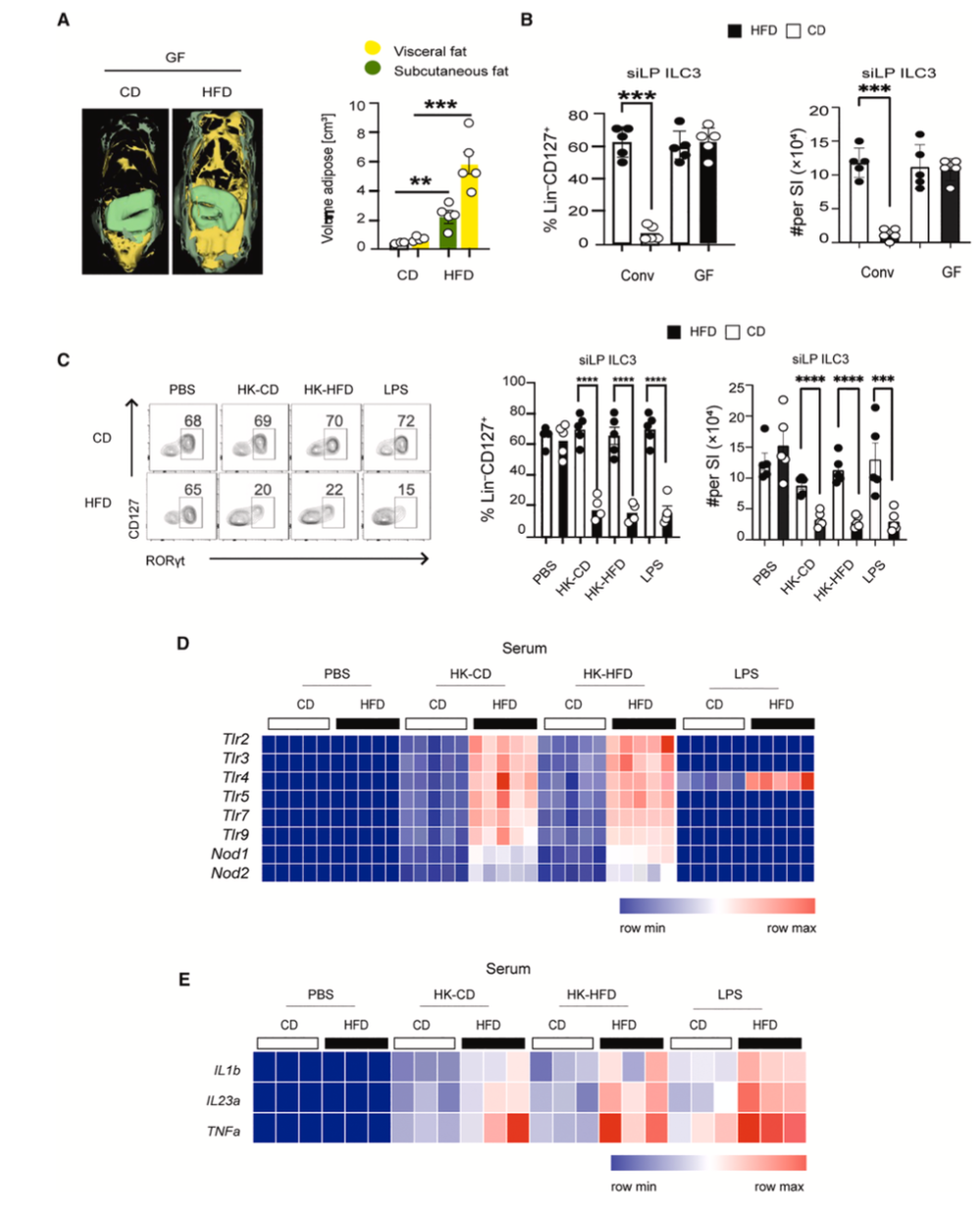
高脂饮食诱导的 ILC3 耗竭,依赖于肠道菌群介导的炎症
这个过程是可逆的,但需要时间
不过,ILC3的减少并非永久性损伤。研究者将已经吃了8周高脂饮食的小鼠换回普通饮食,然后观察ILC3的恢复情况。
他们发现:换回普通饮食3天后,ILC3数量开始慢慢回升;到第6天,进一步增加;到第6周,ILC3逐渐恢复到接近正常水平。
可见,如果长期高脂饮食后决定“洗心革面”,肠道免疫还能重建,但需要耐心。
当然,这项研究也有其局限性。研究用的是纯化高脂饲料,与真实世界中混杂了碳水、蛋白和纤维的人类饮食有一定差距。
但总体而言,这项研究提示,高脂饮食对肠道免疫的打击在24小时内就开始发生,而且与体重无关。即使是个瘦子,一顿高脂大餐也可能让肠道ILC3大量“阵亡”,削弱对病原菌的防御能力。
如果已经吃了几天油腻,也不能指望下一顿吃素就能立刻“补救”。ILC3的再生需要数周的正常饮食。
[1]Torrico EC, Kaptein P, Laalouhmi F, Mitsialis V, El Guendouzi S, El Khayari A, et al. High-fat diet causes rapid loss of intestinal group 3 innate lymphoid cells through microbiota-driven inflammation and mitochondrial stress. Immunity. 2026 Apr 14;59(4):1–18. https://doi.org/10.1016/j.immuni.2026.02.014.
