癌症相关成纤维细胞(CAFs)在肿瘤微环境中扮演着关键角色,通过重塑细胞外基质、分泌细胞因子和抑制免疫反应来促进肿瘤生长和转移。然而,针对CAFs的治疗策略仍然有限。烟酰胺N-甲基转移酶(NNMT)是一种代谢调节酶,能够通过消耗SAM(S-腺苷甲硫氨酸)中的甲基,导致DNA、RNA和组蛋白甲基化减少,从而引发表观遗传变化。NNMT在多种癌症中的表达增加与不良预后相关,但其在CAFs中的作用机制尚不清楚。
近日,Nature期刊上公布了一篇名为“NNMT inhibition in cancer-associated fibroblasts restores antitumour immunity”的文章,通过空间转录组学和单细胞RNA测序技术,揭示了NNMT在高级别浆液性卵巢癌(HGSOC)中的作用机制,并开发了一种有效的NNMT抑制剂,能够减少肿瘤负担和转移,并增强免疫检查点阻断疗法的疗效。这些发现不仅为理解CAFs在肿瘤免疫微环境中的作用提供了新的视角,还为开发针对CAFs的新型癌症治疗策略提供了理论基础。

文章标题
该文章的研究团队来自于芝加哥大学,通讯作者恩斯特·兰格尔(Ernst Lengyel)博士说:“大多数疗法都集中在癌细胞上,但我们对周围基质中的成纤维细胞感兴趣。这些细胞不像癌细胞那样发生突变,这使它们更加稳定,我们认为也更具可靶向性,我们已经确定了CAFs激活背后的机制,并找到了一种可以阻止它的药物。”

高级别浆液性卵巢癌是卵巢癌中最常见且最致命的形式。它通常在晚期才被诊断出来,治疗难度极大。尽管手术和化疗最初能带来显著益处,但癌症经常复发,导致生存率很低。免疫疗法是许多癌症的突破性治疗方法,但在卵巢癌中却未能奏效,主要原因是周围细胞的活性被肿瘤编程以抑制免疫反应。这些细胞被称为癌症相关成纤维细胞(CAFs),与在支持组织完整性和促进伤口愈合中发挥重要作用的正常成纤维细胞不同。相反,CAFs包围肿瘤,提供保护,并释放削弱免疫反应和促进转移的信号。
NNMT这种代谢酶在CAFs中高度表达,并通过改变表观遗传和代谢编程,将正常成纤维细胞转化为促肿瘤成纤维细胞。芝加哥大学的研究团队发现,表达NNMT的CAFs分泌补体蛋白,这些蛋白将单核细胞(一种白细胞)转化为髓系衍生的抑制细胞(MDSCs)。该研究的第一作者表示“酶NNMT在成纤维细胞中引发广泛的表观遗传变化,促进肿瘤生长。抑制NNMT有可能逆转这些变化,减少成纤维细胞的肿瘤支持作用”。
为了将这些发现转化为治疗方法,研究团队筛选了超过15万种化合物后,发现了一种高度靶向的NNMT抑制剂。在卵巢癌的临床前动物模型中,NNMT抑制剂减少了肿瘤负担并恢复了免疫活性。更重要的是,当与免疫检查点抑制剂联合使用时,它能显著抑制肿瘤生长。这项研究表明,通过NNMT抑制靶向CAFs,可以克服疾病进展和治疗耐药性中的关键障碍,即使不直接作用于癌细胞,也能有效控制肿瘤生长。
基础实验小课堂
酶联免疫吸附测定(ELISA)
ELISA广泛应用于生物医学研究和临床诊断中,用于检测各种蛋白质,如细胞因子、抗体、激素等。在该研究中,ELISA被用来检测肿瘤组织中C3蛋白的浓度,以评估NNMT对C3蛋白分泌的影响。研究人员从Nnmt+/+(n = 8)和Nnmt−/−(n = 6)小鼠中提取的MC38肿瘤在皮下(s.c.)注射癌细胞后12天被匀浆化,使用酶联免疫吸附测定(ELISA)检测C3蛋白水平。
实验流程
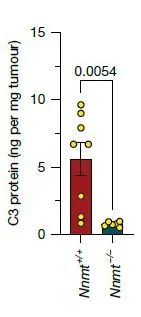
在Nnmt+/+小鼠的肿瘤组织中,C3蛋白水平显著高于Nnmt−/−小鼠的肿瘤组织。(Nnmt+/+小鼠肿瘤组织中C3蛋白的浓度为5 ng/mg肿瘤组织,而Nnmt−/−小鼠肿瘤组织中C3蛋白的浓度为1 ng/mg肿瘤组织。)
NNMT的表达显著增加了肿瘤组织中C3蛋白的水平。这表明NNMT在CAFs中的表达不仅改变了CAFs自身的表型,还通过分泌C3蛋白等补体因子,影响了肿瘤微环境中的免疫细胞组成和功能。C3蛋白是补体系统的重要组成部分,参与免疫反应的调节。在肿瘤微环境中,C3蛋白的增加可能有助于招募免疫抑制细胞(如MDSCs),从而抑制抗肿瘤免疫反应。
通过抑制NNMT的活性,可以减少C3蛋白的分泌,从而削弱肿瘤微环境中的免疫抑制作用,增强抗肿瘤免疫反应。这为开发新的癌症治疗策略提供了理论依据。
该实验结果支持NNMT作为癌症治疗的潜在靶点。通过抑制NNMT的活性,可以减少C3蛋白的分泌,从而改善肿瘤微环境中的免疫反应,增强免疫治疗的效果。这一发现为靶向NNMT的癌症治疗策略提供了重要的实验依据。
实验中使用到的实验试剂:

产品链接:
https://www.abcam.cn/products/elisa-kits/mouse-complement-c3-elisa-kit-ab157711.html
研究方法与结果
NNMT在CAFs中的上调与HGSOC中CD8+T细胞活性降低相关
首先,研究人员通过空间转录组学技术分析了30名化疗初治的HGSOC患者的55个组织样本,包括原发性卵巢肿瘤、癌旁卵巢基质和网膜转移样本,并利用单细胞RNA测序(scRNA-seq)分析了7名患者的化疗初治网膜转移样本,验证NNMT在CAFs中的表达并定义CAFs亚群。
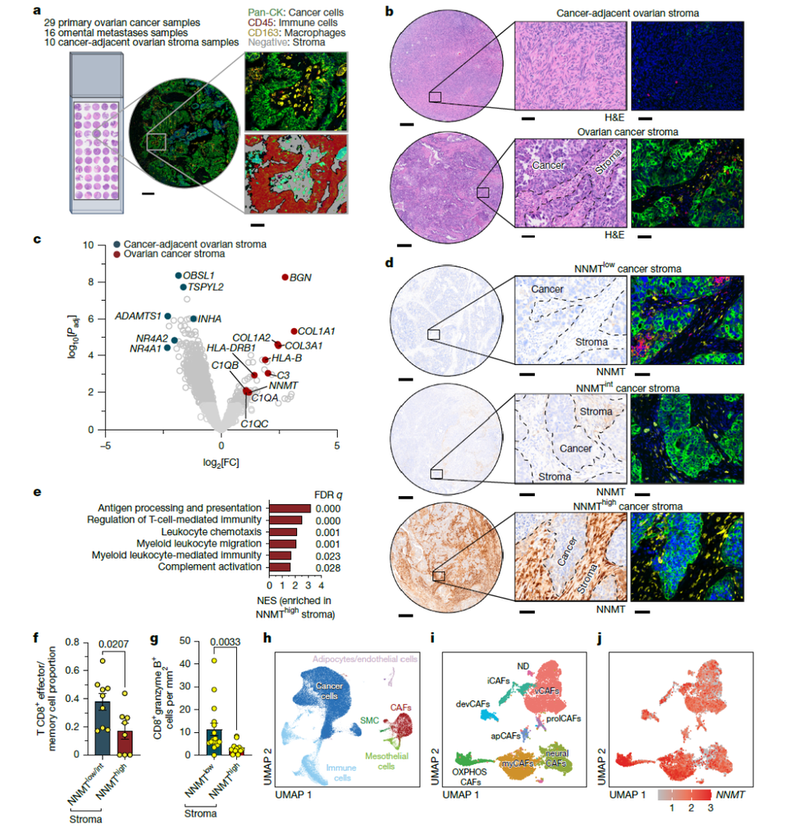
结果表明,NNMT在所有CAFs亚型中均有表达,且其表达水平从癌旁卵巢基质到卵巢肿瘤基质再到网膜转移基质逐渐增加。此外,NNMT高表达的肿瘤基质中效应/记忆CD8+T细胞的比例较低,表明NNMT的高表达与CD8+T细胞活性的降低相关。基因集富集分析(GSEA)进一步揭示了NNMT高表达的肿瘤基质中与免疫功能相关的通路显著上调。
基质Nnmt基因敲除减少肿瘤负担
接下来,研究人员利用CRISPR技术在C57BL/6背景的小鼠中敲除了Nnmt基因,构建了Nnmt−/−小鼠模型,并在这些小鼠中通过向卵巢内注射HGS-2卵巢癌细胞、腹腔内注射ID8卵巢癌细胞、乳腺脂肪垫内注射E0771-LMB乳腺癌细胞和皮下注射MC38结肠癌细胞,观察肿瘤生长和转移情况。
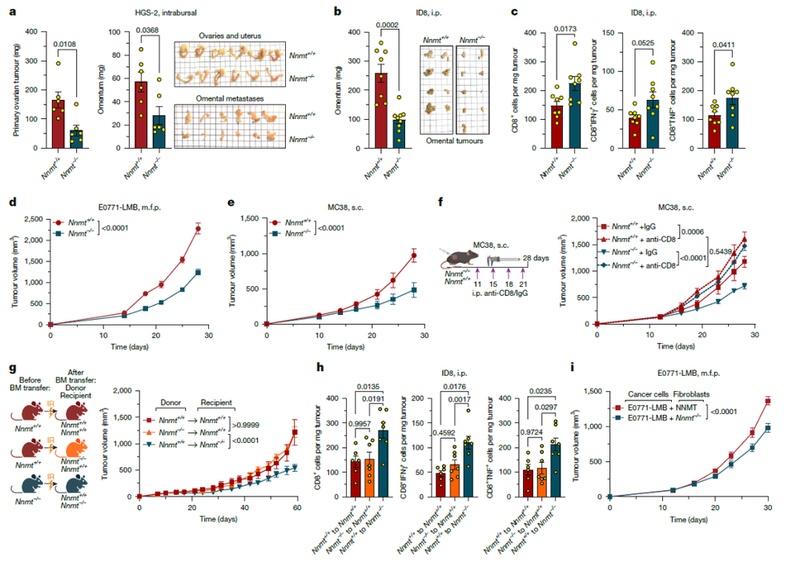
结果发现,Nnmt−/−小鼠在多种肿瘤模型中表现出较小的肿瘤生长和转移,这与CD8+T细胞活性增强有关。流式细胞术分析显示,Nnmt−/−小鼠的肿瘤中CD8+T细胞数量增加,且这些T细胞的IFNγ和TNF产生能力增强。此外,通过骨髓嵌合实验,证实了Nnmt在非免疫细胞(如基质细胞)中的作用对肿瘤生长的影响。
表达NNMT的成纤维细胞通过补体分泌招募免疫抑制性单核细胞
随后,研究人员在NIH-3T3成纤维细胞中过表达NNMT(3T3-NNMT),通过RNA-seq分析其基因表达变化,并使用Transwell实验评估3T3-NNMT条件培养基对骨髓细胞迁移的影响。
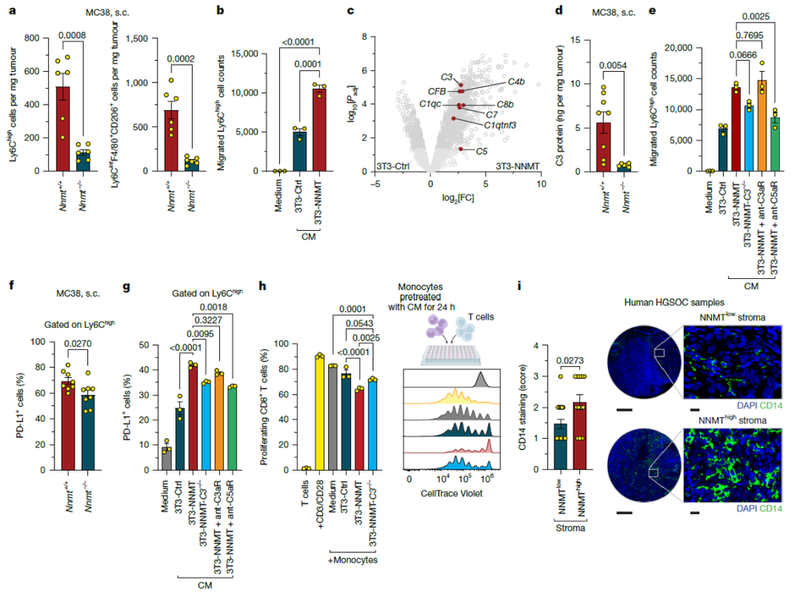
蛋白质组学分析显示3T3-NNMT条件培养基中的补体因子表达增加。在Nnmt−/−和Nnmt+/+小鼠的肿瘤中,研究人员检测了C3蛋白水平和PD-L1表达。结果表明,3T3-NNMT细胞中与髓系细胞迁移、活性和补体激活相关的通路显著富集,且3T3-NNMT条件培养基能够吸引Ly6Chigh单核细胞和单核细胞衍生的肿瘤相关巨噬细胞。通过CRISPR技术敲除3T3-NNMT细胞中的C3基因,显著减少了单核细胞的迁移。在Nnmt+/+小鼠的肿瘤中,Ly6Chigh单核细胞表达高水平的C5aR,且与PD-L1表达相关。
NNMT介导的组蛋白低甲基化诱导CAFs表型
接着,研究人员在低甲硫氨酸培养基中培养3T3-NNMT和3T3-CTRL细胞,检测H3K27me3水平,并通过RNA-seq分析其基因表达差异。ChIP-seq分析揭示了NNMT表达对组蛋白甲基化的影响。用流式细胞术检测了NNMT表达对细胞大小的影响。
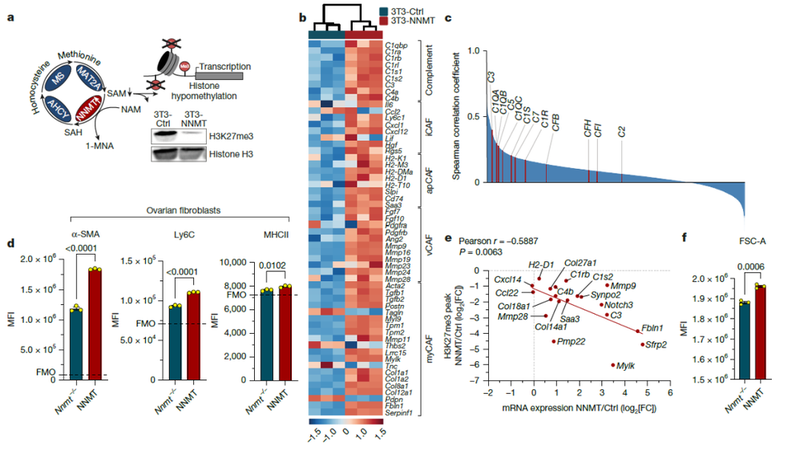
结果表明,NNMT表达导致H3K27me3水平降低,促进补体因子和CAFs相关基因的表达。在NNMT表达的CAFs中,与主要CAFs亚型相关的标记基因表达增加。ChIP-seq分析发现,NNMT表达导致H3K27me3峰大小显著减小,多个肿瘤支持性CAFs基因表达增加。此外,NNMT表达的CAFs细胞大小增加,与CAFs的表型变化一致。
开发一种有效的NNMT抑制剂,减少肿瘤负担,限制MDSC浸润,并增强免疫检查点阻断疗法的疗效
最后,研究人员通过高通量筛选,从152,778个小分子中筛选出361个高质量活性分子,并进一步优化得到了一个有效的NNMT抑制剂(NNMTi)。在体外和体内实验中,评估了NNMTi对CAFs功能和肿瘤生长的影响,并在多种肿瘤模型中测试了NNMTi的疗效,包括与免疫检查点抑制剂(如抗PD-1和抗CD47)联合使用的效果。
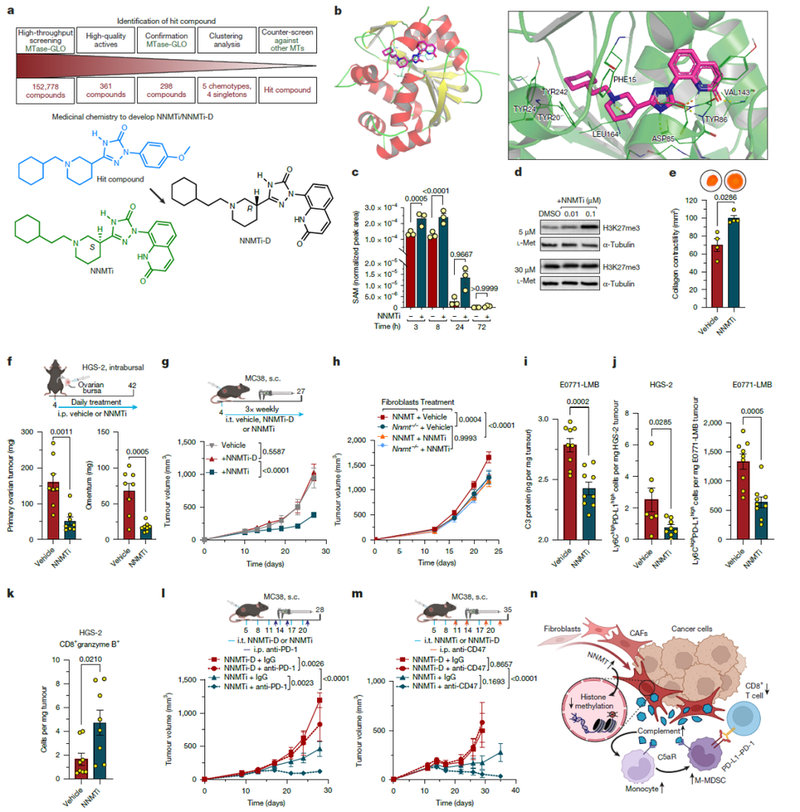
结果表明,NNMTi能够显著减少肿瘤负担和转移,通过减少CAF介导的MDSCs招募和重新激活CD8+T细胞活性来增强免疫检查点阻断疗法的疗效。在多种肿瘤模型中,NNMTi单药治疗显著减少了肿瘤生长,并且与免疫检查点抑制剂联合使用时表现出协同效应。NNMTi处理的肿瘤中,CAFs的数量和大小减少,C3蛋白水平降低,免疫抑制性单核细胞减少,CD8+T细胞活性增强。
结语
综上所述,该研究的主要结论总结如下:
NNMT是CAFs的一个核心调节因子,通过分泌补体因子招募MDSCs,从而抑制CD8+T细胞活性,促进肿瘤生长和转移。
NNMTi作为一种有效的抑制剂,能够减少肿瘤负担和转移,并增强免疫检查点阻断疗法的疗效,显示出作为癌症治疗靶点的潜力。
该研究不仅揭示了NNMT在CAFs中的作用机制,还为开发针对CAFs的新型癌症治疗策略提供了理论基础。
这项研究为理解CAFs在肿瘤免疫微环境中的作用提供了新的视角,并为开发针对CAFs的新型癌症治疗策略提供了有力的证据。通过靶向NNMT,可以调节肿瘤微环境,增强免疫治疗的效果,这对于提高癌症患者的治疗效果和生存率具有重要意义。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。