2024年6月26日,美国FDA批准Verona(VRNA)公司的Ohtuvayre (ensifentrine)上市,作为维持疗法治疗慢性阻塞性肺病(COPD)成人患者。Verona新闻稿指出,该药是COPD治疗领域近20年以来首个获批上市的新机制吸入制剂。
2024年7月3日,赛诺菲针对COPD的新药Dupixent (度普利尤单抗)获欧洲药品管理局(EMA)批准作为以血嗜酸性粒细胞水平升高为特征的不受控制的慢性阻塞性肺病(COPD)患者的附加维持治疗,成为COPD治疗领域的首个获批生物制剂。
短短几天,COPD治疗领域就将迎来重塑,这一严重呼吸系统疾病的治疗格局或许有望在今年发生变革。
COPD 患者盼新药
慢性阻塞性肺疾病(COPD),简称慢阻肺。据慢性阻塞性肺疾病全球倡议(GOLD)2024 版,COPD 是常见、可防可治的异质性疾病,多因长期接触有毒颗粒或气体,致气道和(或)肺泡异常,受宿主因素影响,以气流受限、持续呼吸道症状为特征。
世界卫生组织统计显示,COPD 已成为人类第三大死因,约 11% 的人死于该病。未来 40 年,COPD 患病率预计持续上升,到 2060 年,每年或超 540 万人因 COPD 及相关疾病死亡。2018 年,王辰院士在《The Lancet》发表的研究表明,我国近 1 亿人患 COPD,40 岁以上成人患病率达 13.7%。
GOLD 2024 推荐的 COPD 治疗和预防药物,主要有吸入性糖皮质激素、支气管扩张剂、磷酸二酯酶 - 4 抑制剂、抗生素、疫苗、黏液溶解剂及抗氧化剂 。
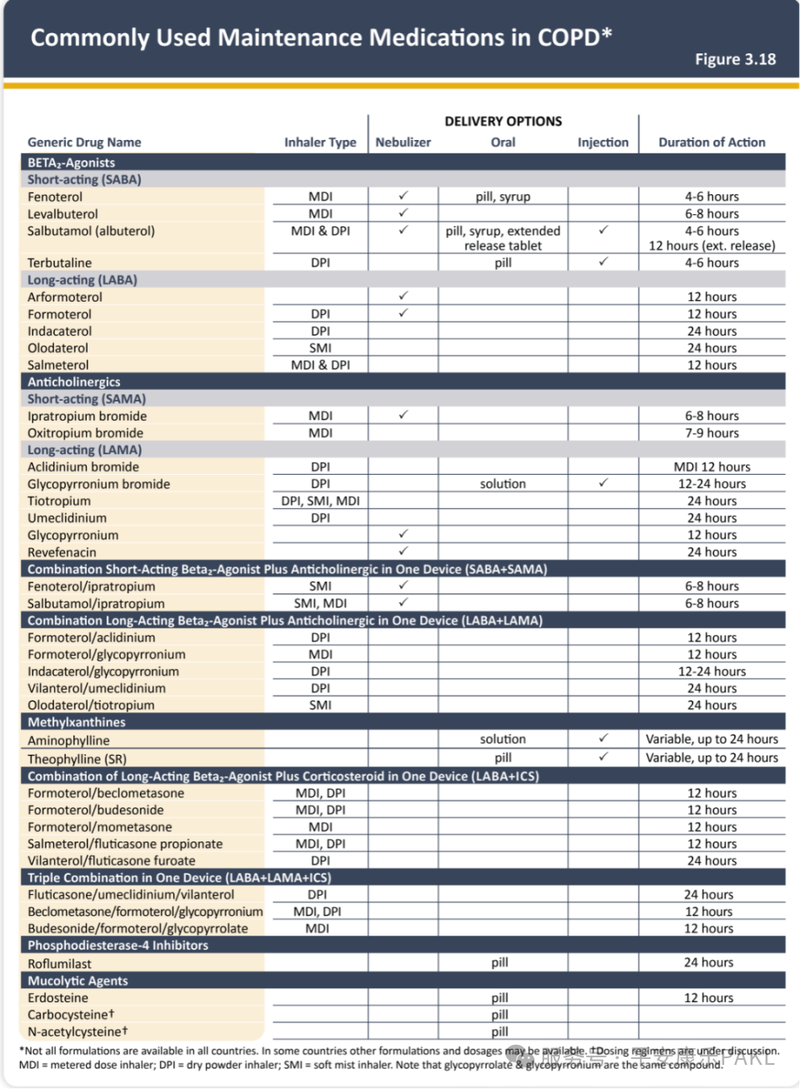
图1. COPD常见维持用药(来源:GOLD 2024指南)
然而,现有药物虽能显著改善 COPD 患者症状,却难以有效预防 COPD 急性加重。临床上,接受三联方案治疗的慢阻肺病患者,仍有 30% - 40% 会出现中度或重度急性加重。
COPD 发病机制复杂且尚未完全明晰,致使临床上极度缺乏对因治疗药物。该领域已有十余年未推出新药,COPD 患者急需新药。
两款新药,有望重塑 COPD 治疗格局
好消息传来,2024 年 6 月,美国 FDA 批准 Ensifentrine 上市,这是二十年来首个 COPD 新机制吸入剂。紧接着,再生元 / 赛诺菲的生物制剂 Dupilumab 在欧洲获批,为 COPD 患者开辟了新的用药路径 。
Ensifentrine:COPD 新机制首秀药物
Ensifentrine 由 Verona 公司研发,是一种小分子选择性磷酸二酯酶双抑制剂(PDE3/4)。PDE3/4 在支气管平滑肌大量表达,Ensifentrine 通过抑制 PDE3/4,提高支气管内 cAMP 水平,从而发挥支气管舒张与抗炎双重功效。2024 年 6 月,该药获批用于 COPD 成人患者维持治疗,商品名 Ohtuvayre 。
2024年初,它被行业媒体 Evaluate 列为 2024 年最有希望获批的 10 款重磅疗法之一,是 20 多年来首个用于 COPD 维持治疗的新机制吸入式疗法。
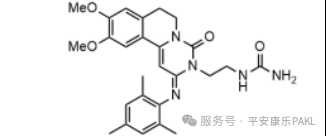 图2. Ensifentrine结构式
图2. Ensifentrine结构式
FDA此次批准基于ENHANCE-1和ENHANCE-2两项Ⅲ期临床研究数据。ENHANCE-1和ENHANCE-2都是随机、双盲、安慰剂对照的Ⅲ期研究,分别入组760和790名COPD成年患者。相较于安慰剂,Ensifentrine可以显著改善0-12小时内1秒钟平均用力呼吸曲线下面积(FEV1 AUC 0-12hr)。
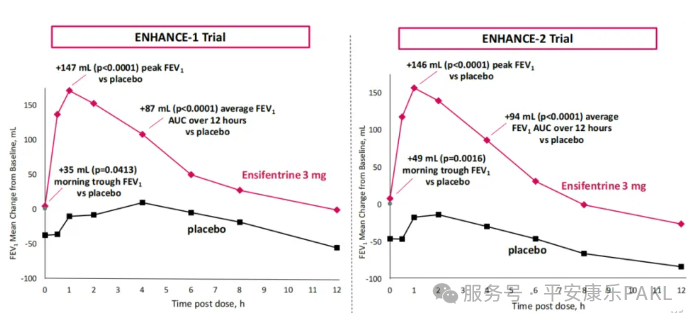
安全性方面,患者对Ensifentrine耐受良好,最常见的不良反应是鼻咽炎、高血压和背疼。
值得一提的是,2021年6月,Verona公司授予优锐医药在大中华区临床开发和商业化ensifentrine的独家权利。2023年2月,优锐医药启动了Ensifentrine治疗COPD的中国Ⅲ期临床试验,该药或将很快惠及国内COPD患者。
Dupilumab:首个获批用于 COPD 的生物制剂
再生元 / 赛诺菲的 Dupilumab(达必妥,IL - 4/13 单抗),继 Ensifentrine 后,也在 COPD 治疗领域取得突破。2024 年 7 月 3 日,赛诺菲与再生元宣布,Dupilumab(商品名:Dupixent)获欧洲药品管理局(EMA)批准,用于血嗜酸性粒细胞水平升高、病情不受控的 COPD 患者的附加维持治疗 。同年 2 月,美国 FDA 受理其治疗 COPD 的补充生物制品许可申请(sBLA),并给予优先审评,预计今年晚些时候出结果。目前,该药在中国也已提交上市申请,获 CDE 受理,后续有望获批。
2024年5月20日,赛诺菲公布了达必妥治疗COPD的NOTUS Ⅲ期研究最新数据,其治疗组中伴有2型炎症特征(血嗜酸性粒细胞≥300/μl)的COPD患者急性加重年化率显著降低34%,且肺功能获得显著改善(此次度普利尤单抗EMA获批,也正是基于上述研究的积极结果),具体如下:
主要终点:治疗52周中重度慢阻肺病急性加重年化率降低34% (p<0.001)。
次要终点:第12周时,肺功能较基线改善超过两倍(139mL vs. 57mL;p<0.001),并且该改善在第52周时得以维持(115mL vs. 54mL;p=0.018)。
次要终点:第52周时,健康相关生活质量评分在数值上较基线改善更明显。
次要终点:第52周时,呼吸道症状的严重程度在数值上降低较基线更为明显。
长期以来,因 COPD 具有异质性,多数针对它的生物制剂研发失败。而度普利尤单抗(Dupilumab)获批,极大提振了该领域研发信心。
赛诺菲从 2 型炎症找到突破点。最新研究表明,20%-40% 的 COPD 患者属于嗜酸性粒细胞水平升高的 2 型炎症型。Dupilumab 作为靶向 IL-4 受体 α(IL-4Rα)的单克隆抗体,能阻断 IL-4/13 与受体复合物结合,抑制 IL-4/13 介导的 2 型炎症反应。
Dupilumab 此前已获批哮喘等多个自身免疫领域适应症,2023 年销售额超 100 亿美元,占赛诺菲整体收入四分之一。凭借 2 型炎症这一突破口,赛诺菲在免疫管线布局上更具优势。
在研药物
MNC、国内药企竞逐COPD赛道
Ensifentrine和Dupilumab通过不同机制有望给不同COPD患者带来新的治疗方案。
此外,COPD领域还有多个小分子和生物制剂已进入临床后期阶段。
表1. COPD领域在研新药(部分)
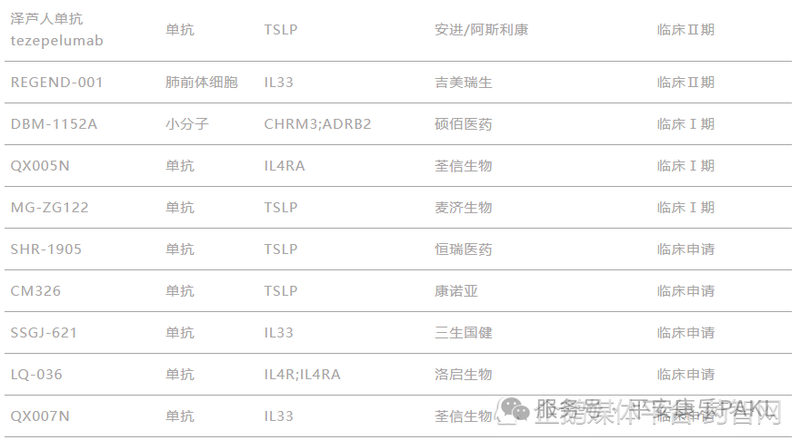
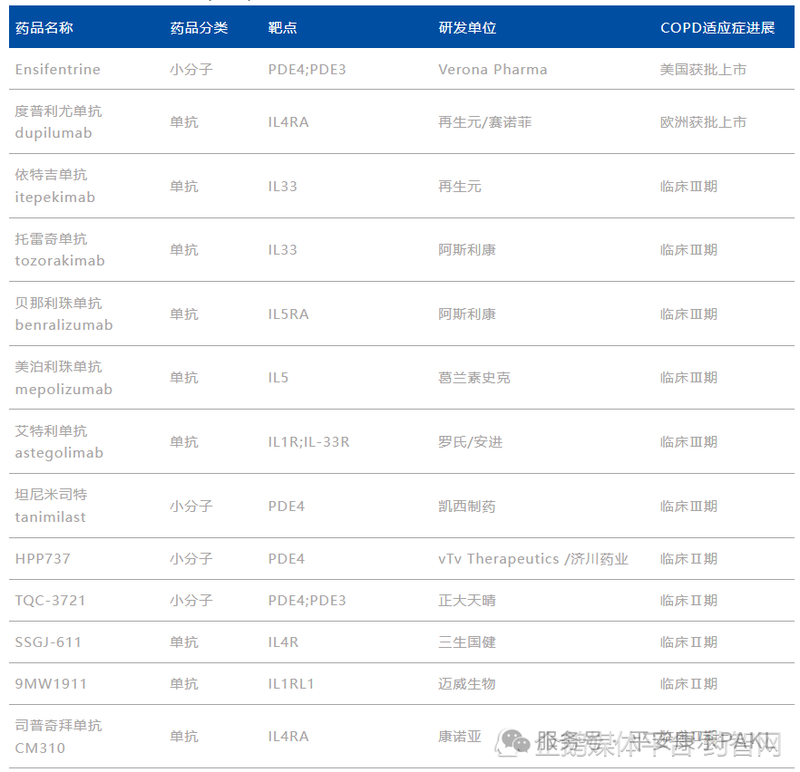
从 COPD 领域在研新药制剂类型看,正加速从小分子药物向生物药转变。生物制剂能精准作用特定炎症通路、阻断免疫关键环节,吸引众多药企布局。
靶向 IL-4、IL-5、IL-33 等介导 2 型炎症的单抗是 COPD 热门治疗机制,占全球临床后期在研项目一半以上。其中,再生元的 Dupilumab 已获批,mepolizumab 等 5 个新药处 Ⅲ 期临床。COPD 领域或迎来治疗范式变革,Dupilumab 有望抢占较大市场份额。
国内众多药企也在布局 COPD 赛道,多个新药进入临床。正大天晴的 TQC - 3721(PDE3/4 抑制剂)已进入临床 Ⅱ 期,三生国健的 SSGJ - 611(抗 IL - 4Rα 单克隆抗体)于 2023 年 9 月获批开展 Ⅱ 期临床试验。康诺亚的 IL - 4Rα 单抗司普奇拜单抗(CM310)、吉美瑞生的肺前体细胞 REGEND001 等进展也较快。
但全球 COPD 在研新药竞争中,MNC 药企临床进度普遍领先国内。临床 Ⅱ 期以上的 8 款药物均来自海外药企,国内药企短期内赶超难度较大。
结语
COPD患者的治疗背景复杂,发育情况、吸烟史、生物标志物水平等的不同也带来了治疗效果的不同,对于COPD患者急性加重的治疗,传统的药物往往效果不佳。此次Ensifentrine与Dupixent的获批为COPD的治疗带来了新的选择。
后续,COPD治疗格局或许也会因这两款新药,而发生巨大重构,请拭目以待。
