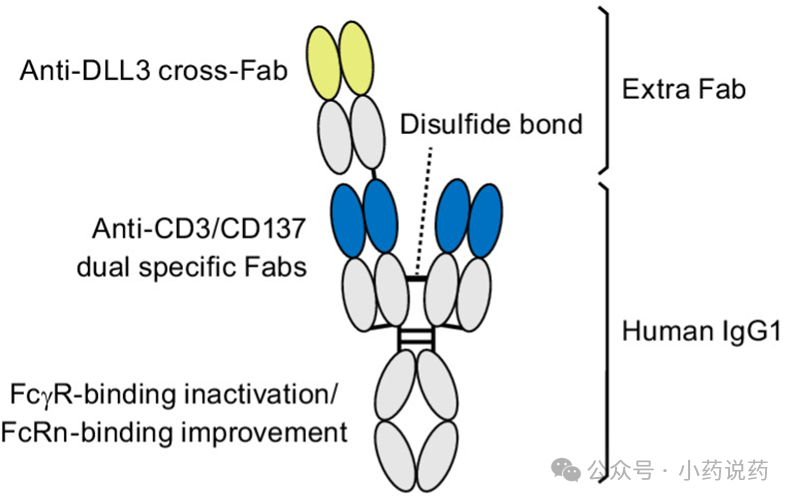
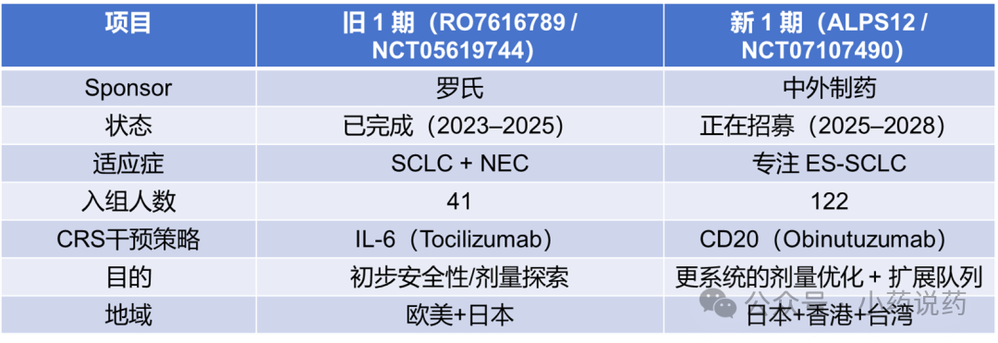
2024年5月,安进CD3/DLL3 TCE Tarlatamab(AMG757)获FDA加速批准用于治疗成人广泛期小细胞肺癌(ES‑SCLC)。ES‑SCLC 是肺癌中最凶险的类型,Tarlatamab获批是SCLC领域30年来最重要的突破之一。DLL3曾被认为是“难以成药”的肿瘤特异性靶点,Tarlatamab的成功证明DLL3可以被安全有效的靶向,DLL3 TCE能在实体瘤中发挥强效免疫杀伤,DLL3是SCLC的核心依赖通路之一。尽管Tarlatamab在临床上取得了突破,但其仍有提升空间:1)ORR ~40%,而DLL3阳性率约80–90%,说明还有一半患者没被真正“撬动”,中位PFS 4.x 个月,很多人是“短暂反应+快速进展”;2)部分患者DoR不长,免疫记忆不够,可能与T细胞耗竭有关;3)CRS/ICANS仍令人担忧,需要住院治疗、严密监测,对社区医院不友好。然而,罗氏至今没有公布其临床1期试验结果,也没有启动临床2期研究。值得注意的是,2025年10月,中外制药启动了一项针对RG6524的新临床1期研究(NCT07107490)。通过比较clinicaltrials.gov官网公布的两项临床研究的细节(表1),不难推测出罗氏已对RG6524的研发策略做出了重大调整。原临床1期的发起者(Sponsor)是罗氏,而新临床1期的发起者是中外制药。此外,原临床1期在全球17个Sites(主要集中在欧美)进行,而新临床1期则在包括4个日本Sites+香港、台湾各1个Site的6个东亚Sites进行。这些细节暗示,该项目已从一个由罗氏主导的全球重点项目降级为由罗氏旗下中外制药主导的区域性项目。在临床设计方面,适应症由SCLC+NEC变为专注于ES-SCLC。SCLC及NEC两者都属于高等级神经内分泌肿瘤,但来源部位不同,基因特征也不同。但两者都高表达DLL3,便于扩大入组、快速验证机制。尽管Tarlatamab已在ES‑SCLC(约占SCLC的70%)取得突破,但至今尚未在局限期SCLC(LS‑SCLC)及DLL3高表达的其它神经内分泌肿瘤(NEC)取得充分临床验证。因此,推测RG6524没有在已完成的临床1期研究中获得足够的药效(及安全性)验证,更没有获得RP2D(推荐2期剂量)。而ES‑SCLC属于肿瘤负荷高、病情凶险、CRS风险极高的人群,携带4-1BB共刺激信号的RG6524属于高风险免疫激活类药物。
因此,中外制药将CRS处理策略由Tocilizumab(IL-6)变为Obinutuzumab(CD20)。
RG6524遭遇ES‑SCLC细胞后,会强烈激活T细胞,导致大量细胞因子释放、肿瘤快速裂解、免疫系统急剧放大。而B细胞是重要的抗原呈递细胞(APC),会进一步放大T细胞激活。Obinutuzumab通过清除外周B细胞,可以降低APC数量、减弱T细胞初始激活强度,从而降低CRS的“起点”。
而Tocilizumab通常在CRS已经发生时,通过阻断IL‑6受体快速降低炎症反应引起的发热、低血压、肺水肿等症状,同时不影响T细胞杀伤。
因此,Obinutuzumab是“预防CRS的免疫调节器”,而Tocilizumab是“治疗CRS的急救药”。
这种CRS处理策略的转变也从另一个角度暗示,RG6524在已完成的临床1期中出现了令人担忧的CRS毒性。
2025年1月,罗氏以8000万美元首付款、总额超10亿美元的价格从信达引进刚刚进入临床1期的DLL3-ADC(IBI3009)。如果从时间线上回溯(图1),我们也许更能理解罗氏当时的策略:2024年下半年,罗氏可能已经发现RG6524的临床表现(药效and/or毒理)不及预期,公司需要引进一款药物填补其空白,而其自有的Tecentriq(PD-L1)+ DLL3-ADC治疗SCLC无疑是一个更具成功可能性的方案。而RG6524的早期研发团队(中外制药)可能对罗氏的原临床1期方案有所质疑,不甘心放弃而选择将资产拿回中外制药重做临床1期。尽管已有众多国内外药企的携带共刺激信号的TCE已进入临床治疗实体瘤,但截至目前尚未获得明确的临床验证。在中外制药启动RG6524的第二项临床1期后,有两款来自中国的类似的TCE也陆续进入临床,分别是艾科联的CD3/4-1BB/DLL3三抗TCE(EXP011)及复宏汉霖的CD3/CD28/DLL3/DLL3四抗TCE(HLX3901)。三款TCE的临床1期设计方案及结果值得进一步关注。下一代TCE的成功离不开精巧的分子设计与优化、严谨的体内外筛选以平衡药效与毒理、富有经验的临床设计及CRS管理。因此,想要全面超越第一代DLL3 TCE(Tarlatamab)可能还有相当长的路要走。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。