美国食品药品监督管理局(FDA)在审批新药时,面临一个根本性矛盾:既要确保疗效的确定性,又要加快患者用药的可及性。1992年设立的“加速批准”通道,允许基于替代终点(如无进展生存期)批准药物上市,前提是企业后续开展确证性试验验证临床获益。
这一政策的初衷是:患者愿意接受疗效的不确定性,换取更早用上救命药。然而,超过一半的加速批准抗癌药最终未能证实总生存期获益,却让患者在未知中承受毒性、花费高昂费用。
问题是:患者真的愿意用“不确定性”换“快一点”吗?这项发表在The Lancet Oncology的离散选择实验(DCE),首次给出了量化答案。
一、研究背景与目的
自1992年以来,FDA已批准超过200个抗癌药的加速上市,基于的替代终点(如无进展生存期)只需“合理可能”预测临床获益。然而,真实世界数据显示:过半加速批准药物最终未在总生存期或生活质量上带来获益,而确证性试验常被拖延,有些药物上市十余年仍未证实疗效。
FDA声称,加速批准反映了“患者愿意接受疗效的不确定性,换取更早用上急需药物”。但这一假设从未被实证检验:患者究竟愿意为“快”牺牲多少“准”?不同人群的容忍度是否不同?替代终点的疗效数据能否弥补不确定性的缺憾?
本研究旨在通过离散选择实验(DCE),量化有癌症经历的人群对“疗效确定性”与“等待时间”的权衡意愿,为监管政策提供实证依据。
二、研究方法与结果
1.样本:870位“有癌症经历”的美国成年人
研究通过Cint平台招募了3427人,最终纳入870位完成高质量问卷的受访者。纳入标准是“有癌症经历”:即本人曾患癌、或有亲友患癌。
这一设计巧妙之处在于:它既保证了样本对肿瘤治疗有真实体验和认知,又通过配额抽样(年龄、性别、种族、收入、教育)实现了全国代表性,特别是年龄分布与美国癌症发病率高度匹配。
最终样本中,21%本人患癌,81%有亲属患癌,36%有好友患癌。平均年龄较高,符合癌症高发于老年人群的现实。
2.属性设定:5个维度还原真实决策
研究团队与临床肿瘤学家合作,将复杂的监管决策转化为患者能理解的5个属性:
功能状态:从“能从事轻体力工作”到“完全卧床不起”,共4级
预期寿命:从6个月到3年,共4级
疗效确定性:即“医生有多大把握确定药物能延长生命”,分“非常低/低/中/高”4级,并配以“无/弱/一些/强”的证据强度说明
替代终点疗效:即“药物在临床试验中延缓肿瘤生长的效果”,从1个月到5个月
等待时间:即“FDA批准该药还需等待多久”,从0个月到2年
这5个属性,覆盖了肿瘤治疗决策的核心维度:我还能活多久?我现在状态如何?这药到底有没有用?证据有多硬?我要等多久?
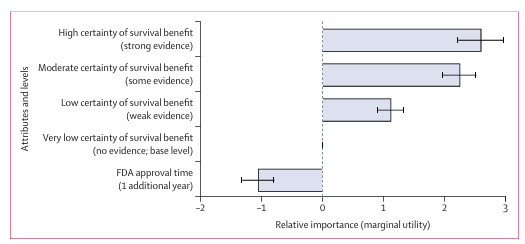
属性的相对重要性
三、实验设计:12道选择题,严控质量
采用Ngene软件生成贝叶斯高效设计,每位受访者完成10个核心选择任务,外加优势检验和一致性检验,共12道题。每道题呈现两个新药方案,要求受访者选择偏好哪个。答题时间过短(<40%中位时间)的样本被剔除,确保数据质量。
四、核心发现
条件logit模型显示,受访者对“疗效确定性”有极强的正向偏好:从“非常低”到“高”,效用值提升2.61。对“等待时间”则有强烈的负向偏好:每多等1年,效用值下降1.04。这意味着,患者同时对“准”和“快”有强烈需求,但两者冲突——要更确定,就要等更久。
五、愿意等多久?
答案:比FDA想象的要久
在“非常低确定性”下,患者愿意为达到“低确定性”等待7.86个月,为“中确定性”等待16.34个月,为“高确定性”等待21.68个月。真实世界中,从替代终点到总生存期数据平均只需11个月。这意味着患者愿意等待的时间远超确证疗效所需时间:FDA可能低估了患者等待更高确定性的意愿。
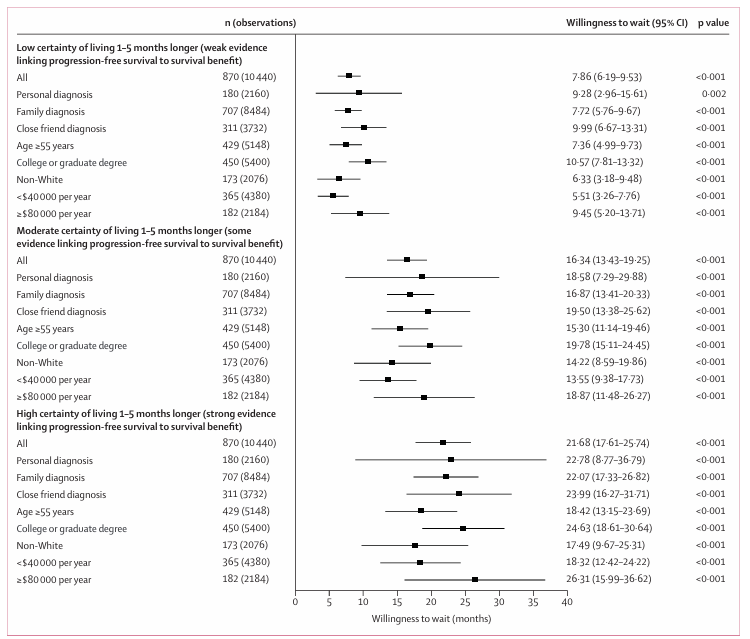
等待新癌症药物生存获益更有把握的意愿
六、谁更愿意等?
亚组分析显示:个人患癌者、高学历者、高收入者更愿意等待;非白人、低收入、低学历、55岁以上人群更不愿意等待。加速批准政策对不同群体影响不同,监管决策需精细考虑人群差异。
七、替代终点数据有用吗?
受访者对“替代终点疗效”几乎不敏感——即便药物延缓肿瘤生长效果显著(5个月 vs 1个月),只要疗效确定性很低,患者依然不买账。这直接挑战了加速批准的核心假设:用替代终点数据“替代”总生存期证据,患者并不认可。
八、健康状态如何影响决策?
功能状态越差、预期寿命越短的患者,对等待时间越敏感,对疗效确定性越不敏感。生命倒计时的人,宁愿要“可能有用”的药,也不愿等“确定有用”的药。加速批准对晚期患者更有价值,但对状态尚可的患者可能是“不必要的冒险”。
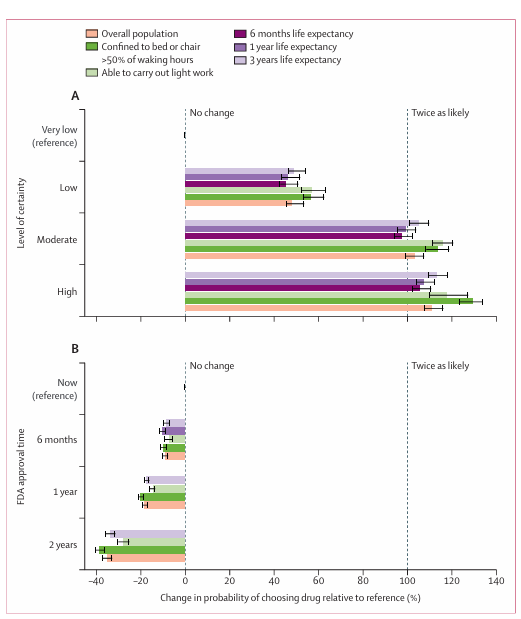
功能状态和预期寿命对药物选择概率的边际效应
九、总结
这项DCE研究之所以能发表在顶刊,并非因为方法学多么复杂,而是因为它做对了三件事:
第一,选题“怼”上监管痛点。FDA的加速批准政策争议二十年,却从未被实证检验。这项研究直接回应了这一核心问题,提供了患者偏好的量化证据。
第二,样本设计体现“政治正确”。不是随便抽样,而是配额匹配全国人口特征,年龄分布贴合癌症发病率,确保结论的外部效度。
第三,输出具有政策转化力。不是止步于“患者更喜欢什么”,而是计算出“愿意等待多久”,并与真实世界确证时间(11个月)对比,直接回应监管决策阈值。
对中国学者的启示是:如果要做类似研究,请找到中国特色的监管/医保矛盾。 比如NMPA的附条件批准、国家医保谈判中“疗效不确定性”与“价格”的权衡、以临床价值为导向的改革背景下,医保是否该为“不确定性”买单。
选题“怼”上本土痛点,方法学严格复刻,临床专家深度参与。这样的DCE研究,完全具备冲击顶刊的潜力。
[1]https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(24)00596-5/fulltext
