
近日,印度制药公司Zydus Lifesciences(下称Zydus)宣布,其授权给康哲药业控股有限公司(867.HK/8A8.SG,下称“康哲药业”)的创新口服片剂Desidustat(德昔度司他)已获NMPA批准,用于治疗非透析成人慢性肾病(CKD)患者的肾性贫血。
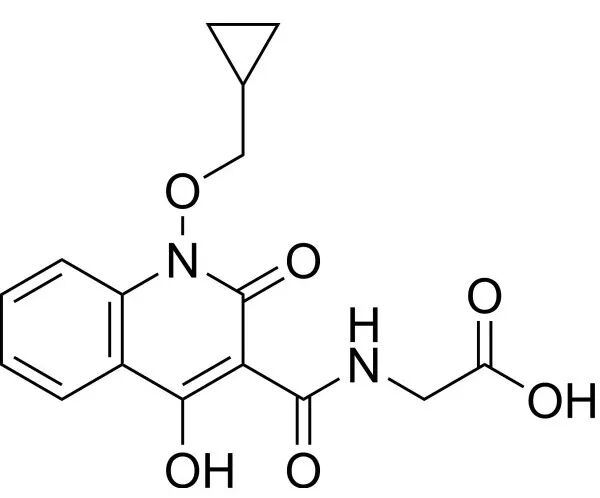
据悉,Desidustat是一种缺氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI),于2020年独家授权给康哲药业。Desidustat在印度已获批上市,以Oxemia™为品牌名进行销售,自2022年推出以来已成功治疗超过10万名因CKD贫血的患者。
01
口服HIF-PHI,让治疗转向“生理性调控”
要理解Desidustat等一类HIF-PHI新药的意义,需要首先挖掘肾性贫血治疗的核心痛点。肾性贫血主要因慢性肾脏病导致肾功能受损,致使红细胞生成素 (EPO) 生成不足、铁利用障碍、红细胞寿命缩短(如尿毒症毒素影响)及失血等因素,引起骨髓造血功能减低,通常表现为正细胞正色素性贫血。
而传统治疗的“天花板”效应在于EPO产生不足与铁代谢障碍并存,传统治疗需高剂量ESA(红细胞生成刺激剂)导致心血管风险增加,且静脉铁剂使用受限、患者依从性差。慢性肾病患者体内存在慢性炎症,会产生高水平的铁调素,导致补铁后铁离子难以从储存库中释放出来利用,出现“有铁也用不上”的现象。
此外,口服铁剂胃肠道副作用大、吸收不佳,而静脉铁剂的使用与心血管及过敏风险相关,且频繁静脉注射给血液透析患者带来极大的心理和身体负担。肾性贫血需要长期管理,患者可能因经济压力、治疗副作用或频繁的医疗访视而中断治疗。
而HIF-PHI的出现,则标志着肾性贫血从替代治疗向“生理性调控”的转变。与传统外源性红细胞生成刺激剂(ESAs)不同,HIF-PHI通过小分子口服制剂特异性抑制脯氨酰羟化酶(PHD)的活性,稳定细胞内的缺氧诱导因子(HIF-α)。
这一机制模拟了人体的低氧适应反应:稳定的HIF-α转入细胞核,与HIF-β形成异二聚体,进而启动下游靶基因的转录。其临床价值体现在双重调控上:一方面,它诱导肾脏及肝细胞内源性促红细胞生成素(EPO)的合成与分泌,恢复了符合生理节律的红细胞生成指令;另一方面,它同步调控铁代谢相关基因,抑制铁调素(Hepcidin)表达,促进肠道铁吸收及巨噬细胞铁释放,有效改善了功能性缺铁状态。
已有III期临床试验及真实世界研究证实,HIF-PHI在非透析及透析依赖的CKD患者中均能显著提升并维持血红蛋白水平,且口服给药方式极大地优化了患者的治疗依从性与生活质量。随着2025年多项国际指南的更新推荐,HIF-PHI正逐步确立其在肾性贫血全程管理中的重要地位。
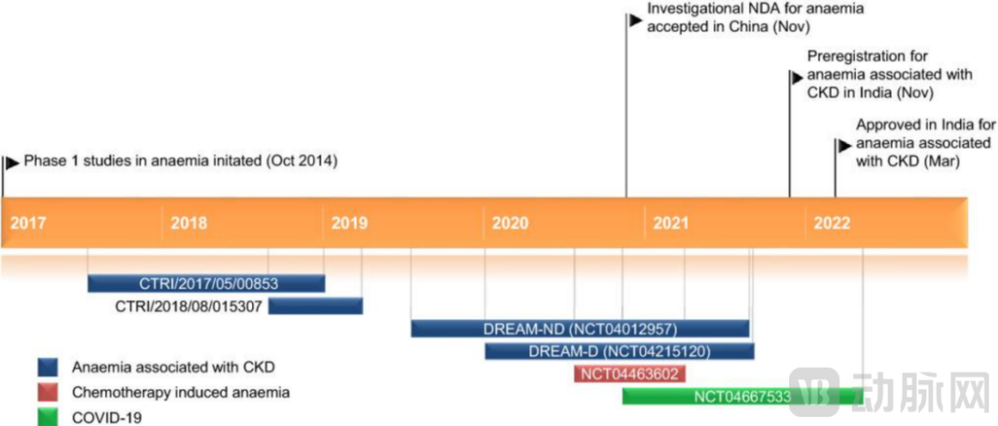 Desidustat的关键里程碑
Desidustat的关键里程碑
02
安全性+被验证的“可控”,III期数据打消临床顾虑
不过,业内也有一种担忧,即“新型药物HIF-PHI虽有改善,但长期疗效与安全性仍需随访;与此同时,由于且铁利用率高,有导致功能性铁缺乏的风险”。
基于Zydus公布的III期临床试验(DREAM-D和DREAM-ND研究)数据及印度药品控制总署(DCGI)的审评报告,Desidustat的安全性特征已得到充分验证。作为一类口服HIF-PHI药物,其安全性谱系与传统的注射用促红细胞生成素(ESA)及其他同类口服药物相比,展现出独特的优势与可控的风险特征。
Desidustat组的TEAEs(治疗在治疗过程中出现的突发不良事件)发生率与安慰剂组或活性对照组(如ESA)相当,未出现显著差异。大多数不良事件为轻度至中度(Grade 1-2),严重不良事件(SAE)的发生率低,且多数被评估为与药物无直接因果关系。
因不良事件导致的停药率在Desidustat组中极低(通常<5%),表明患者能够长期耐受该药物治疗。Desidustat最常见的不良反应主要集中在消化系统和一般性症状,通常具有自限性或易于管理。
其中,高血压这是ESA类药物备受关注的副作用。数据显示,Desidustat组的高血压发生率与对照组相似,且由于内源性EPO分泌更符合生理节律,避免了血药浓度峰谷波动,理论上降低了血压剧烈波动的风险。研究中未观察到因高血压导致的停药率显著增加。
此外,对于任何红细胞生成刺激剂,血栓栓塞事件(如深静脉血栓、肺栓塞、心肌梗死、中风)是核心安全监测指标。III期研究显示,Desidustat组的血栓栓塞事件发生率处于低风险水平,与对照组相比无统计学显著差异。这表明在规范监测血红蛋白(Hb)水平(控制在10-12 g/dL)的前提下,该药物并未额外增加血栓风险。
而在铁代谢相关安全性方面,与传统ESA易导致功能性缺铁不同,Desidustat通过抑制铁调素(Hepcidin)改善铁利用。临床数据未显示血清铁蛋白或转铁蛋白饱和度异常升高至危险水平。药物的“按需动员”机制确保了铁释放与红细胞生成的平衡,避免了盲目补铁带来的氧化应激风险。
而康哲药业也在公告中称,Desidustat在中国Ⅲ期临床试验取得了积极结果。主要研究终点血红蛋白(Hb)水平(第7-9周Hb平均值相对于基线的变化)结果显示,试验组优于安慰剂组。扩展期研究结果显示,该产品可使Hb水平长期维持在达标水平,且安全性良好。此外,产品还可以显著降低铁调素水平,纠正铁代谢紊乱。
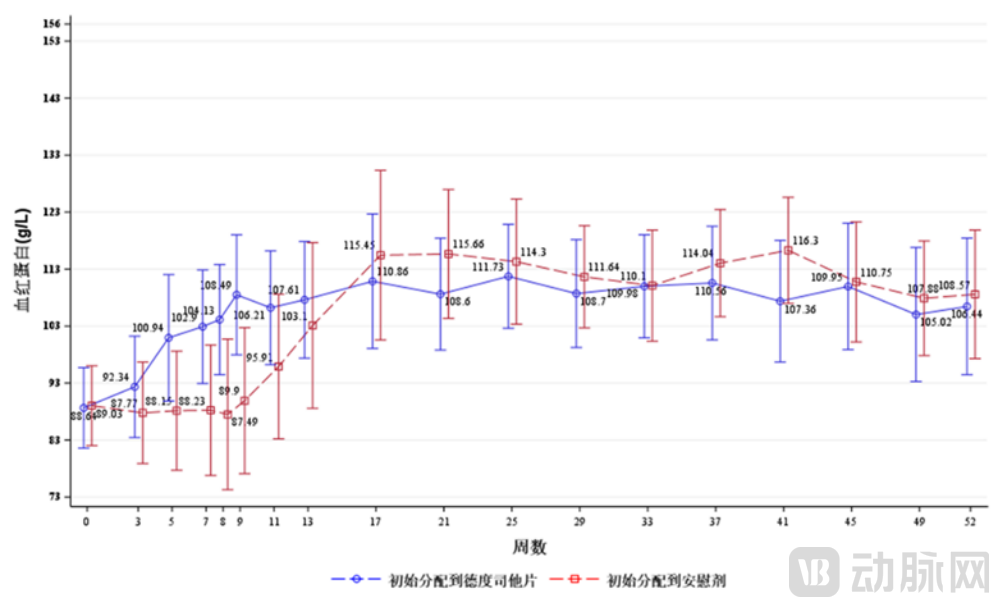 Hb随时间变化
Hb随时间变化
03
1.56亿患者的新解:Desidustat叩开中国市场大门
而Desidustat在中国的获批,则标志着这款已在印度上市多年的HIF-PHI类药物正式叩开中国市场大门。
从市场机遇看,Desidustat可谓踩在了一个巨大的“未满足需求”之上。《中国高磷血症医患诊疗现状蓝皮书》指出,中国CKD患者人数已达约1.56亿。而根据《糖尿病肾脏疾病肾性贫血认识与管理中国专家共识(2023年版)》和《中国肾性贫血诊治临床实践指南》,中国CKD患者贫血发生率极高,非透析患者贫血患病率为28.5%-72.0%,而维持性透析患者贫血患病率高达91.6%-98.2%。
这一落差的背后,是现有治疗手段的局限:促红细胞生成素(ESA)需要注射给药,患者依从性差;传统口服铁剂吸收不稳定。Desidustat采用口服给药,其III期临床数据显示能长期维持血红蛋白达标,同时显著降低铁调素、纠正铁代谢紊乱,在依从性和作用机制上具备差异化优势。
另一方面,Desidustat进入中国市场后,必然也会加入逐渐变得激烈的竞争局面。国内HIF-PHI赛道已有产品占位:珐博进/阿斯利康的罗沙司他(爱瑞卓)作为全球首款HIF-PHI,自2018年在中国获批后已深耕多年,占据先发优势;此外,信立泰的恩那度司他于2023年6月获批用于非透析的成人慢性肾脏病(CKD)贫血治疗,并于2025年9月获批新增用于透析的成人慢性肾脏病(CKD)贫血治疗,目前已实现CKD患者(非透析和透析)治疗的全面覆盖。
在定价层面,罗沙司他已进入国家医保目录,后发者若无法在疗效或安全性上形成明确区隔,也将面临价格博弈。
不过,康哲药业的应对策略也值得关注:公司将Desidustat与已商业化的高磷血症药物维福瑞(蔗糖羟基氧化铁咀嚼片)协同布局,通过肾内科专家资源与渠道网络的高效联动,试图打造肾病专科产品矩阵。这一“组合拳”思路,有望在一定程度上对冲单一产品的竞争压力。
整体而言,Desidustat踩准了非透析CKD贫血这一蓝海细分市场,口服优势切中依从性痛点,而如何在当下的竞争格局中撕开缺口,则考验康哲药业的商业化执行力。
如果您想对接文章中提到的项目,或您的项目想被动脉网报道,或者发布融资新闻,请与我们联系;也可加入动脉网行业社群,结交更多志同道合的好友。



近
期
推
荐



