引言
免疫检查点抑制剂(ICI)治疗极大地改变了实体瘤的治疗前景。然而,免疫疗法治疗通常受到毒性或原发性或继发性免疫疗法耐药性发展的限制。耐药机制包括肿瘤内在和外在因素,从抗原呈递受损和功能失调的信号通路到免疫抑制性肿瘤微环境(TME)和宿主系统因素。
此外,包括脾脏和淋巴结在内的免疫系统器官在ICI反应中起着至关重要的作用。循环T细胞可以被驻留在脾脏中的抗原呈递细胞(APC)激活,并随后在肿瘤内发挥其作用。在肿瘤进展期间,脾脏经历增强的髓外造血作用,并含有免疫抑制性骨髓细胞,包括骨髓来源的抑制细胞(MDSCs),其钝化T细胞活化,促进肿瘤生长,并有助于ICI抗性。脾脏还通过脾脏PD-L1+骨髓细胞促进肿瘤免疫逃逸和抗原特异性耐受。靶向脾脏内的PD-1/PD-L1轴可以帮助逆转免疫抑制并促进更有效的抗肿瘤反应。占脾脏细胞70%以上的红细胞起着免疫调节剂的作用,具有独特的特性,使其成为细胞药物输送的合适候选者。先前的研究已经设计了工程红细胞来激活脾脏免疫系统以产生抗肿瘤作用;然而,这些模型显示出有限的功效。
近期,一种新型的红细胞-抗体偶联物通过将抗PD-1抗体偶联至红细胞表面,显示出重塑抗肿瘤免疫反应的潜力,并在对抗PD-1耐药的晚期实体瘤患者中展现出有前景的安全性和疗效数据。
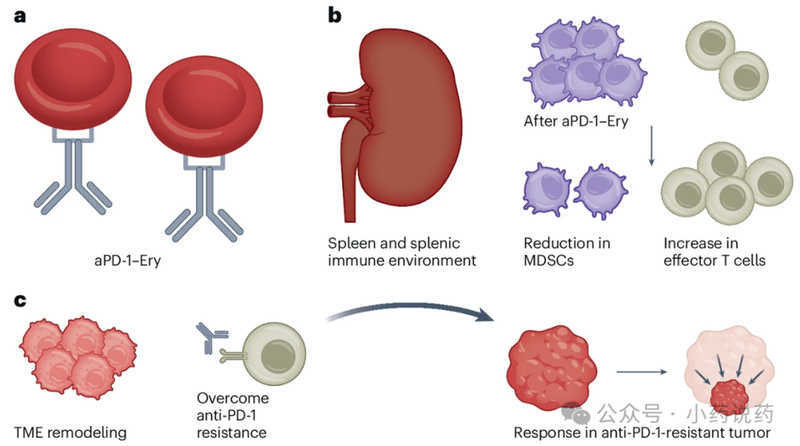
作者通过化学交联剂将市售抗PD-1抗体pembrolizumab与天然红细胞共价连接,开发了aPD-1-Ery。值得注意的是,通过测量临床前小鼠模型中的生物分布特征,他们表明,与抗PD-1抗体不同,aPD-1-Ery可以有效地在脾脏中持续积累,从而激活局部免疫系统。aPD-1–Ery的抗肿瘤作用取决于完整的脾脏功能。
-02-
一、aPD-1-Ery的作用机制
aPD-1-Ery的核心机制在于其独特的生物分布特性。与抗PD-1抗体不同,aPD-1-Ery能够在脾脏中有效蓄积并长期存在,从而激活局部免疫系统。其抗肿瘤作用依赖于完整的脾脏功能。具体机制包括:
重塑脾脏免疫景观:aPD-1-Ery通过扩增效应T细胞并减少免疫抑制性髓系细胞,有利地重塑了脾脏免疫景观。
调节肿瘤微环境:这种重塑作用有助于重塑肿瘤微环境并抑制肿瘤生长,从而产生强烈的抗肿瘤反应。
全身性免疫调节:在临床前模型中,aPD-1-Ery治疗导致脾脏、外周血及肿瘤微环境中的MDSCs显著减少,并伴随效应T细胞的增加和肿瘤内促炎状态的增强。
-03-
二、临床前研究证据
1. 对敏感肿瘤模型的疗效
在对抗PD-1敏感的MC38肿瘤携带小鼠模型中,aPD-1-Ery通过改变脾脏免疫细胞的组成和重塑肿瘤微环境抑制了肿瘤生长。质谱流式细胞术分析显示,与帕博利珠单抗治疗组相比,aPD-1-Ery治疗组小鼠的MDSC亚群减少幅度更大,同时单核细胞和巨噬细胞减少,CD8和CD4效应T细胞增加。此外,IFNγ检测证据表明脾细胞中肿瘤反应性T细胞增强,提示源自脾脏的特异性免疫反应增强。
2. 克服耐药性
研究进一步在抗PD-1耐药的小鼠模型(同基因KP肺癌和pB3乳腺癌模型)中评估了疗效。在KP模型中,aPD-1-Ery治疗组肿瘤大小减少了超过80%,而帕博利珠单抗治疗组仅有轻微缩小。在pB3模型中,aPD-1-Ery治疗组肿瘤大小减少了超过50%,而帕博利珠单抗治疗组无肿瘤缩小。这表明aPD-1-Ery通过脾脏调节,在多种ICI耐药肿瘤模型中具有显著的抗肿瘤活性。
3. 协同作用
研究还发现,aPD-1-Ery与抗PD-1抗体联合使用可产生协同抗肿瘤作用。
-04-
三、临床转化:首次人体试验
基于临床前研究的积极结果,研究人员开展了一项针对aPD-1-Ery的首次人体I期临床试验(NCT06026605)。该试验纳入了14例对抗PD-1/PD-L1免疫治疗耐药的晚期实体瘤患者(涵盖11种肿瘤类型),并在两个剂量水平接受aPD-1-Ery单药治疗。
2. 安全性与耐受性
试验的主要终点是安全性和耐受性。结果显示,治疗耐受性良好,未出现剂量限制性毒性,也未发生4级或5级治疗相关不良事件。值得注意的是,重复给药未导致治疗相关的严重溶血性贫血、免疫相关毒性或针对帕博利珠单抗的抗药物抗体产生。
3. 临床疗效
根据RECIST 1.1指南评估肿瘤反应(次要终点)。结果显示,6例患者达到客观缓解(1例完全缓解,5例部分缓解),11例患者达到疾病控制,总体缓解率为42.9%,疾病控制率为78.6%。中位无进展生存期为5.5个月,总生存期尚未达到。获得完全缓解的患者在6个月随访时仍维持缓解,3例部分缓解患者的缓解持续时间超过一年,提示获益持久。
4. 外周免疫指标变化
aPD-1-Ery治疗导致患者体内循环免疫抑制性髓系细胞减少,T细胞快速且持续增加。在缓解者中,首次给药后72小时,总T细胞和CD8效应T细胞数量分别增加了1.68倍和1.59倍。这些发现与临床前研究结果一致。
结语
aPD-1-Ery作为一种新型红细胞-抗体偶联物,通过将抗PD-1连接至红细胞膜并在脾脏蓄积,通过扩增效应T细胞和减少免疫抑制性髓系细胞有利地重塑脾脏免疫景观,最终重塑肿瘤微环境并抑制肿瘤生长。这项研究填补了通过靶向脾脏免疫环境来克服ICI耐药的关键空白。目前,针对抗PD-1耐药患者的治疗策略包括与替代检查点抑制剂联合治疗、根据肿瘤分子检测切换靶向治疗以及T细胞疗法,而靶向脾脏环境代表了克服抗PD-1耐药的重要策略。基于发表的结果,该红细胞-抗体偶联物有理由在II期研究中进一步研究,并鉴于其与抗PD-1单药治疗的协同反应证据,可考虑不仅在二线治疗中,也在一线治疗中进行探索。此外,该平台为其他治疗性单克隆抗体的替代偶联模型开辟了广阔可能性,这可能对改善多种实体瘤的抗肿瘤疗效和克服ICI耐药产生深远影响。
参考资料:
Erythrocyte-antibody conjugates to overcome immunotherapy resistance. Nat Cancer. 2026 Feb 20.公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
