引言
G蛋白偶联受体(GPCR)构成了最大的药物靶标家族之一,反映了它们在众多病理生理过程中的参与度。本文综述了GPCR超家族的药物发现趋势,涵盖了已获得监管批准或正在临床试验中研究的化合物、靶点和适应症。分析发现,目前有516种获批药物靶向GPCR,占所有获批药物的36%。这些药物作用于121个GPCR靶点,占所有非感官GPCR的三分之一。此外,针对133个GPCR(包括30个新靶点)的337种药物正处于临床试验阶段,这表明未来获批药物的数量将持续增长。
-02-
一、历史背景
GPCR形成一个包含约800种膜蛋白的超家族,它们被细胞外刺激激活,共享典型的七螺旋跨膜结构域,并主要与细胞内转导蛋白(如G蛋白和抑制蛋白)偶联。大多数GPCR具有共同的进化起源,共同参与复杂的信号系统,调节无数的生理和病理生理过程。因此,GPCR一直是所有主要治疗领域的常用靶标,超过30%的获批药物靶向GPCR。
GPCR相关药物开发的历史可以追溯到“GPCR”一词被创造之前。最早有文献记载的GPCR作用制剂研究可追溯到19世纪,描述了1805年吗啡和1875年毛果芸香碱的分离及医疗应用。20世纪中叶,发现了由被称为“肾上腺素能受体”的实体介导的肾上腺素分子功能。1980年代末和1990年代,药物-靶标相互作用理解的进步揭示了配体不仅可以选择性激活特定受体,还可以选择性触发不同的细胞内转导蛋白,这为“偏向信号”这一新范式铺平了道路。此外,研究显示配体可以结合在生理配体结合位点(“正构”位点)之外的远处“变构”位点,这些机制为设计副作用更少的药物提供了机会。
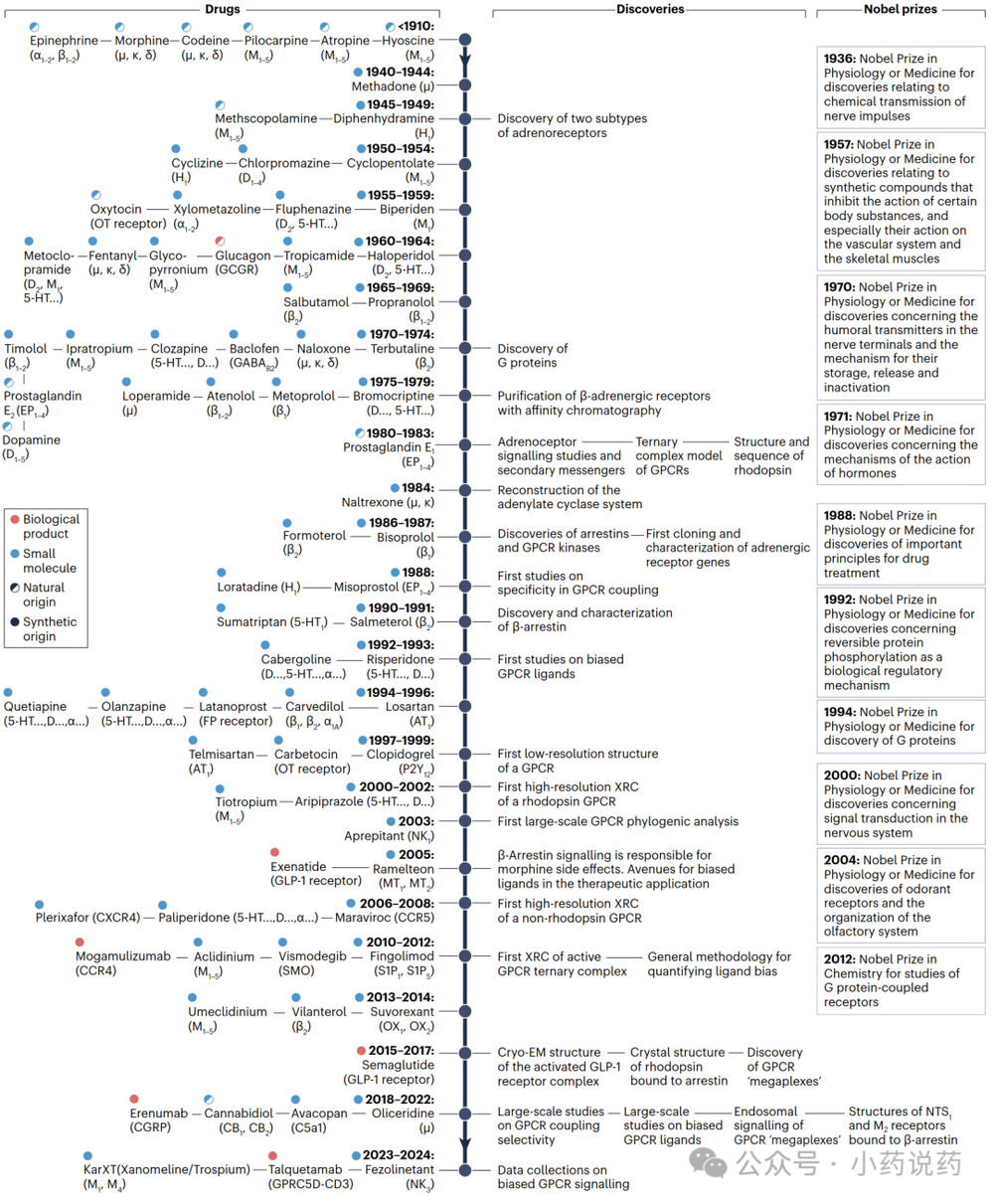
2000年牛视紫红质和2007年β2 -肾上腺素能受体的首批X射线晶体结构的报道,揭示了其整体高分辨率架构,提供了机制见解并使基于结构的药物设计成为可能。近年来,随着冷冻电子显微镜和核磁共振技术的进步,针对GPCR的生物制剂(如单克隆抗体)研发也获得了动力,2018年FDA批准了首个靶向GPCR的单抗Erenumab用于预防偏头痛。
-03-
二、获批药物与靶点概览
1. 获批药物统计
目前在北美、欧洲、亚洲和澳大利亚市场上有516种不同的药物靶向GPCR用于治疗。这些靶向GPCR的药物约占所有获批药物的36%,略高于此前报道的30-33%。在过去5年(自2019年以来),有37种靶向GPCR的新药获得批准,其中包括7个首次获批的受体:胃抑制多肽(GIP)受体(GIPR)、GPRC5D、C5A、神经激肽-3(NK3)以及黑素皮质素受体3、4和5(MC3/4/5)。最近批准的是KarXT(Cobenfy),这是一种xanomeline(M4毒蕈碱乙酰胆碱受体选择性激动剂)和trospium(外周毒蕈碱拮抗剂)的组合,是首个治疗精神分裂症的同类药物。
2. 临床试验中的药物
基于ClinicalTrials.gov的数据,目前有337种药物正处于临床试验阶段,其中172种为新药,165种为老药新用药物。在新药中,分别有51、76和45种药物进入了I期、II期和III期临床试验。
3. 靶点分布
总体而言,已有121个GPCR被“成药化”,即成为获批药物的靶点,占所有362个非感官人类GPCR的三分之一。此外,目前有133个GPCR正被临床试验中的药物靶向,其中30个尚未有获批药物靶向它们。值得注意的是,共有151个临床GPCR靶点,主要属于A类(130个),其次是B1类(13个)、C类(7个)和F类(1个)。目前尚无靶向B2类/粘附GPCR的药物进入临床试验。
-04-
三、畅销药物与主要靶点
1. 畅销药物
在2023年销量前50的药物中,有5种靶向GPCR的产品。其中Entresto(沙库巴曲/缬沙坦)用于心力衰竭和高血压。另外四种产品(含三种独特化合物)的适应症为代谢疾病领域:2型糖尿病和肥胖症,包括Ozempic(司美格鲁肽)、Trulicity(度拉糖肽)、Mounjaro(替尔泊肽)和Wegovy(司美格鲁肽)。值得注意的是,这三种化合物均靶向GLP-1受体,而替尔泊肽还作用于GIP受体。2023年,靶向GPCR的糖尿病和肥胖症药物销售额接近300亿美元。
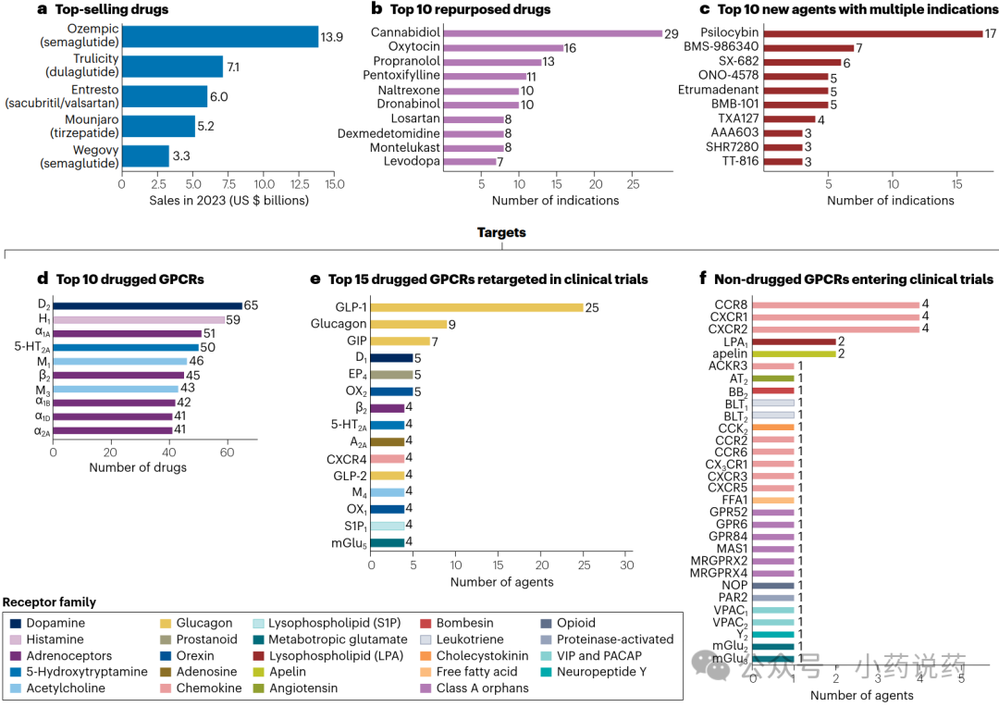
2. 主要靶点
为了确定哪些GPCR被“成药”最多,研究识别了获批药物数量最多的靶点。排名前十的GPCR均有41至65种获批药物,且均属于胺能受体亚家族,由多巴胺、组胺、肾上腺素、血清素或乙酰胆碱激活。这些靶点的获批药物众多,反映了它们是最早被发现、获得药理学分析并进行结构表征的受体之一。
-05-
四、新药与新靶点的趋势
1. 新型药物的特性
通过对临床试验中药物的分析,发现了一些显著趋势:
靶点选择性:与2017年的分析相比,新药进入临床试验显示出更强的选择性趋势。惊人的是,77%的新药只有一个靶点,20%有两个靶点,仅3%有三个或更多靶点。
变构调节剂比例增加:在新药中,变构调节剂的比例(8%)显著高于所有获批药物(1%)。变构调节提供了增加亚型选择性的优势,因为变构结合位点比正构位点保守性更低。目前有14种变构调节剂正在针对A类和C类GPCR进行研究,覆盖精神分裂症、阿尔茨海默病、肥胖症等多种适应症。
抗体和蛋白/肽类比例增长:与获批药物相比,新药中抗体的比例更高(10%对1%),蛋白/肽类的比例也更高(19%对12%),相应的小分子比例较少(71%对87%)。激动性抗体和纳米抗体有望特异性激活GPCR,提供比传统小分子更高的选择性和更长的半衰期。
2. 新型靶点
目前有30个尚未有任何获批药物的GPCR正被临床试验中的药物靶向,其中最大的一组是A类GPCR,包含9个趋化因子受体。其他新型A类GPCR靶点包括胆囊收缩素受体CCK2 、白三烯受体BTL1−2 、血管紧张素受体AT2 、Apelin受体、铃蟾肽受体BB2等。此外,还包括孤儿受体GPR6、GPR52、GPR84、MAS1、MRGPRX2和MRGPRX4。例如,CVN424靶向GPR6用于帕金森病,EP262靶向MRGPRX2用于荨麻疹治疗。
-06-
五、药物再利用与GPCR重靶向
1. 药物再利用
药物再利用定义为已获批药物用于新适应症,可能因利用现有的安全性概况而降低开发时间、成本和风险。目前,在516种获批的GPCR靶向药物中,有165种正在I期、II期或III期试验中测试新适应症。再利用药物占临床试验所有化合物的近一半(49%),表明再利用是GPCR靶向药物开发的主要驱动力。例如,大麻二酚是研究最广泛的再利用药物,有29种适应症正在研究中;催产素正在研究用于精神分裂症和PTSD;普萘洛尔则被研究用于癌症和罕见病。
2. GPCR重靶向
目前临床试验中的337种GPCR靶向药物作用于133个不同的GPCR,其中103个(77%)已是获批药物的靶点。这反映了从胺能受体向肽/蛋白受体的转移。在获批药物数量最多的前十大靶点中,只有5-HT2A 受体和β2-肾上腺素能受体也出现在当前临床试验药物数量最多的前15个靶点中。这种转移可能归因于胺能受体的饱和,以及肽/蛋白配体的GPCR数量多于小分子配体的GPCR。
3. 关键受体家族
GLP-1R, GLP-2R, GIPR和GCGR:针对这些受体的药物(如司美格鲁肽、替尔泊肽)是顶级畅销药。替尔泊肽是首个获批的GLP-1R/GIPR双重激动剂,目前还有11种双重GLP-1R/GCGR激动剂处于I至III期试验中,以及两种三重激动剂正在评估中。
食欲素受体:食欲素受体OX1和OX2参与多种神经和精神疾病的病理生理学。已获批的药物(如Suvorexant)是双重OX1和OX2拮抗剂,用于治疗失眠。目前,选择性OX1拮抗剂正在研究用于阿片类药物使用障碍,选择性OX2拮抗剂正在研究用于失眠和抑郁症。
-07-
六、适应症格局
1. 主要适应症
根据解剖学治疗化学(ATC)代码分类,获批药物数量最多的主要适应症包括精神抑制药(58种)、眼科用药(44种)、全身用抗组胺药(43种)、镇痛药(42种)和阻塞性气道疾病药物(38种)。根据ICD11分类,获批药物数量最多的疾病领域是症状/体征(132种)、循环系统疾病(86种)、精神/行为/神经发育障碍(81种)和神经系统疾病(72种)。
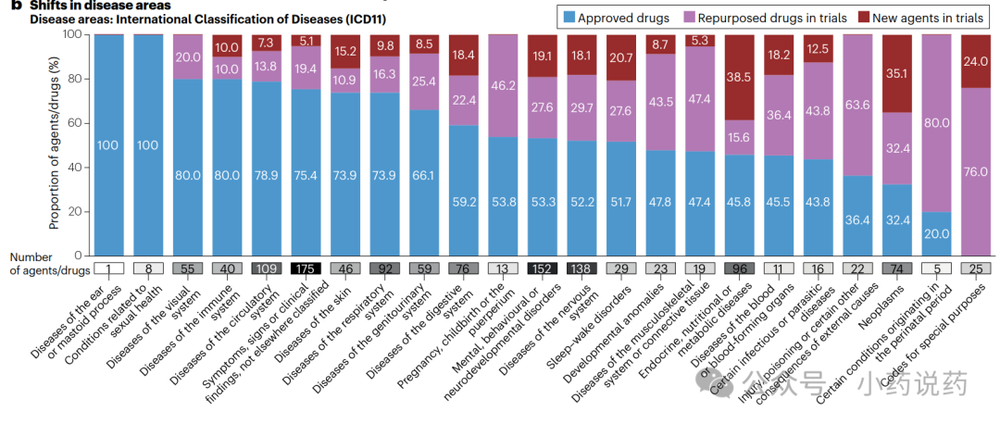
2. 适应症趋势
过去20年获批的药物在糖尿病、便秘、免疫抑制剂和抗肿瘤药物等适应症中占相当大比例。这反映了GPCR在癌症中作用的认知加深,以及GLP-1R激动剂等药物在代谢领域的成功。
3. 疾病领域的临床试验分布
在某些疾病领域,临床试验中的药物比例相对于获批药物较高,例如发育异常、肌肉骨骼系统疾病、内分泌/营养/代谢疾病、肿瘤等,这些领域超过50%的化合物处于试验阶段。相反,在循环系统疾病和免疫系统疾病中,获批药物的比例远高于试验中的药物。临床试验中药物数量最多的领域是精神/行为/神经发育障碍(71种)、神经系统疾病(66种)、内分泌/营养/代谢疾病(52种)和肿瘤(50种)。
4. 特定疾病领域的突破
糖尿病药物:靶向GPCR的糖尿病药物虽然数量不多(8种),但影响巨大,如司美格鲁肽和替尔泊肽。
免疫调节剂:已有5种GPCR药物获批作为免疫调节剂,如Fingolimod及其后续药物靶向S1P受体用于多发性硬化症。
抗肿瘤药物:首个GPCR在癌症中作用的描述可追溯到1986年MAS癌基因的发现。近期,靶向SMO受体的药物获批用于急性髓系白血病和基底细胞癌,靶向CCR4的抗体Mogamulizumab获批用于蕈样肉芽肿或Sézary综合征。Talquetamab作为一种双特异性GPRC5D-CD3 T细胞接合剂,于2023年获批用于多发性骨髓瘤。
-08-
七、未开发的靶点与偏向信号
1. 未开发靶点的潜力
尽管GPCR是最重要的药物靶标家族之一,但其非感官受体中仅有三分之一被临床靶向。通过关联文献数据、配体数据和结构数据,研究人员评估了不同靶点的开发状态。分析显示,一些未靶向受体(如CCR7、MCH1、Neuropeptide S受体)拥有丰富的公共数据,可能是潜在的新兴靶点。例如,CCR7有超过300篇出版物,可能在癌症中作为靶点。
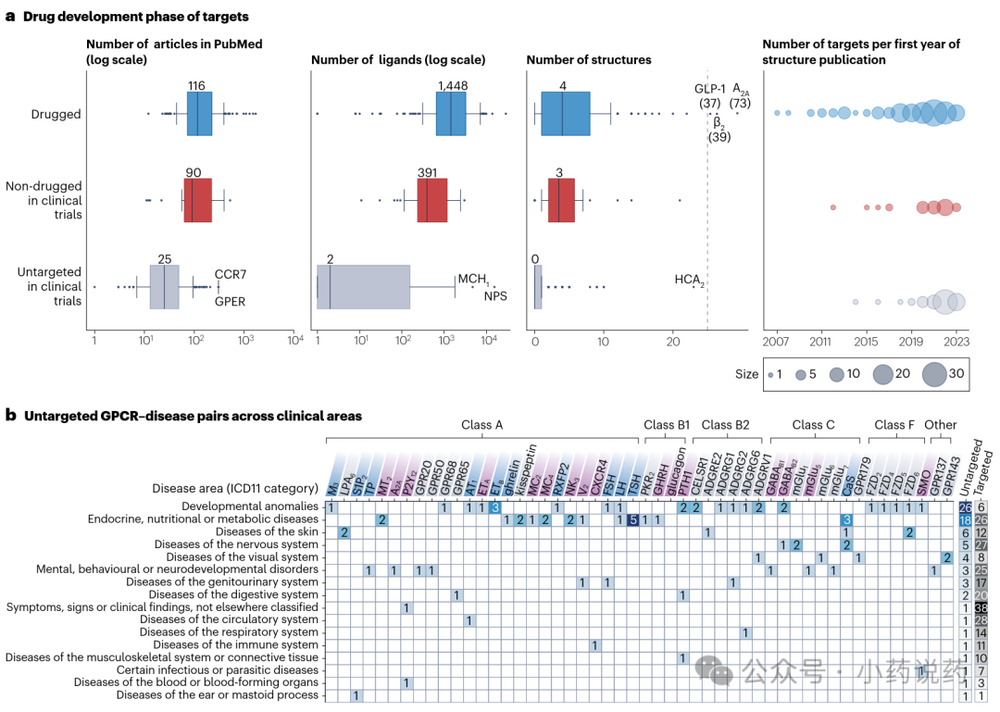
2. 未靶向的GPCR-疾病对
通过整合Open Targets平台的疾病关联评分,研究发现有50个非感官GPCR与84种疾病相关。其中,发育异常(26种疾病)和内分泌/营养/代谢疾病(18种疾病)领域的疾病数量最多。钙敏感受体具有最多的未靶向疾病关联(6种),TSH受体则关联5种未靶向疾病。此外,整个粘附受体类(B2类)和Frizzled受体类的大多数成员仍处于未靶向状态。
3. 偏向信号
“偏向配体”能够差异性地激活GPCR信号传导的细胞内转导蛋白(如G蛋白和β-抑制蛋白)。偏向信号在设计具有更好疗效和安全性的药物方面具有巨大潜力,因为它可以优先激活治疗有益的信号通路,同时避免引起不良反应的通路。例如,BnOCPA通过腺苷A1受体产生偏向性激活,在不引起心肺抑制的情况下发挥镇痛作用。首个被设计为偏向激动剂的获批药物是Oliceridine,一种μ-阿片受体配体。然而,偏向信号的临床转化仍面临挑战,如体外结果向临床概况改善的转化有限,以及参考配体的选择问题。
-09-
结语
GPCR作为药物靶标家族的重要性毋庸置疑。分析表明,GPCR在未来的药物开发中将继续发挥重要作用,这得益于临床试验中大量的药物、不断增长的适应症格局、未开发的疾病关联以及近期公布的公司合作伙伴关系。考虑到临床试验中生物制剂比例的翻倍(从13%增至29%)和变构调节剂比例的八倍增长(从1%增至8%),这些新型药物形式将为下一代GPCR靶向药物做出重要贡献。同时,药物再利用也占据了临床试验药物的近一半,表明这也是未来GPCR疗法的重要来源。
参考文献:
GPCR drug discovery: new agents, targets and indications. Nat Rev Drug Discov. 2025 Jun;24(6):458-479.
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
