近日,百济神州宣布注射用塔拉妥单抗通过国家药品监督管理局(NMPA)优先审评程序,获附条件批准上市,用于:既往接受过至少 2 种系统性治疗(含铂化疗)失败的广泛期小细胞肺癌(ES-SCLC)成人患者。
根据其新闻稿,该药是目前国内首个且唯一获批靶向 DLL3 和 CD3 的双特异性 T 细胞衔接器(TCE)抗体。
新药有效性
本次获批依据 DeLLphi-301、DeLLphi-307 两项关键注册临床研究结果。
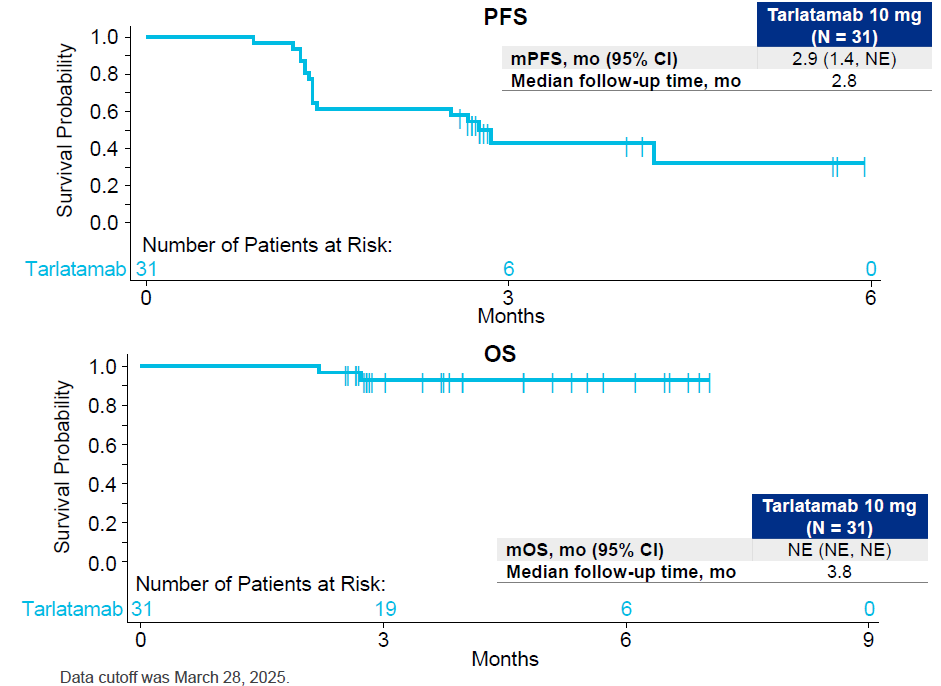
新药安全性
最常见不良反应为细胞因子释放综合征(CRS)、食欲减退、发热、味觉倒错、便秘、贫血、疲劳、恶心;
因治疗期间不良事件导致的永久停药比例较低。其中 CRS 多发生在前两次给药,以 1-2 级轻度事件为主,通过常规支持性护理即可有效控制,整体未出现新增或非预期安全信号。
参考来源:
1.药企官网
2.Hummel HD, Ahn MJ, Blackhall F, et al. Patient-Reported Outcomes for Patients with Previously Treated Small Cell Lung Cancer Receiving Tarlatamab: Results from the DeLLphi-301 Phase 2 Trial. Adv Ther. 2025;42(4):1950-1964. doi:10.1007/s12325-025-03136-4
3.2025 WCLC
声明:本文旨在促进医药学术的沟通和交流,仅供医疗卫生专业人士参阅,梅斯医学不对任何药品和/或适应症作推荐。文中涉及的药品信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医院医生的意见或指导。
