
2025年5月27日,GlycoEra公司宣布完成1.3亿美元的B轮融资,至此公司累计融资1.79亿美元。此次融资将用于推进细胞外蛋白降解剂的管线研发。
这一动态背后折射出自身免疫疾病治疗领域在实际应用中的三大局限:疗效深度不足、免疫抑制风险较大、起效速度缓慢。
首先是疗效深度不足,传统药物仅能实现对目标蛋白的功能阻断,无法彻底清除致病蛋白。这会导致疾病难以根治;其次是免疫抑制风险较高,广泛抑制免疫系统的作用机制使患者感染风险显著上升;最后是起效速度缓慢,患者需要长期用药才能维持治疗效果。
针对这些关键困境,GlycoEra凭借双功能降解剂技术,可精准锁定并彻底清除血液中的致病蛋白(如自身抗体)。
01
双功能糖工程降解剂:分子级“智能回收系统”
以类风湿关节炎、红斑狼疮为代表的自身免疫疾病,其核心发病机制是异常抗体等蛋白质对自身组织发起攻击。传统的单抗药物(如抗TNFα制剂)在治疗中虽能够与目标蛋白结合,但这种作用更像是给致病蛋白贴上“封条”,只能暂时阻断其功能,而无法实现对致病蛋白的清除。
据GlycoEra官网,传统疗法仅能使30%~50%的患者达到临床缓解,且有40%的患者因耐药或副作用不得不停药,同时系统性免疫抑制还会使患者的感染率升高2-3倍。
GlycoEra的核心产品是双功能糖工程降解剂(Bifunctional Glyco Degrader),这款降解剂主要由三个组件构成,分别是靶蛋白结合域(Target Protein-Binding Domain)、糖链信号域(Glycan-Sensing Domain)、连接桥(Linker)。
靶蛋白结合域如同“智能夹钳”,能够特异性地捕获致病蛋白;糖链信号域就像“邮政编码”,可以展示特定的聚糖,用于结合内吞受体(ASGPR);而连接桥则类似“可调式关节臂”,能够优化空间构象,保证双功能协同运作。
双功能糖工程降解剂的“工作流程”主要分为四步:首先是精准锚定,降解剂通过抗体样结构域(Fab/scFv)锁定血液中的致病蛋白。
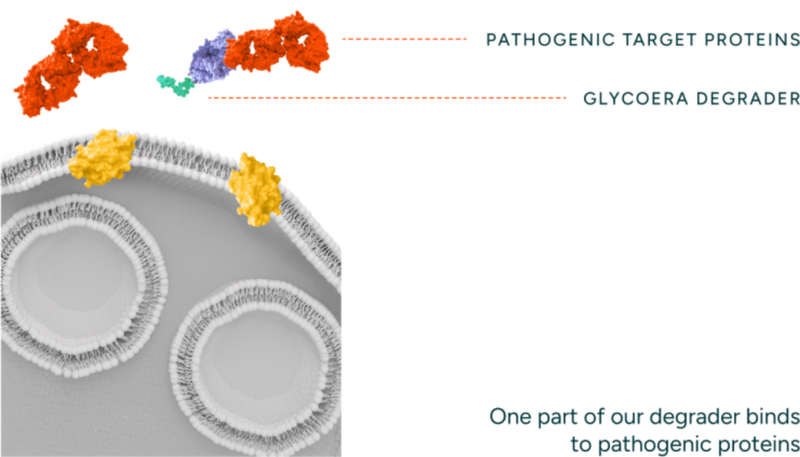
接着进行受体招募,其修饰的特定糖链(如半乳糖-N-乙酰半乳糖胺)会被肝细胞表面的ASGPR高亲和力识别。
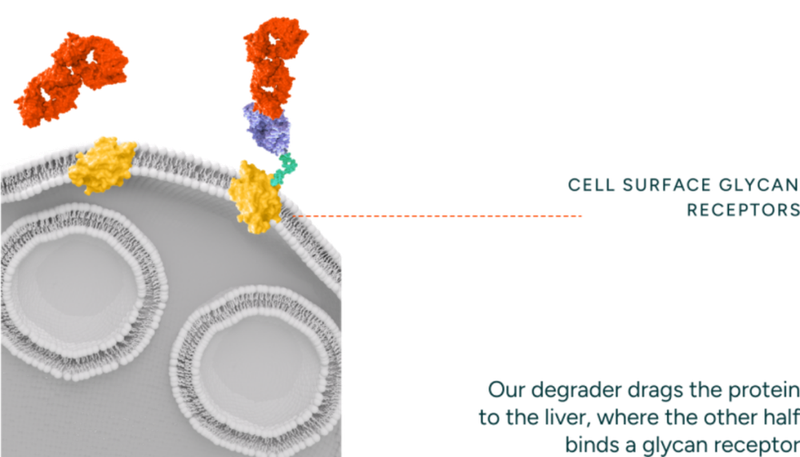
随后进入溶酶体清除阶段,复合物被内吞后转运至溶酶体,靶蛋白会被酶解为氨基酸。
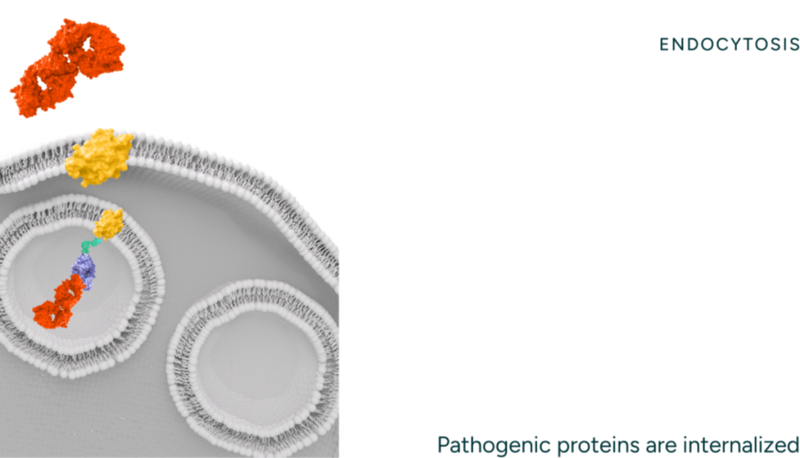
最后是受体再生,ASGPR重返细胞膜,单分子受体可循环降解200+次。
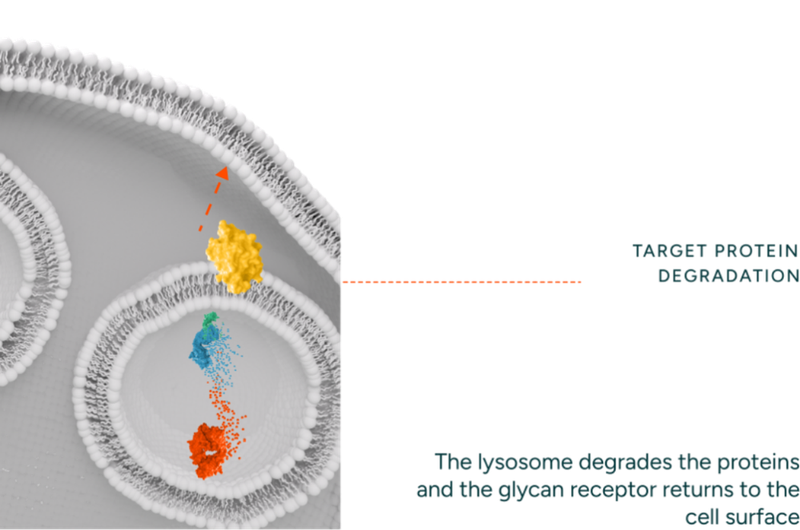
以针对类风湿关节炎的IgG自身抗体清除为例,传统单抗只能阻断IgG与Fc受体结合,但游离抗体仍会在血液中累积。而GlycoEra降解剂能将IgG抗体“押送”至肝细胞溶酶体,30分钟内清除率超过95%。
02
CustomGlycan平台:四步克服糖基化异质性难题
GlycoEra专有的CustomGlycan平台通过合成生物学实现“糖链编程”,成功解决了糖蛋白药物开发中存在的历史性难题——糖基化异质性。这一突破得益于以下四个方面的优化。
■ 细胞工厂工程化
CustomGlycan通过敲除野生型糖基转移酶基因,消除随机糖修饰,可以同时导入定制糖基化工具箱。以宿主细胞CHO-K1为例,插入β-1,4-半乳糖基转移酶基因,并插入α-2,6-唾液酸转移酶抑制基因,从而表达均一化半乳糖化N-糖链,产出降解剂的糖链均一性可达99.7%。
工作逻辑示意图
■ 一步法重组生产
传统抗体生产需经过6步纯化来去除错误糖型,而GlycoEra利用工程细胞,在发酵罐中直接表达完整降解剂,收获后仅需亲和层析单步纯化,不仅使生产成本降低了60%,批次间差异也小于5%。
■ 模块化分子设计
平台支持“即插即用”式开发,结构为[靶蛋白结合域]-[连接子]-[糖信号域]。其中,结合域可选纳米抗体/Fab/scFv;糖信号域可选ASGPR配体/甘露糖受体配体;连接子长度可调,以优化空间位阻。
在应用场景上,针对自免疾病,可选用高亲和力Fab结合自身抗体;针对阿尔茨海默病,可改用纳米抗体靶向Aβ寡聚体;针对肿瘤,可设计双靶向降解剂同时清除PD-L1和CTLA-4。
■ 内吞动力学优化
平台特有的糖链-受体亲和力预测模型解决了“内吞效率瓶颈”。CustomGlycan利用量子力学计算模拟糖-受体结合能,筛选最优糖链结构(如三触角N-糖vs二触角N-糖),使降解剂-ASGPR复合物解离常数(Kd)达到10nM级。
02
首发管线聚焦自免疾病,扩展性平台将逐步拓展疾病领域
GlycoEra的管线开发遵循严格的三重筛选逻辑:首先,靶蛋白必须是疾病的核心驱动因子,如自身免疫疾病中的自身抗体。其次,需针对现有疗法存在清除率低或安全性缺陷的临床痛点。最后,靶标需为循环蛋白或膜蛋白,以适配其细胞外蛋白降解技术平台。
遵循这样的筛选规则,GlycoEra目前已开发了以GDE-101、GDE-201为核心的多条自免疾病管线:
■ GDE-101:类风湿关节炎(RA)
GDE-101靶向IgG自身抗体,目前处于临床前阶段。其核心优势是能在30分钟内清除超过95%的致病抗体(据GlycoEra披露数据),相较于传统抗CD20单抗仅能阻断抗体功能却无法清除的局限,展现出根本性突破。
2025年第一季度,该项目已完成灵长类GLP毒理试验,数据显示,在食蟹猴模型中单次给药后,血清IgG水平下降98%,(传统抗CD20单抗平均能使IgG水平下降45%)、关节炎症评分改善90%(传统疗法平均改善50%)。
■ GDE-201:重度哮喘
GDE-201靶向IgE,用于治疗重度哮喘,目前处于先导优化阶段。作为首个可清除IgE的降解剂,其突破性在于能特异性降解游离IgE,而不直接清除表达膜结合IgE的B细胞,从而避免对正常免疫功能的干扰。2024年第四季度的小鼠模型数据显示,该药物可使肺功能改善80%,为重度哮喘患者提供了全新的治疗思路。
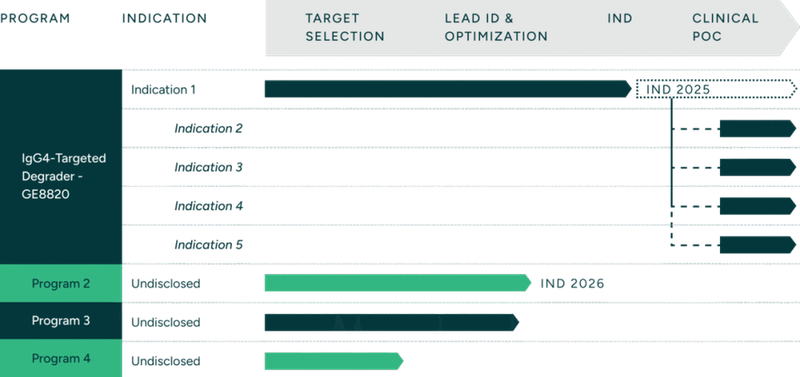
GlycoEra管道布局情况(来源:公司官网)
值得一提的是,GlycoEra专有技术平台CustomGlycan具备广泛的扩展性,能够针对任意循环蛋白设计降解剂。这意味着,其应用场景不仅局限于自身免疫疾病领域,在肿瘤驱动因子清除、神经退行性疾病毒性蛋白去除等更广阔的医学领域。
03
超20年经验的制药老将团队,融资1.79亿美元
成立仅5年的GlycoEra,在资本层面展现出了强大的吸引力。公司经历三轮融资,累计融资已达1.793亿美元。其融资节奏与公司关键里程碑紧密绑定,每一轮融资都精准助力技术研发和管线推进。
GlycoEra之所以能获得高估值,源于其平台强大的可扩展性——单次技术验证成果能够衍生出多条研发管线,这一特性显著降低了研发的边际成本,让资本看到了其技术背后巨大的商业价值和发展潜力。
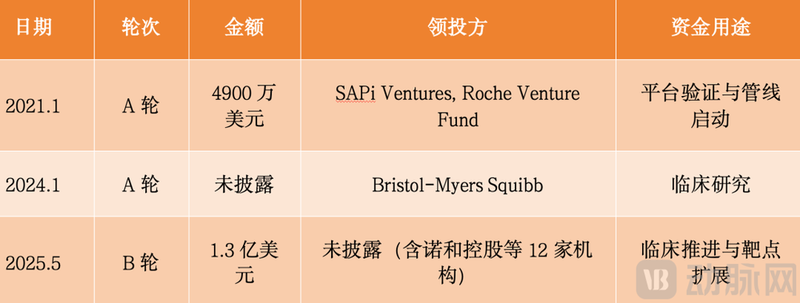
GlycoEra历史融资情况(来源:Crunchbase)
GlycoEra的竞争力不仅体现在技术创新上,更凝结于一支行业经验平均超过20年的制药老将团队。
CEO GaneshKaundinya博士曾担任Momenta Pharmaceuticals的前CSO,主导了首个生物类似药的FDA批准,拥有麻省理工学院化工博士背景。CBO Greg Fralish是蓝鸟生物前肿瘤业务开发副总裁,主导过超10亿美元的合作项目,拥有佐治亚大学生物化学博士学位,在业务开发和项目合作方面具有丰富经验。
CSO Tanmoy Ganguly博士曾担任BD Biosciences研究负责人,拥有25年免疫疗法研发经验,主导了降解剂技术从概念到动物验证的全过程。此外,公司的科学顾问委员会阵容同样强大,团队包括诺奖得主领衔的糖生物学专家,为平台的底层创新提供了坚实的学术和技术支持。
04
从阻断到根除,平台技术多领域延伸
GlycoEra未来还需跨越双重关键挑战:首先是临床转化风险,虽然在动物模型中该技术实现了>95%的致病蛋白清除率,但这一效果能否在人体中成功复现仍是未知数;其次是生产放大量产问题,一步法生产工艺的批次均一性需要经过工业化验证,以确保药物生产的稳定性和质量可控性。
针对这些挑战,GlycoEra制定了清晰的战略应对方案:短期目标是在2026年前将首个针对IgG自身抗体的降解剂推进至I期临床,开启人体试验阶段;中期计划通过合作开发非自免领域靶点,如阿尔茨海默症β淀粉样蛋白,拓展技术应用场景,实现平台价值的多元化释放。
GlycoEra的治疗理念是从过去与疾病蛋白“共存”转向主动“根除”。正如公司CEO Ganesh Kaundinya博士所强调的:“这不仅仅是新药的开发,更是治疗范式的转变——从传统的‘阻断’治疗走向‘清除’的治疗模式。”
随着其平台技术向神经科学、肿瘤学等更多领域延伸,人类或许可以不再承受广谱免疫抑制等传统疗法的负面影响,取而代之的是对致病蛋白的精准靶向清除。
如果您想对接文章中提到的项目,或您的项目想被动脉网报道,或者发布融资新闻,请与我们联系;也可加入动脉网行业社群,结交更多志同道合的好友。

近
期
推
荐



