近年来,以司美格鲁肽(semaglutide)和替尔泊肽(tirzepatide)为代表的GLP‑1 受体激动剂类药物,凭借强效的减重与代谢改善作用,彻底改写了全球超重与肥胖的治疗格局,成为全民热议的 “减肥神药”。
但在临床与真实使用场景中,一个普遍又令人困惑的问题始终存在:同样剂量、同样药物,有人轻松减重超 20%,有人却不足 5%;有人几乎无不适,有人却被恶心、呕吐等副作用严重困扰。这种巨大的个体差异究竟从何而来?
近日,发表于国际顶级期刊Nature的一项大规模研究给出了关键答案——基因差异。
在题为“Genetic predictors of GLP1 receptor agonist weight loss and side effects”的研究中,来自23andMe研究所等机构的团队,对27,885名使用GLP‑1类药物的受试者开展了全基因组关联分析(GWAS),首次从遗传学层面精准锁定了决定药物减重疗效与副作用风险的核心基因变异,为GLP‑1减肥药物的个体化使用提供了里程碑式的科学依据。
研究团队首先聚焦减重疗效的遗传调控,结果显示,GLP1R基因上的一个错义变异rs10305420(p.Pro7Leu)与减重效果呈现极强的关联性。该位点每携带一个效应等位基因,就可额外实现约0.76 kg的体重下降,且效应以加性方式稳定存在,这一结果在独立的 All of Us 队列中得到成功验证。
这意味着,GLP1R作为GLP‑1类药物的直接作用靶点,其天然遗传变异,是导致不同人用药后减重效果天差地别的核心原因。
更重要的是,该变异在不同人群中存在频率差异,在欧洲与中东人群中更常见,在非洲人群中则最低,这也在一定程度上解释了不同族裔对药物反应的客观差异。
在副作用方面,研究同样发现了清晰的遗传规律,恶心、呕吐这两类最常见的不良反应,同样受基因严格调控。
团队首先在GLP1R基因区域定位到与恶心、呕吐显著相关的变异位点,且这些信号与减重疗效信号高度共定位,提示减重效果更好的人群,往往也更容易出现恶心、呕吐。
而另一项关键发现极具临床指导意义:GIPR基因上的错义变异rs1800437(p.Glu354Gln)与呕吐风险高度相关,且呈现严格的药物特异性。该关联仅出现在使用替尔泊肽的人群中,在使用司美格鲁肽的人群中完全不存在。
这是因为替尔泊肽是GLP‑1R/GIPR双靶点激动剂,而司美格鲁肽仅作用于GLP‑1R,GIPR的功能缺陷会削弱其对GLP‑1通路所致恶心的缓冲作用,进而升高呕吐风险,这一发现也为不同药物的副作用预判提供了精准的遗传依据。
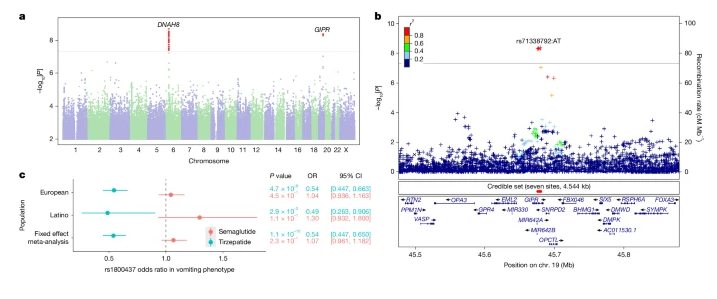
GLP-1药物副作用的遗传关联因素
基于上述核心遗传位点,结合年龄、性别、基线BMI、药物类型、用药时长、剂量以及2型糖尿病、高血压等临床指标,研究人员构建了整合遗传与非遗传因素的GLP‑1药物反应预测模型。
该模型不仅能有效解释约25%的减重差异,还能对恶心、呕吐的发生风险进行分层预测,在独立电子健康记录(EHR)数据中得到了良好验证。
数据显示,结合基因与临床特征后,个体用药后的体重下降幅度可从6%跨度至20%,中重度恶心或呕吐的发生风险可在5%至78%之间浮动,如此巨大的区间差异,直接证明“一刀切”的用药模式远非最优选择,而遗传信息正是实现精准用药的关键突破口。
这项研究最具突破性的意义在于,它首次提供了直接的遗传学证据,证实药物靶点基因的天然变异是GLP‑1类药物反应个体差异的重要来源,彻底打破了以往用药全靠“试错”、效果如同“开盲盒”的被动局面。
目前,23andMe已将这些研究成果整合进健康服务体系,通过基因信息结合年龄、病史等因素,为用户提供个性化的减重效果与副作用风险预测。
当然,现阶段并非所有人都需要先做基因检测再使用GLP‑1药物,但这项研究清晰地宣告:肥胖治疗的精准医学时代,已经从概念真正走向现实。
未来,一次简单的遗传筛查,就可能帮助使用者提前避开无效方案、规避高副作用风险,直接选择最适配自己基因的药物与剂量,让科学减重不再只依赖药物,更依赖基于基因的精准“计算”,在保证效果的同时,最大程度提升用药安全与舒适度。
[1]Su, Q.J., Ashenhurst, J.R., Xu, W. et al. Genetic predictors of GLP1 receptor agonist weight loss and side effects. Nature (2026). doi:10.1038/s41586-026-10330-z
