
近日,诺贝尔奖得主詹姆斯·罗斯曼(James Rothman)表示,人工智能对药物发现的影响令他深受启发。
詹姆斯·罗斯曼出生于1950年,1971 年在耶鲁大学获得物理学学士学位, 1976 年在哈佛大学获得生物化学博士学位。
他是耶鲁大学细胞生物学系系主任、纪念FergusF.Wallace生物医学教授。
因“揭示了细胞运输的精确控制机制”,即囊泡如何将大分子运出细胞体外,以便运输到达正确的目的地。
该研究彻底改变了人们对细胞组织方式以及细胞形成和分泌糖蛋白的方式的理解。
2013年,詹姆斯·罗斯曼与其他两位科学家获得诺贝尔生理或医学奖。如今这一发现是大火的“外泌体疗法”的开山之作。
如今,这位74岁的诺贝尔奖得主认为:人工智能在生物学和医学领域发挥了变革性作用,挑战了传统方法,并预示着药物发现理解和控制的新时代即将到来。
在近年来的一系列成果中,最让詹姆斯·罗斯曼感到震惊的是AlphaFold在预测蛋白质结构方面的精确度。
2020年,在第14届国际蛋白质结构预测竞赛(CASP14)中,AlphaFold2以惊人的表现力压一众模型摘得桂冠,刷新蛋白质三维结构预测的新高度。
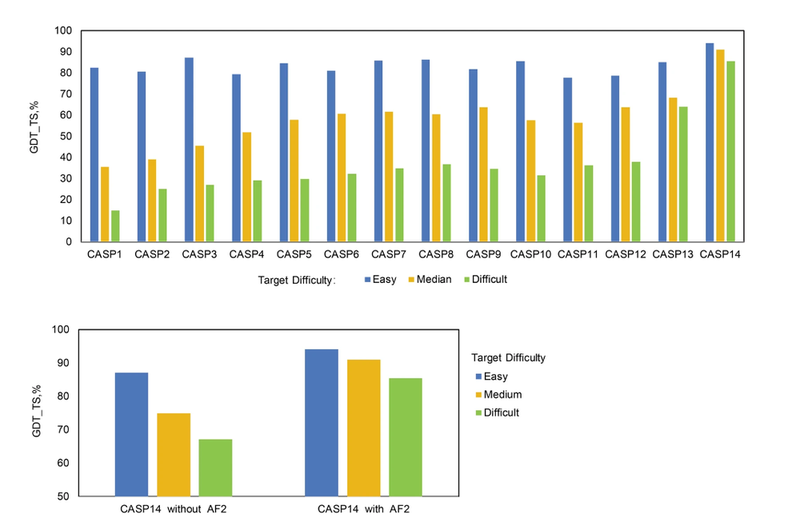
历届 CASP的得分与 AlphaFold 的得分
随后,DeepMind又用AlphaFold2预测了约2亿个蛋白质的结构,范围覆盖地球上几乎所有已知生物。

这些成果都让詹姆斯·罗斯曼认为,“以AlphaFold 为代表的人工智能技术开启了基础科学实验室和工业环境中发现的新时代。”
要知道,此前科研人员一直在用X射线晶体学和冷冻电镜这种耗时且成本高昂的实验技术解析蛋白质的结构。
AlphaFold已经成为为生命科学家和医学研究人员的一种革命性工具,该论文的被引量已经达到了2.3万。
对此罗斯曼表示,人工智能已经导致我们医学研究方法的范式转变。
如今AlphaFold2已经用于可应用于生物和医学的多个领域,包括结构生物学、药物发现、蛋白质设计、蛋白质-蛋白质相互作用、靶点预测、蛋白质功能预测、生物作用机制等(如蛋白质进化、罕见病治疗研究、突变对治疗的影响、疫苗设计)等。
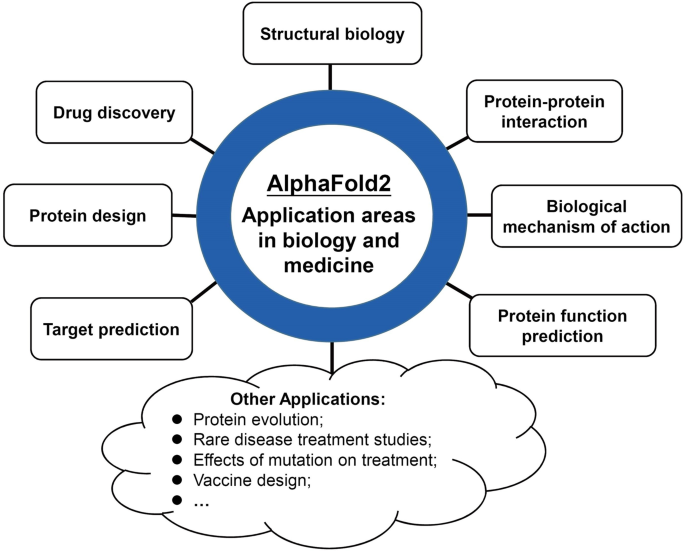
“人工智能挑战了传统观念,即对生物过程的完整理解对于有效干预至关重要。能够在没有详尽知识的情况下有效控制生物功能,标志着医学和药物发现的革命性方法。”罗斯曼说。
另外,关于AI算法黑箱的问题,詹姆斯·罗斯曼也表达了自己的看法。
"我认为人们并不真正了解它是如何工作的,尽管AI算法工程师知道怎么训练人工智能,但是归根结底,AI通过计算得出的结果中间,还有太多未知的东西。”
与很多人表示对AI+生物学的算法黑箱的忧虑不同,詹姆斯·罗斯曼却非常乐观。
由于研发的失败率非常高,人们都认为必须掌握基本的生物学和医学知识才能进行药物开发,但整个过程非常耗费成本和时间,一款药物的上市甚至经历了几十年。
在他看来,AI的出现或许表明,在生物学、医学以及药物发现中,人们不需要了解身体运作的所有原理,就能够有效地控制身体的运作方式。
如果AI能够在这方面发挥效用,那么这绝对是一个革命性的突破。
有意思的是,不少业内人士认为AlphaFold2是一项“诺奖级突破”。2023年,被誉为“诺奖风向标”的拉斯克奖就颁给了AlphaFold2的领导团队。
而AlphaFold后,AI+药物发现的下一步是什么?
或许DeepMind近期发布的AlphaFold3可以回答一部分答案。
AlphaFold3的重磅升级,将AI不再仅限于蛋白质结构预测,而是能够以前所未有的精度预测所有生命分子的结构和相互作用。
药物发现的关键不仅仅是了解蛋白质结构,而是实际设计与蛋白质表面结合的称为配体的药物化合物。知道它的结合位置以及结合强度,才能设计出正确的药物化合物。
因此,AlphaFold 3是朝着预测蛋白质配体结合以及这种相互作用如何发挥作用的方向迈出的一大步。
我们即将见证人工智能和生物学腾飞的十年。未来,机器学习模型将显著增强药物发现科学家的能力,高质量的预测将有望取代部分耗时耗力的湿实验分析。
然而,无论面临何种挑战,现在都是开启人工智能与医药的最佳时期。
—The End—