Chin Med:突破肝癌治疗瓶颈!中医药靶向肠道菌群-代谢-免疫轴,开辟肝细胞癌精准干预新路径
2026年4月12日
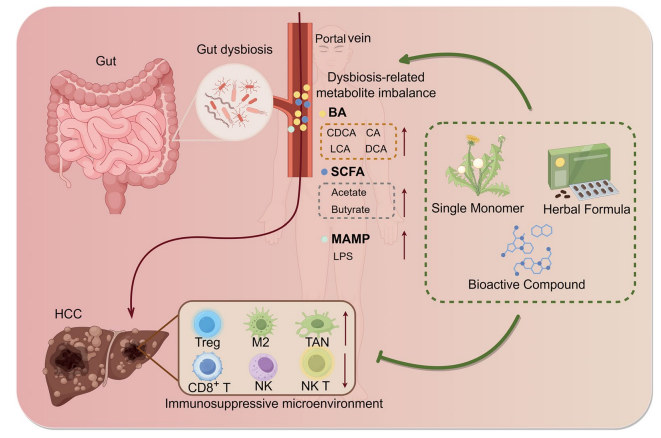
肝细胞癌(HCC)是全球高发的恶性肿瘤,其发病机制与肠道-肝脏轴功能紊乱密切相关。传统中医基于整体脏腑理论提出的相关理念,与现代“肠-肝轴”框架高度契合。近年来研究证实,肠道菌群-代谢-免疫轴的异常调控是HCC发生发展的核心病理环节,而中医药通过多靶点、多层面调控该轴稳态,为HCC治疗提供了全新视角,且相关研究已积累了丰富的临床与基础证据。肠道菌群-代谢-免疫轴的紊乱是HCC进展的关键驱动力。正常情况下,肠道菌群通过发酵膳食纤维产生短链脂肪酸(SCFAs)等有益代谢物,维持肠道屏障完整性并调节肝脏免疫平衡;而HCC患者普遍存在肠道菌群失调,表现为厚壁菌门与拟杆菌门比值升高,脱硫弧菌、大肠杆菌等促炎菌富集,双歧杆菌、 Akkermansia muciniphila等有益菌减少。这种失调会破坏肠道屏障功能,导致脂多糖(LPS)等病原体相关分子模式移位至肝脏,激活TLR4/NF-κB通路,促进肝星状细胞活化和慢性炎症,同时通过改变胆汁酸代谢、减少SCFAs生成,抑制CD8⁺T细胞、NK细胞功能,形成免疫抑制微环境,加速肿瘤进展。临床数据显示,BCLC C期患者的肠道菌群香农多样性指数显著低于A期,且血清脱氧胆酸(DCA)升高、干扰素-γ(IFN-γ)降低,提示该轴紊乱程度与HCC分期密切相关。中医药对HCC的干预作用,核心在于重塑肠道菌群-代谢-免疫轴的稳态。在肠道菌群调控方面,中药单体、复方及提取物均表现出明确效果:小檗碱可富集Akkermansia muciniphila等有益菌,抑制促炎菌生长;桃核承气汤通过调节肠道菌群组成,抑制肝星状细胞活化;麦冬多糖则能增加有益菌丰度,修复肠道屏障。更重要的是,肠道菌群可生物转化中药成分,增强其抗HCC活性,如肠道菌群将人参皂苷Rb1、Rd代谢为Compound K,将黄芩苷转化为黄芩素,后者的抑瘤效果显著优于原型成分。中医药还可通过调节代谢物水平和修复肠道屏障,进一步优化轴功能。 Yinchenhao decoction可使HCC小鼠促炎胆汁酸(DCA、TCA)降低30%-45%,升高抗炎胆汁酸(CDCA);小檗碱通过增加SCFA产生菌丰度,提升肠道乙酸、丁酸浓度,激活PPARδ通路诱导肝癌细胞凋亡。同时,Zn(II)-姜黄素固体分散体可使肠道紧密连接蛋白(occludin、ZO-1)表达升高1.8-2.3倍,减少LPS移位,减轻肝脏炎症。这些调控作用最终会重塑肝脏免疫微环境,如华蟾素多糖可抑制M2型肿瘤相关巨噬细胞极化,红花黄色素可促进CD8⁺T细胞肝脏浸润,增强 antitumor免疫。临床研究进一步证实了中医药的应用价值:一项多中心随机对照试验显示,华蟾素颗粒辅助治疗可使HCC术后2年无复发生存率从49.05%提升至62.39%;小檗碱6年随访研究表明其可有效预防HCC复发。但目前研究仍存在不足,如动物模型与人类HCC的物种差异、中医证候与菌群代谢表型的关联缺乏大样本验证等。未来需结合类器官共培养、单细胞多组学等技术,建立“中药-菌群-宿主”相互作用框架,优化靶向递送系统,推动中医药与免疫检查点抑制剂等疗法的协同应用。综上,肠道菌群-代谢-免疫轴是HCC病理机制的核心,中医药通过多维度调控该轴稳态,实现抑瘤、抗炎、免疫调节的综合效应,展现出独特的系统医学优势。随着研究的深入,中医药有望为HCC精准治疗提供新策略,推动形成具有中国特色的HCC综合治疗范式。
老中医(微信号:wxid_rszr95aw79ie22)