我们知道大脑是极其复杂的器官。我们的大脑里住着一群勤劳的星形胶质细胞。它们每天的主要工作之一,就是清理大脑中的代谢垃圾,维持神经系统的整洁与高效。
然而,当阿尔茨海默病来袭时,淀粉样蛋白这种有毒“垃圾”开始在大脑中疯狂堆积,形成顽固的斑块。这些斑块像路障一样,阻断了神经元的正常沟通,最终导致记忆衰退、认知功能丧失。
面对这些顽固的蛋白斑块,传统的单克隆抗体药物面临着重重挑战。它们通过静脉注射进入人体,艰难地穿过血脑屏障,然后标记出淀粉样蛋白,召唤大脑中的小胶质细胞来把它们“吃掉”。
这种方法虽然有效,但也存在明显短板:需要反复、高剂量给药,治疗窗口期狭窄,费用高昂,还可能引发脑水肿或出血等副作用。
那有没有一种办法,能让大脑自己的星形胶质细胞变得足够强大,能够自主识别并清除这些有毒“垃圾”呢?
给星形胶质细胞装上“GPS”
近期,来自华盛顿大学医学院的研究团队发表于Science的一项重磅研究试图回答了这个问题。研究团队从癌症免疫疗法中大名鼎鼎的“CAR-T”技术中汲取灵感,创造性地将其应用于阿尔茨海默病的治疗。
他们首次开发出一种被称为“嵌合抗原受体星形胶质细胞(CAR-A)”的细胞疗法。简单来说,这种细胞疗法利用基因工程技术,对大脑中原本就存在的星形胶质细胞进行改造,让它们获得类似“导航系统”的能力,可以专门识别并清除β淀粉样蛋白。
并且,这种疗法在动物实验中表现出惊人的效果:只需一次静脉注射,这些改造后的细胞便能够进入大脑并持续发挥作用,显著降低淀粉样蛋白斑块的负担。
DOI:10.1126/science.ads3972
在肿瘤治疗领域,CAR-T技术是指从患者体内提取T细胞,在体外给它们装上能够识别癌细胞的“GPS”(即嵌合抗原受体,CAR),然后大量扩增后再输回患者体内,让这些改造后的T细胞去精准追杀癌细胞。
受此启发,研究团队提出了一个大胆的设想:能否给大脑中的星形胶质细胞也装上类似的“GPS”,让它们能够主动识别并吞噬淀粉样蛋白?他们将这种改造后的细胞命名为“CAR-A”,即表达嵌合抗原受体的星形胶质细胞。
给星形胶质细胞装上四种“GPS”
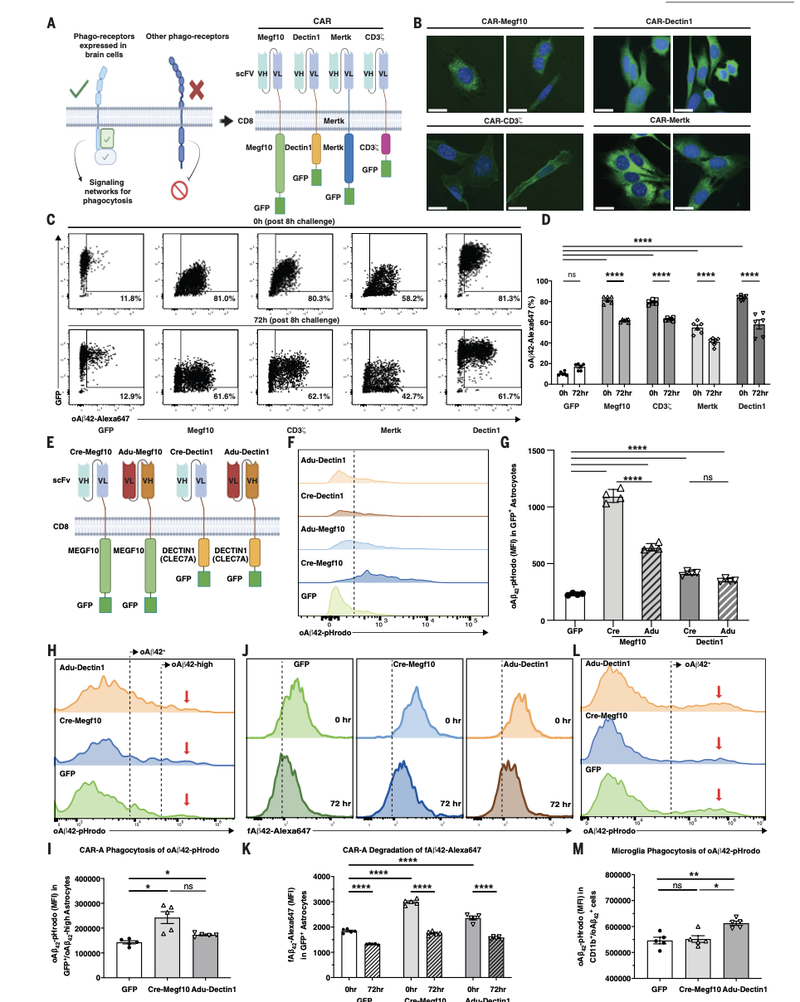
研究的第一步,是在体外验证这个设想是否可行。研究人员设计了四种不同的CAR-A。每个CAR-A都包含两个核心部分:一个是可以识别并结合淀粉样蛋白的“探针” ,另一个是可以激活星形胶质细胞吞噬功能的“信号开关”。
结果,当这四种CAR-A被表达在星形胶质细胞表面后,无论是永生化的小鼠星形胶质细胞系,还是原代培养的小鼠星形胶质细胞,其吞噬淀粉样蛋白的能力都得到了显著增强。其中,两种CAR-A的表现尤为突出:一种是Cre-Megf10,另一种是Adu-Dectin1。
体外实验的成功为后续研究注入了强心剂。但大脑有血脑屏障这道天然防线,如何将这些改造后的“基因指令”安全、高效地递送到大脑里的星形胶质细胞中呢?
接下来,研究人员巧妙地利用了AAV-PHP.eB这个经过工程化改造的病毒载体。这种载体有个“特技”,它能够通过静脉注射后,高效地穿越血脑屏障,并将携带的基因指令递送到中枢神经系统的细胞中。
于是,研究人员将装载有Cre-Megf10或Adu-Dectin1基因指令的AAV-PHP.eB病毒,通过一次性静脉注射的方式,送入了阿尔茨海默病模型小鼠(5xFAD小鼠)的体内。病毒入血,穿越血脑屏障,找到星形胶质细胞,精准递送基因指令。接收到指令的星形胶质细胞,开始在自身表面组装这些特制的“GPS”。
星形胶质细胞靶向Aβ的CAR设计与体外验证
一场“大脑清洁战”
改造完成后,就到了检验实战效果的时刻。研究人员设计了两套作战方案。
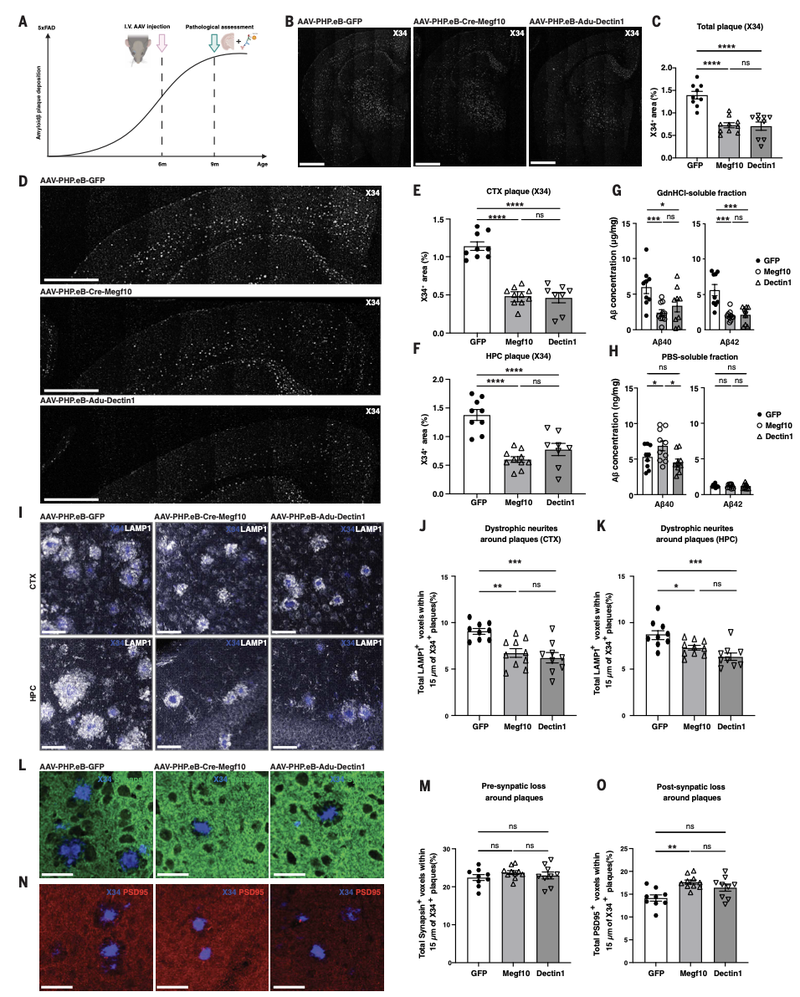
第一套方案是“后期干预”,即在6月龄、小鼠大脑中已形成大量淀粉样斑块时,才给它们注射CAR-A病毒。3个月后(小鼠9月龄时)的检测结果表明,无论是接受了Cre-Megf10还是Adu-Dectin1治疗的小鼠,其大脑中的淀粉样斑块总量都减少了约50%。在皮层和海马这两个关键脑区,斑块的减少同样显著。
进一步的生化分析也证实,不可溶的、有毒的Aβ42蛋白数量大幅下降。伴随斑块的清除,神经元周围受损的轴突和树突(即神经炎性营养不良)也明显减轻。
星形胶质细胞CAR体内晚期干预效果
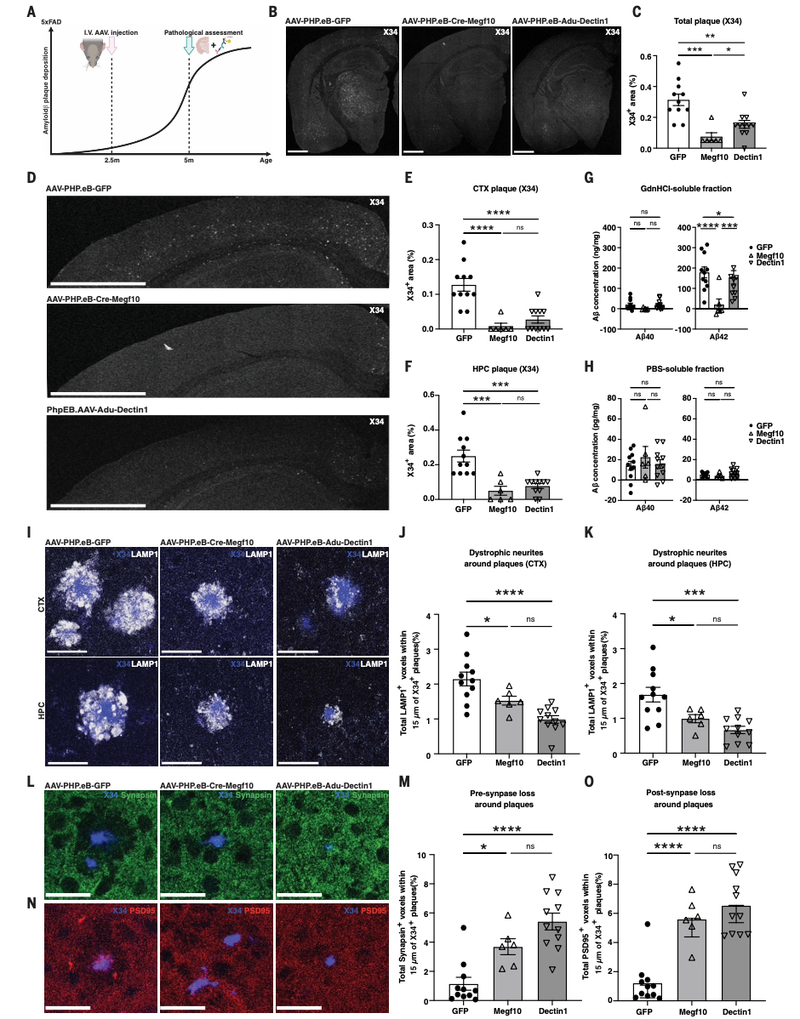
第二套方案是“早期预防”,即在2.5月龄、小鼠大脑中尚未出现淀粉样斑块时,就提前进行CAR-A干预。等到小鼠长到5月龄,也就是斑块刚开始形成的时候,再进行检查。结果,接受了Cre-Megf10治疗的小鼠,大脑中几乎看不到任何淀粉样斑块的踪影。
星形胶质细胞CAR体内早期干预效果
被重塑的“大脑免疫微环境”
斑块减少了,那么大脑中负责清理垃圾的“微环境”发生了怎样的变化呢?为了回答这个问题,研究人员对小鼠大脑海马区的细胞进行了单细胞核RNA测序。
他们发现,两种CAR-A都成功地激活了疾病相关星形胶质细胞。这些被激活的星形胶质细胞,积极地向斑块周围聚集,并上调了LRP1这种能结合并清除淀粉样蛋白受体的表达。
不仅如此,CAR-A还间接地影响了小胶质细胞的状态。在阿尔茨海默病中,小胶质细胞长期处于过度激活状态,最终会走向“耗竭”。而经过CAR-A治疗后,这些耗竭的小胶质细胞比例显著下降,取而代之的是一类全新的、高表达CSF1R和CD68的细胞群体。这个新群体既保留了部分“稳态”特征,又具备更强的吞噬活性。
为何行为未见改善?
尽管病理层面的改善令人鼓舞,但一个关键问题依然悬而未决:这些显著的病理改变,能转化为小鼠行为能力的提升吗?遗憾的是,在本次研究中,无论是早期干预还是晚期干预组,研究人员都没有观察到治疗组小鼠在记忆相关行为学测试(如Y迷宫、条件恐惧实验)中的显著改善。
他们对此提出了几种可能的解释。首先,AAV病毒载体本身或CAR的过度激活,可能引起了一些轻微的运动功能改变或副作用,干扰了行为学测试的结果。其次,增强的吞噬功能可能在清除淀粉样蛋白的同时,也“误伤”了部分重要的神经突触,从而抵消了病理改善带来的益处。
总的来说,这项研究首次证明了,通过一次性、非侵入性的静脉注射,将携带抗淀粉样蛋白嵌合抗原受体的基因工程病毒递送到大脑,改造常驻的星形胶质细胞,使其能够持久、高效清除淀粉样蛋白斑块,这一策略在阿尔茨海默病小鼠模型中是可行的。
当然,从实验室走向临床应用,还有很长的路要走。如何进一步优化CAR的设计,在增强清除效率的同时,避免对正常神经环路的干扰?如何寻找更安全的递送载体,以规避AAV病毒可能带来的副作用?这些都是摆在研究者面前的新课题。
[1]Chen Y, Liu Y, Nguyen K, Wu J, Song S, Lin K, Rodrigues PF, Du S, Zhou C, Xiong K, Bosch M, Lin PB, Khantakova D, Wu S, Wu M, Yuede C, Holtzman DM, Colonna M. Targeting amyloid-β pathology by chimeric antigen receptor astrocyte (CAR-A) therapy. Science. 2026 Mar 5;391(6789):eads3972. doi: 10.1126/science.ads3972. Epub 2026 Mar 5. PMID: 41785364.
