前言
CDK4/6抑制剂作为激素受体阳性(HR+)乳腺癌治疗的里程碑药物,显著延长了患者的无进展生存期(PFS),但其耐药性问题逐渐成为临床治疗的“阿喀琉斯之踵”。据统计,约30%-40%的转移性乳腺癌患者最终会对CDK4/6抑制剂产生耐药性,导致疾病进展。耐药机制不仅涉及细胞周期调控异常,还与肿瘤微环境重塑、表观遗传改变及信号通路代偿激活密切相关。因此,深入了解癌症中CDK4/6信号传导的关键方面及其对靶向疗法的反应,有助于我们解析CDK4/6抑制剂的耐药性挑战并寻找应对策略。
-01-
CDK4/6的生物学功能
CDKs包含一个丝氨酸-苏氨酸激酶家族,通过结合细胞周期蛋白伴侣被催化激活,并调节基本的生物过程。尽管每种CDK的具体细胞功能尚未完全阐明,但它们可以大致分为细胞周期进程的调节因子(CDK1、CDK2和CDK4/6)和转录相关激酶(CDK7、CDK8、CDK9、CDK12和CDK13)。细胞周期进程受CDK及其相应细胞周期蛋白在特定细胞周期阶段的不同复合物的顺序表达和激活的调节,导致细胞周期事件发生所必需的特定底物的协同磷酸化。
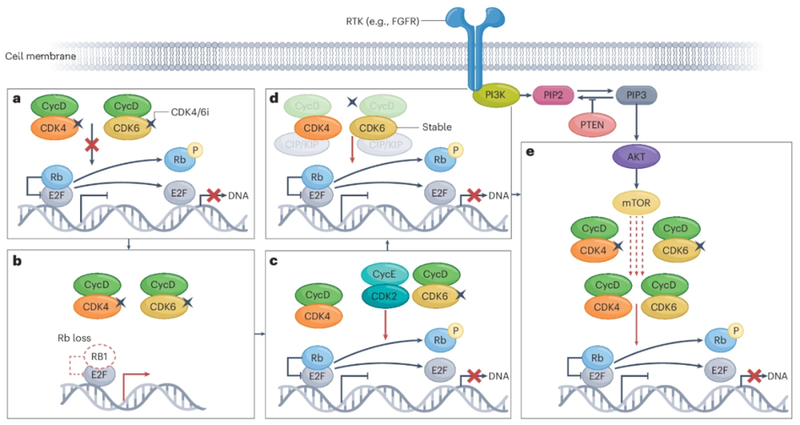
CDK4/6是高度同源的激酶,与细胞周期蛋白D家族形成复合物,通过磷酸化Rb肿瘤抑制因子促进G1至S期细胞周期转换,从而缓解转录因子E2F1的抑制。E2F转录因子与Rb的解离导致E2F的核定位以及随后与细胞周期进展相关的基因的转录。已发现CDK4/6-Rb-E2F通路的成分在癌症中经常失调,包括Rb表达的缺失或下调、CDK4或CDK6扩增或过表达、INK4蛋白和细胞周期蛋白D1或细胞周期蛋白D3扩增或过表达。美国食品药品监督管理局(FDA)已批准四种CDK4/6抑制剂(palbociclib、ribociglib、abemaciclib和triracilib)用于癌症治疗。