引言:免疫代谢与B细胞的核心地位
免疫反应和自身耐受对于维持系统和组织稳态至关重要。自身免疫病源于针对自身抗原的失控免疫反应,而癌症则发生在免疫反应未能抑制恶性细胞生长和扩散时。在自身免疫和癌症中,免疫细胞都会经历改变其功能的代谢转变,反之,改变的细胞功能也构成了代谢重编程的基础。理解免疫细胞在特定病理环境中所经历的代谢变化,有助于研究人员开发新的策略来重编程改变的细胞功能。
B细胞在自身免疫和癌症中都具有重要作用,因此可能成为治疗干预的宝贵靶点。作为适应性免疫的关键组成部分,B细胞能够产生广泛的抗体谱并分泌促炎细胞因子,以帮助清除外来抗原和癌细胞。B细胞还被发现通过细胞间接触机制和/或产生抗炎细胞因子(包括IL-10、IL-35和TGF-β)来抑制不受控的炎症反应,从而有助于免疫调节。因此,更全面地理解B细胞免疫代谢、发病机制和疾病进展之间的关系,有助于开发重编程和重构B细胞代谢与功能的治疗策略。
-02-
一、B细胞在发育、激活和分化过程中的免疫代谢
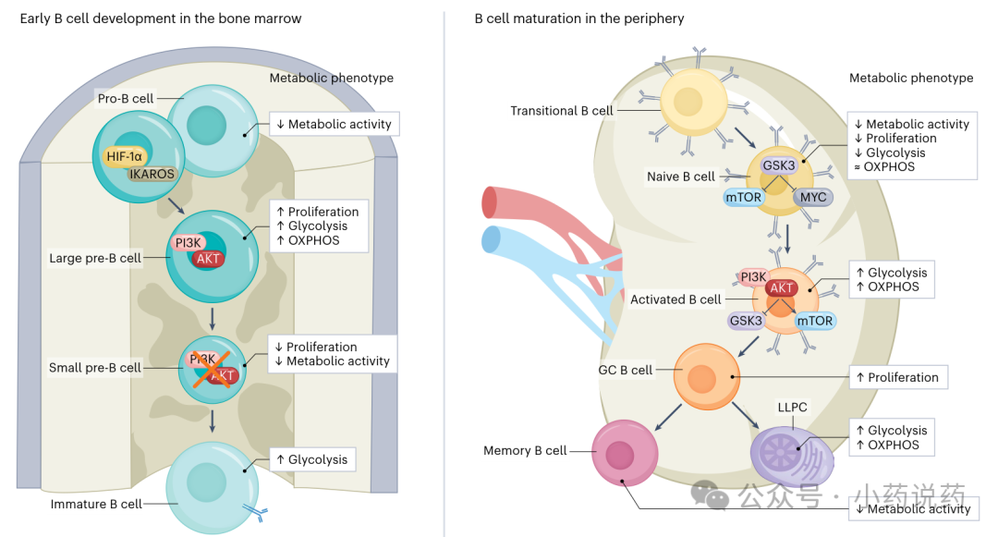
1. 骨髓中的B细胞发育与外周B细胞成熟
B细胞在其整个生命周期中在静息和高代谢活性之间循环。在骨髓中发育时,祖B细胞表现出最小的增殖,以确保基因组稳定性。成功的基因重组导致前B细胞受体产生,驱动祖B细胞分化为大前B细胞。前BCR信号传导增加胞质钙水平,导致增殖增加。在此阶段,IL-7促进磷脂酰肌醇3-激酶-AKT通路激活,增强糖酵解和氧化磷酸化,从而支持细胞增殖、葡萄糖摄取和活性氧产生。
随后,大前B细胞变为小前B细胞,其中PI3K-AKT通路失活,导致增殖和代谢活性降低。在骨髓早期发育过程中,B细胞经历由保守的代谢调节因子控制的代谢变化,包括缺氧诱导因子-1α、PAX5和IKAROS。HIF-1α通过上调葡萄糖转运蛋白和磷酸果糖激酶3的表达来驱动祖B细胞向前B细胞的转变。PAX5通过抑制谱系不适当基因的转录同时激活B细胞特异性基因,确保共同淋巴祖细胞定向于B细胞谱系。IKAROS通过诱导编码前BCR信号转导蛋白的基因表达并抑制抑制前BCR信号传导的基因转录,促进祖B细胞向前B细胞的转变。
随后,小前B细胞通过提高糖酵解速率分化为未成熟B细胞。未成熟B细胞从骨髓迁移到脾脏,在那里进一步分化为过渡B细胞,进而产生成熟的初始B细胞。成熟初始B细胞库包括两个亚群,B1和B2细胞。B1细胞比B2细胞具有更高的糖酵解速率。B1细胞表现出较高的基础耗氧率,表明其具有强大的氧化磷酸化、磷酸戊糖途径活性和增加的脂肪酸合成。相比之下,初始B2细胞的特点是增殖率和糖酵解活性低,具有中等水平的氧化磷酸化。这种状态由糖原合酶激酶3维持,它通过抑制哺乳动物雷帕霉素靶蛋白和MYC来减弱细胞生长、代谢活性和增殖。
总之,B细胞发育过程中代谢重编程和转录调控之间的动态相互作用确保了其通过不同的成熟阶段。这种严格控制的代谢回路保持了B细胞的谱系定向,并构成了免疫反应功能完整性的基础。
2. B细胞激活
成熟B细胞可以通过T细胞依赖方式(通过BCR结合和共刺激信号)或T细胞非依赖方式(如通过Toll样受体)被激活。在这两种情况下,PI3K-AKT通路均被激活,从而促进向糖酵解的转换。具体而言,在BCR或TLR刺激后,PI3K-AKT信号传导促进葡萄糖摄取,为糖酵解途径和三羧酸循环提供燃料。这导致糖酵解和氧化磷酸化大幅增加,以在细胞激活后维持增殖和功能活动。在活化的B细胞中,增加的细胞内葡萄糖水平提供了细胞扩增所需的生物分子。在抗体分泌细胞中,B细胞激活后磷酸戊糖途径活性增加,以支持核苷酸生物合成。增加的脂肪酸氧化和谷氨酰胺分解提供了为三羧酸循环提供燃料的中间体。
B细胞激活由细胞因子BAFF促进,它支持细胞存活和代谢适应,从而促进抗原反应。从机制上讲,BAFF-BAFF受体信号传导导致PI3K-AKT通路激活,进而磷酸化控制细胞存活和代谢能力的AKT靶基因。
T细胞依赖性和非依赖性激活之间的一个主要区别在于信号的自我维持能力。特别是,TLR介导的激活足够强大,可以维持B细胞存活和增殖,而仅BCR激活则导致B细胞凋亡。BCR激活的B细胞需要在激活后24小时内获得第二个信号才能存活,否则细胞内ROS和钙会积累,导致线粒体功能障碍。
激活后,滤泡B细胞可以进入淋巴滤泡,分化为滤泡外浆细胞和记忆B细胞,或形成生发中心,产生长寿浆细胞和长寿记忆B细胞。它们向滤泡外或GC表型的分化取决于PI3K信号的强度。PI3K-AKT-mTOR通路的不均衡转导驱动同源B细胞走向两种命运:强信号传导导致滤泡外浆细胞分化,而弱信号则将B细胞导向GC表型。
3. 滤泡外与生发中心反应
从分化角度看,GC反应产生长寿浆细胞和长寿记忆B细胞。在长寿浆细胞中,持续的葡萄糖和氨基酸摄取提供了支持增加的糖酵解和氧化磷酸化的底物。葡萄糖尤其被用于抗体糖基化和丙酮酸生产,以为氧化磷酸化提供燃料。核苷酸生物合成升高以满足这些细胞增加的代谢需求,并且自噬衍生的营养物质被分解代谢并用于ATP产生。
长寿记忆B细胞的代谢在很大程度上仍然未知,尽管认为这些细胞比长寿浆细胞代谢活性更低。在再次暴露于其同源抗原后,记忆B细胞迅速改变其代谢,通过mTOR激活和AMPK抑制之间的受控平衡,以及糖酵解和氧化磷酸化的参与,实现浆细胞分化。
-03-
二、B细胞恶性肿瘤中的免疫代谢
骨髓中的祖细胞可以产生B细胞急性淋巴细胞白血病,这是一种常以B细胞特异性转录因子替换为特征的淋巴样恶性肿瘤。PAX5的替换常导致葡萄糖摄取和糖酵解增加。在体外将PAX5重新表达于前B-ALL细胞中可减少葡萄糖摄取和ATP消耗,表明该代谢通路可能是克服B-ALL患者耐药性的靶点。
慢性淋巴细胞白血病起源于过渡性或初始B细胞,其代谢谱因其解剖定位而异。循环中的CLL B细胞以线粒体质量增加以及线粒体呼吸增强为特征,表明其代谢主要依赖于氧化磷酸化。还观察到ROS积累和氧化应激。然而,大多数CLL B细胞在CLL淋巴结中增殖,在那里它们的增殖通过与树突状细胞、T细胞和细胞因子的接触以及BCR结合得到支持。在这种环境中,B细胞表达高水平的MYC,促进糖酵解活性和氧化磷酸化。
另一种常见的淋巴瘤类型,弥漫性大B细胞淋巴瘤,在近一半病例中存在MYC突变。DLBCL根据不同的标准分为几个亚型。根据细胞起源可以区分生发中心B细胞DLBCL和活化B细胞DLBCL。在GCB-DLBCL中,细胞的转录组特征类似于GC明区B细胞;在ABC-DLBCL中,B细胞类似于用抗BCR和CD40连接在体外激活的细胞,并且需要BCR信号传导以进行增殖,随后糖酵解通路上调。
第二种分类基于B细胞的代谢谱:它包括OXPHOS-DLBCL、BCR-DLBCL和宿主反应DLBCL。OXPHOS-DLBCL B细胞显示线粒体代谢增加,营养来源的碳掺入三羧酸循环,谷胱甘肽水平升高,活跃的mTOR信号传导和谷氨酰胺分解,以及糖酵解酶甘油醛-3-磷酸脱氢酶的低表达。在BCR-DLBCL中,B细胞以细胞周期基因上调为特征,并且更依赖于有氧糖酵解。
套细胞淋巴瘤是另一种侵袭性B细胞淋巴瘤,以BCR信号通路激活为特征。使用依鲁替尼抑制布鲁顿酪氨酸激酶已被证明有效。PI3K-AKT-mTOR信号通路在依鲁替尼耐药套细胞淋巴瘤的细胞生长和增殖调控中起主要作用。在临床前模型中,同时靶向mTOR和exportin 1通过抑制三羧酸循环和糖酵解有效降低了套细胞淋巴瘤细胞生长。另一组研究表明,依鲁替尼耐药是由于癌细胞通过谷氨酰胺分解和氧化磷酸化进行代谢重编程。使用临床可用的分子IACS-010759抑制氧化磷酸化可在体外和来自癌症患者的依鲁替尼耐药细胞中减少癌细胞生长。
最后,B细胞的最后一个分化步骤也有恶性对应物:多发性骨髓瘤,其特征是骨髓中浆细胞的失控扩增。这些恶性细胞高度依赖葡萄糖和谷氨酰胺代谢,类似于浆细胞的代谢特征。然而,它们的代谢可以被肿瘤微环境重编程为氧化磷酸化,从而促进耐药表型。
-04-
三、肿瘤微环境中的B细胞免疫代谢
在肿瘤进展过程中,癌细胞调整其代谢以满足增加的生物合成和生物能量需求,以维持细胞存活和增殖。结果,营养物质被耗尽,代谢废物产物在肿瘤微环境中异常积累。这导致周围免疫细胞的免疫代谢改变。在TME中,多种因素可能影响B细胞代谢。
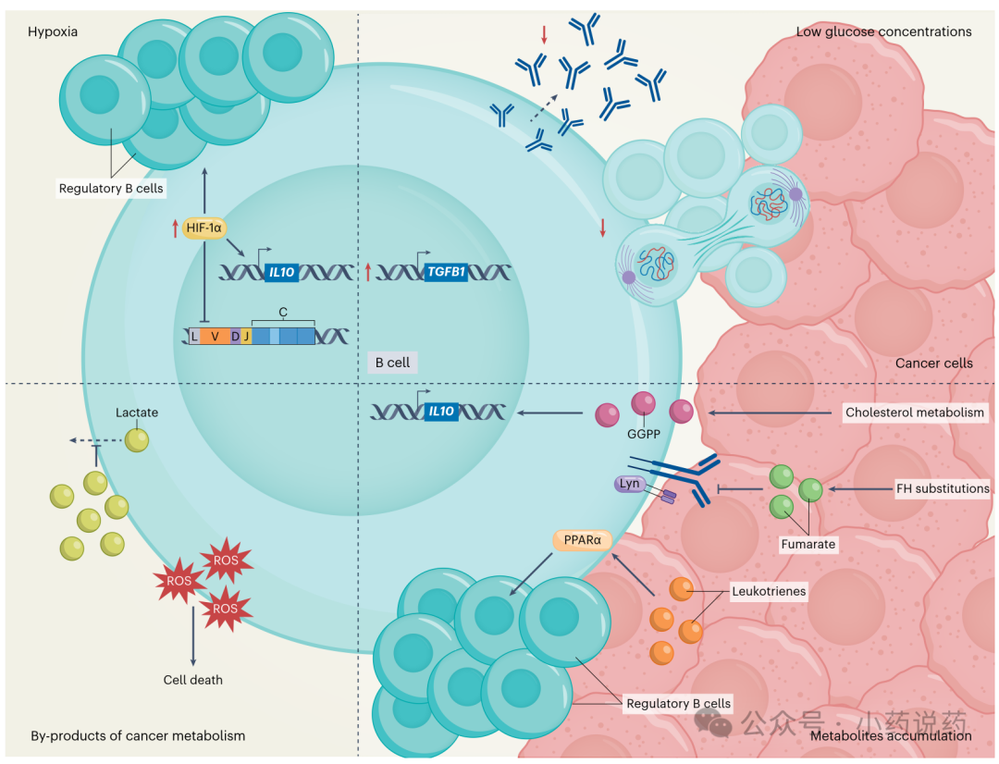
TME中的营养竞争是实体瘤的一大标志。快速增殖的癌细胞消耗大量营养物质,使免疫细胞饥饿并阻碍其功能。在B细胞中,葡萄糖和谷氨酰胺是基本的能量来源。TME中的葡萄糖剥夺会损害B细胞代谢,阻碍B细胞分化为产生IgG的浆细胞。
具体而言,在葡萄糖饥饿的B细胞中,介导STAT6与胚系Cγ基因启动子结合的AT富集序列结合蛋白-1的下调导致IgG产生减少。在葡萄糖耗尽的条件下,谷氨酰胺可以作为替代碳源,但在TME中常常稀缺。在B细胞中,谷氨酰胺耗竭会损害记忆和浆细胞分化,因此,TME中的谷氨酰胺缺乏,类似于葡萄糖缺乏,可能抑制B细胞对肿瘤的反应。
TME中代谢物的积累可以改变代谢和免疫功能。在癌细胞中,胆固醇代谢常常增加,并且TME中胆固醇衍生代谢物的积累会抑制免疫反应。在人B细胞中,胆固醇前体香叶基焦磷酸可以诱导IL-10产生。香叶基香叶基依赖性修饰控制PI3Kδ-AKT-GSK3通路的激活,促进B淋巴细胞诱导成熟蛋白-1依赖性IL-10表达。几种肿瘤以编码三羧酸循环酶的基因突变为特征,包括延胡索酸水合酶。突变型FH导致延胡索酸积累,后者抑制BCR下游的酪氨酸激酶Lyn。在B细胞中,通过FH抑制剂或外源性补充导致延胡索酸积累会急剧抑制B细胞体外激活和功能。
除了代谢物外,肿瘤代谢的副产物,如乳酸,会因有氧糖酵解增加而在TME中积累。由于乳酸通过单羧酸转运蛋白的流动取决于间质和胞质之间的梯度,TME中乳酸水平的增加可能影响肿瘤浸润细胞(包括B细胞)的乳酸分泌,酸中毒已被证明对T细胞有影响。此外,研究表明酸中毒通过可能潜在地影响免疫细胞的机制介导多种细胞系中的mTOR抑制。
最后,作为线粒体代谢副产物的ROS在TME中的积累可导致B细胞死亡,损害体液反应。总之,尽管TME中B细胞的代谢需要进一步研究,但B细胞和癌细胞之间的代谢串扰可以被靶向以调节B细胞对抗肿瘤的活动。
-05-
四、自身免疫性疾病中的B细胞免疫代谢
免疫代谢学研究日益突出了B细胞代谢在导致自身免疫性疾病致病事件中的关键作用。B细胞代谢检查点功能障碍和B细胞对BAFF暴露增加已被证明是系统性红斑狼疮中耐受缺陷的主要机制。SLE患者BAFF水平升高,过表达BAFF的转基因小鼠表现出多克隆高丙种球蛋白血症、高水平的抗双链DNA自身抗体以及肾脏中免疫球蛋白积累。BAFF破坏B细胞中的葡萄糖稳态并激活ERK1-ERK2通路,促进糖酵解、增强细胞增殖并挽救自身反应性B细胞。B细胞还具有增强的依赖于CD36的线粒体呼吸,敲除CD36可抑制小鼠狼疮模型中的自身反应性并减少自身抗体产生。
年龄相关B细胞是一群表达T-BET、CD11c和CD11b的记忆B细胞,在自身免疫性疾病患者和SLE、类风湿关节炎、多发性硬化症及常见变异型免疫缺陷的小鼠模型中增加。年龄相关B细胞以MHC-II和T细胞共刺激分子的高表达为特征;在狼疮易感小鼠中,这些细胞表现出对2-NBDG的摄取增强以及与野生型小鼠相比线粒体激活增加,表明自身免疫环境在塑造其代谢中起作用。在RA中,类风湿因子和抗瓜氨酸化蛋白抗体的存在表明自身反应性B细胞的激活。在佐剂性关节炎大鼠中,抑制糖酵解可改善疾病,表明B细胞代谢在自身免疫性关节炎中起作用。
尽管关于B细胞的代谢最近才引起研究人员的兴趣,并且该领域的知识仍然有限,但已经有人在努力开发靶向和限制B细胞代谢作为治疗自身免疫的方法。
-06-
结语
大量证据表明多种疾病中存在各种免疫代谢失衡。在此背景下,越来越多的证据强调了B细胞及其改变的代谢状态在多种病理生理状况中的作用。这些代谢参与者可能代表新免疫疗法的共同靶点,这些疗法利用B细胞代谢来诱导更具反应性的B细胞以对抗癌症,或更好地控制其在自身免疫中的异常功能。因此,免疫代谢的靶向调节可能为治疗干预提供新的可能性。
参考文献:
B cell immunometabolism in health and disease. Nat Immunol. 2025 Mar;26(3):366-377.
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
