引言
随着抗体-寡核苷酸偶联药物(AOCs)从概念验证加速进入临床开发阶段,建立与之匹配的、严谨的质量控制体系并深刻理解其面临的临床转化挑战,已成为推动该领域成熟的关键。AOCs作为一种由大分子抗体与化学大分子寡核苷酸通过连接子共价结合而成的复杂实体,其结构异质性高,生产过程涉及多步合成与纯化。为确保最终产品的安全性、有效性和批次间一致性,必须建立一套从中间体到成品的全方位质量控制策略。其质量控制远非两者简单的叠加,而是需要对寡核苷酸-抗体比率(OAR)、偶联位点、游离杂质及生物活性等独特属性进行多维度的精准表征。
-02-
一、AOC的制造工艺
AOC制造通常涉及裸抗体、连接子、寡核苷酸、AOC散装溶液和AOCs的生产。基于质量源于设计和风险评估等原则的工艺设计和开发,指导生产过程中宿主细胞、培养基和试剂的控制。应全面管理与AOC组件制造过程相关的潜在杂质和病毒污染风险。应在工艺开发层面进行优化,以主动实现质量控制。
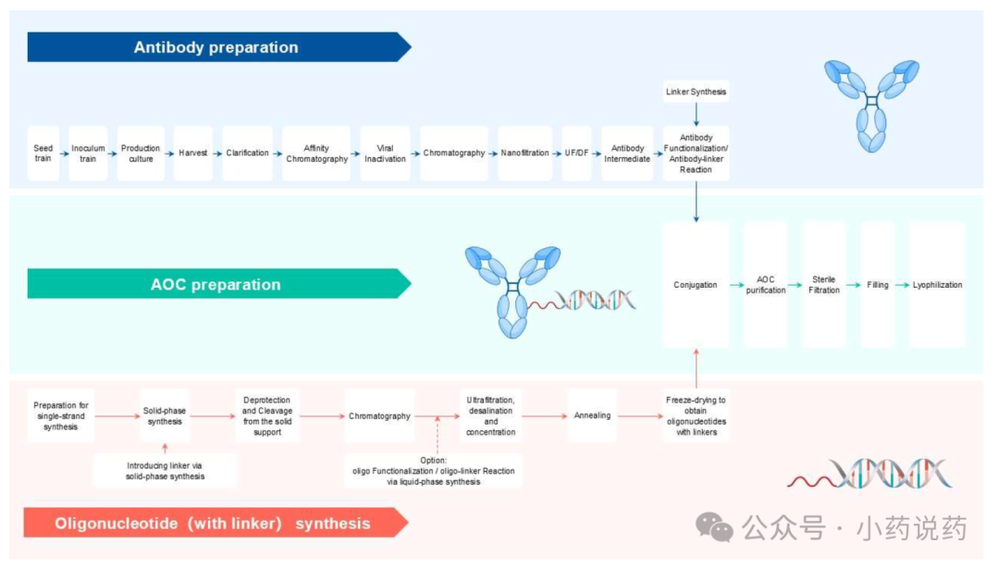
AOC生产材料包括制造材料、细胞基质、耗材和容器。制造材料涵盖起始物料、生产过程中使用或添加的材料、辅料和生产耗材。制造材料的质量与最终产品的质量、安全性和有效性密切相关,应在稳健和标准化的质量管理体系内使用风险评估原则进行控制。例如,当生产具有高疏水性的AOCs时,应特别注意AOC分子与灭菌滤膜之间潜在的非特异性结合,因此需要仔细选择合适的膜。
1. 单克隆抗体
单克隆抗体通常用于AOCs,mAbs的制造工艺与传统抗体治疗药物的制造非常相似。然而,由于为定点偶联设计的基因工程mAbs的修饰基团,生产工艺可能有所不同。因此,除了常规抗体生产的风险因素外,还必须解决AOC制造特有的风险因素。例如,在采用赖氨酸介导缀合的AOCs中,应注意裸抗体上N末端赖氨酸残基的水平以及裸抗体溶液中的氨基酸组成。在采用半胱氨酸介导偶联的AOCs中,必须监测裸抗体中的半胱氨酸变体,如具有二硫键和游离硫醇基团的半胱氨酸。在裸抗体溶液的开发过程中,应防止抗体降解和聚集。此外,与后续偶联工艺的兼容性将防止在AOC生产的后期阶段(包括缀合和制剂)产生不利影响。
典型的抗体生产过程包括细胞增殖、mAb表达、mAb纯化以及mAb修饰和功能化。在细胞增殖和蛋白质表达过程中,应控制关键的细胞培养参数。亲和层析通常用于mAbs的初步纯化。低pH处理通常用于病毒灭活;但是,如果产品在低pH条件下不稳定,则可以使用替代的病毒灭活策略。中间和精制纯化通常采用离子交换层析和疏水相互作用层析。使用层析方法(包括混合填充材料的层析)从蛋白质中去除工艺相关和产品相关杂质。大多数纯化工艺还结合了纳滤以去除对化学灭活具有抵抗力的小病毒。最后,通过超滤浓缩mAbs并交换缓冲液。细胞培养和纯化后,对抗体进行修饰以引入偶联所需的官能团。修饰过程根据偶联技术而异;主要目标是在抗体上引入反应性化学基团。例如,可以使用还原剂切割二硫键并生成反应性游离硫醇基团。可以通过糖基的酶修饰引入反应性官能团。抗体修饰是决定AOCs中寡核苷酸负载能力和分布的关键步骤。因此,必须基于特定的偶联技术和修饰开发合适的制造工艺,并建立合理的中间过程控制策略。如果需要纯化修饰后的裸抗体,则应实施适当的纯化工艺。如果修饰过程中使用的试剂引入了外源性病毒污染物,则必须在纯化过程中去除这些污染物。应根据国际人用药品注册技术协调会(ICH)Q5A指南进行病毒清除研究。如果将修饰后的裸抗体作为中间体管理,则必须建立质量标准,并且必须进行稳定性研究以确定保质期。对于需要定点缀合的AOCs,mAb修饰过程中的还原和再氧化条件尤为关键。抗体修饰中的关键工艺参数包括试剂类型、接触时间、试剂浓度和温度。
2. 连接子
AOCs合成中采用两种类型的连接子。含连接子的亚磷酰胺单体和含有两个偶联基团的连接子。含连接子的亚磷酰胺单体应根据适用于治疗性寡核苷酸合成中用作起始物料的单体的控制标准进行开发和制造。含有两个偶联基团的连接子可以根据适用于常规小分子活性药物成分的标准进行开发。应为连接子制造过程中使用的中间体、关键起始物料和试剂建立质量控制标准。当原材料或中间体中的杂质与最终产品的关键质量属性相关时,必须验证在制造过程中去除此类杂质或其衍生物。如果工艺涉及过滤器的重复使用,应注意过滤器的使用寿命和清洁方法,并进行相关研究。对于含有手性中心的连接子,应评估手性对AOC产品生物活性的影响,并适当控制手性杂质。连接子的关键质量属性应通过基于其对AOC缀合工艺以及最终产品安全性和有效性的潜在影响的风险评估来确认。
3. 寡核苷酸
目前寡核苷酸活性药物成分的工业生产采用以单体为原料的固相合成。合成过程在固相支持物上启动,该支持物可能预装载有递送配体。使用固相合成设备,通过去保护、偶联、氧化/硫代和加帽,将核苷单体依次连接到寡核苷酸链的3'至5'方向。通过氨解将寡核苷酸链从固相支持物上切割下来,并去除保护基团。随后的纯化、超滤和冻干(如适用)产生单链寡核苷酸中间体。然后将所得的正义链和反义链以适当的比例退火(如适用)形成双链寡核苷酸(如适用),随后进行冻干(如适用)和包装以获得活性寡核苷酸药物成分。
寡核苷酸的生产应根据ICH Q9-Q11中概述的原则进行评估,特别关注固相合成过程中每个步骤的关键性。基于寡核苷酸制造和质量控制的平台赋能模块的可用性,应根据先前项目的经验和历史批次数据进行系统的风险评估。应基于寡核苷酸活性药物成分的质量目标产品概况,建立将关键质量属性与关键工艺参数相关联的风险管理策略,以制定适当的制造工艺质量控制策略。高级控制策略可能包括过程分析技术(离线、在线、在线)、由设备内传感器监测的工艺参数直接通知的直接控制、生产线和设施中设备操作的实时控制以及数据管理和风险预测。
4. 含连接子的寡核苷酸
AOCs的有效载荷是低细胞毒性的寡核苷酸。因此,寡核苷酸的合成和制造可以在具有标准防护设备的常规生产设施中进行。通常不需要使用通风柜动力空气净化呼吸器、高活性材料隔离策略和环境卫生监测程序。连接子通常通过使用相容的连接子和亚磷酰胺单体进行一步固相合成掺入寡核苷酸中。如果所需连接子的化学性质与固相合成条件不兼容,则使用固相和液相合成以两步法制备具有特定连接子的寡核苷酸。
5. AOC散装溶液制备
使用各种技术平台进行偶联反应,通过快速化学或酶促反应将寡核苷酸精确附着到修饰裸抗体上的反应位点。在此过程中,必须考虑裸抗体、连接子和有效载荷物理化学性质的差异,并严格优化关键工艺参数。有机溶剂的类型、小分子进料比例、pH、温度和裸抗体浓度直接影响反应效率,必须精细控制以最小化聚集和非特异性结合的形成。
鉴于AOCs的高度异质性,工艺开发应关注以下方面:(1)如果涉及还原,则选择抗体二硫键还原位点并控制还原程度;(2)偶联位点的特异性以及对缀合寡核苷酸的精确控制;(3)有效载荷分布的均匀性;(4)监测偶联过程中的杂质。对于定点缀合,必须基于潜在机制评估脱靶缀合的风险和副反应的发生率。对于酶促偶联,应验证与酶相关的安全风险,特别是散装溶液中的残留水平。
扩大生产时需要特别注意两个风险类别。首先,原材料投入过多可能导致副产物积累,需要进行风险评估,并结合下游纯化能力进行工艺优化。其次,必须通过逐步参数优化和过程监控来防止多步缀合反应中原材料比例不平衡或反应效率不足,例如偶联未负载连接子的抗体比例增加、次优OAR或残留有效载荷过多。
偶联后,应从AOC反应混合物中去除工艺相关和产品相关的杂质。工艺相关杂质包括残留的修饰试剂(如还原剂)、催化剂、酶、有机溶剂和其他外源性物质。产品相关杂质包括聚集体、抗体片段、游离小分子及其衍生物、副产物和其他内源性污染物。值得注意的是,在AOC生产过程中,可以通过纯化选择性去除特定组分,以精细控制OAR和有效载荷分布。因此,纯化技术的选择应以特定的纯化目标(例如杂质清除或产品属性优化)以及对生产过程中可能出现的杂质类型和水平的全面评估为指导。应建立有针对性的纯化策略并验证去除效率,以确保最终产品符合质量标准。
6. AOC制剂
AOC剂型和配方必须根据每个AOC的复杂性和独特特性量身定制。应进行全面研究,以确定适当的剂型,防止AOCs在储存期间在溶液中降解和聚集。
-03-
二、AOC的质量控制
AOCs具有抗体药物和寡核苷酸治疗药物的属性。鉴于AOC治疗药物独特的分子结构和作用机制,在建立质量标准时应考虑整体AOC分子(散装溶液和制剂)及其关键成分(裸抗体和寡核苷酸)。此外,质量控制策略应针对具体产品,并考虑设计原理和制造工艺。与ADCs类似,AOCs表现出复杂的结构、高异质性和多种多样的产品相关和工艺相关杂质。应根据抗体和寡核苷酸的质量属性以及与缀合工艺相关的因素来确定关键质量属性。应开发适当的技术和分析方法,以全面表征结构、物理化学性质、生物活性和杂质。对AOC中间体、散装溶液和制剂的关键质量属性的研究应基于以下章节提供的先前经验。
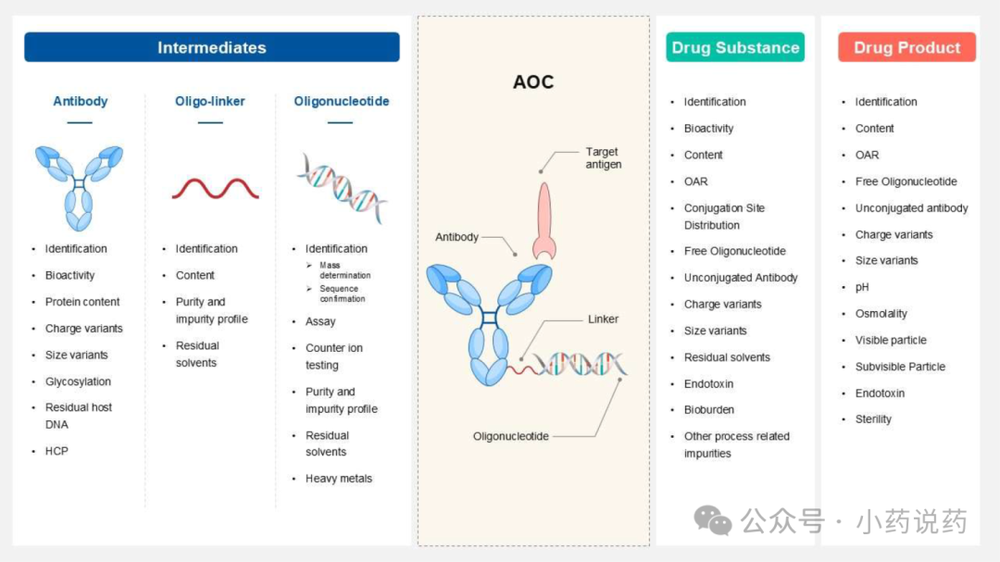
1. 中间体
AOCs中的寡核苷酸有效载荷大于ADCs中的小分子有效载荷,导致分子大小和电荷发生显著变化。ADCs中偶联分子的特性更像抗体而非小分子。然而,AOCs中的偶联物表现出双重特性,既像带正电荷的抗体,又像带负电荷的寡核苷酸。例如,ADC散装溶液放行阶段的质量控制属性,如大小变异杂质、电荷变异杂质和糖基化变异杂质,在AOC散装溶液放行阶段控制起来要困难得多。这种复杂性也适用于寡核苷酸中的核酸杂质。寡核苷酸的产品相关杂质通常包括N-1和N+1序列变异;裸抗体的引入显著复杂化了将这些杂质与AOCs分离的过程。因此,应在中间体放行阶段单独控制偶联工艺之前产生的杂质。
裸抗体:评估用于AOCs的裸抗体中间体的质量类似于评估抗体药物;但是,应考虑与偶联工艺相关的质量属性。例如,在采用半胱氨酸介导缀合的AOCs生产中,必须仔细监测裸抗体中半胱氨酸变体(例如具有二硫键和游离硫醇基团的半胱氨酸)的水平。用于AOCs的裸抗体可能是新分子或生物类似药,应具有明确的基因来源和背景信息。裸抗体生产细胞库的表征和稳定性评估必须符合《中华人民共和国药典》和ICH Q5A。此外,培养基和添加剂不应存在传染性海绵状脑病或牛海绵状脑病的风险。总体而言,可能影响最终产品安全性和有效性的质量属性应根据产品特有的特性进行适当控制。工艺相关杂质,包括宿主细胞DNA和蛋白质,应在中间体放行阶段控制,而不是在AOC散装溶液放行阶段。
寡核苷酸和含连接子的寡核苷酸:寡核苷酸生产通常采用固相合成。ICH Q6A明确指出,其范围不包括放射性药物、发酵产品、寡核苷酸、草药或源自动物和植物的粗制品,或寡核苷酸治疗药物。但是,一些测试项目和限度仍可使用本指南作为补充参考进行开发,包括外观、鉴别、含量测定和杂质。此外,美国食品药品监督管理局和欧洲药品管理局最近发布的寡核苷酸药物草案指南也可作为参考。
除了小分子化学药物或合成肽活性药物成分的标准质量评估外,固相合成寡核苷酸药物的质量评估应纳入针对其独特制造工艺、结构特征和物理化学性质的具体测试,包括序列验证和反离子含量分析。寡核苷酸中的产品相关杂质多样且结构复杂(例如N-1、N+1、不完全去保护和P=O),需要多种正交分析方法来控制。工艺相关杂质,包括残留试剂和小分子污染物,通常在寡核苷酸制造过程中完全去除。此外,遗传毒性杂质、残留溶剂和无机杂质的控制策略应与相关ICH指南保持一致。
含连接子的寡核苷酸的质量控制取决于合成路线,可分为两种情况。如果连接子是通过固相合成过程中使用专门的亚磷酰胺单体引入的,则可以使用标准寡核苷酸质量控制策略评估含连接子的中间体寡核苷酸。但是,如果连接子是通过与寡核苷酸中间体反应引入的,则应评估寡核苷酸和连接子偶联的寡核苷酸中间体。应评估含连接子的寡核苷酸在偶联过程中引入的杂质或反应副产物。例如,用马来酰亚胺基团修饰的寡核苷酸通常会发生缓慢水解,导致产生非反应性寡核苷酸-连接子副产物。此外,应控制在寡核苷酸-连接子偶联反应中使用的溶剂等工艺相关杂质。
与ASOs和PMOs不同,siRNA作为双链寡核苷酸,需要确保siRNA在寡核苷酸连接子偶联步骤和抗体缀合物制备步骤中的稳定性。通常,siRNA连接子的制备在抗体偶联物制备之前完成。策略1涉及首先制备寡核苷酸连接子偶联物,然后与互补链杂交。策略2涉及首先制备连接子siRNA的杂交,然后将连接子与带有连接子的siRNA偶联。无论采用何种策略,都需要确保siRNA在工艺步骤中的稳定性,并避免在高温和高pH下变性。对于siRNA纯度的检测,可以使用尺寸排阻色谱法和非变性离子对反相色谱法来控制双链和残留单链的纯度。应过量使用不含连接子的互补链,因为它不会在抗体缀合物制备步骤中引入AOC储备溶液,并且在工艺步骤中更容易去除。此外,对于偶联过程中产生的寡核苷酸或寡核苷酸-连接子降解产物,例如由马来酰亚胺水解形成的非反应性连接子-寡核苷酸杂质和反应性寡核苷酸脱硫杂质,一个可用的选择是使用反相色谱法,它提供增强的分辨率、变性离子对或变性离子交换色谱法。
2. AOC散装溶液
寡核苷酸-抗体比率(OAR):OAR定义为每个抗体分子缀合的寡核苷酸分子数。OAR决定了AOC的分子量和大小,并与AOC的物理化学性质密切相关,包括溶解度、亲和力和聚集。OAR直接影响产品的效力、安全性和药代动力学。因此,优化OAR可显著提高成本效益和制造效率。OAR必须在散装溶液制造过程中进行控制和监测,尤其是在偶联过程中。用于OAR的常见分析方法包括紫外-可见光谱法、强阴离子交换色谱法、毛细管区带电泳-质谱法、还原毛细管凝胶电泳法和尺寸排阻色谱-质谱法。ADCs的药物-抗体比率分析通常利用不同数量小分子有效载荷的疏水性差异。然而,对于AOCs,寡核苷酸的变化导致疏水性和与色谱固定相的二次相互作用差异最小。因此,使用疏水相互作用色谱法或反相液相色谱法分析AOCs的OAR具有挑战性。带负电荷的寡核苷酸通常会改变AOC分子的整体电荷。因此,可以采用能够区分电荷差异的分析方法来分析具有不同OAR的AOCs。Tian等人首次使用毛细管区带电泳-质谱法来表征和量化具有不同OAR值的AOCs。优化鞘流缓冲液和干燥气体条件显著提高了AOCs的电离和解吸效率,并通过调节背景电解质的pH实现了具有不同OAR的AOCs的分离。Cochran等人使用还原毛细管凝胶电泳分析了抗体缀合PMOs的OAR。使用还原毛细管凝胶电泳可以分离还原的轻链、缀合一个PMO的轻链、重链和缀合一个至五个PMO的重链,显著提高了OAR测定的准确性。此外,通过尺寸排阻色谱结合质谱分析AOCs中的OAR值与ADCs相比具有明显优势。ADCs中的药物分子通常分子量低于2 kDa。然而,寡核苷酸要大得多,通常超过10 kDa。因此,具有不同OAR值的AOCs之间的分子量差异非常明显。利用这一优势,Nagornov等人采用天然尺寸排阻色谱结合Orbitrap傅里叶变换质谱法分析了曲妥珠单抗-寡核苷酸偶联物的完整分子和亚基的OAR分布,并计算了平均OAR。将FTMS Booster X2数据采集系统与Q Exactive HF Orbitrap仪器用于傅里叶变换质谱,实现了简化的数据采集和处理。因此,在OAR分析之前不再需要纯化和去糖基化步骤,简化了药物开发流程。值得注意的是,基于质谱的方法往往会低估OAR,因为寡核苷酸的负电荷会显著降低正离子模式下高OAR分子的信号。因此,应使用正交技术(如强阴离子交换高效液相色谱法)补充基于质谱的OAR测定。
偶联位点分布和未偶联mAbs:AOCs的异质性反映在偶联寡核苷酸数量的变化和偶联的特定位点上,这会影响其效力和安全性。当前的AOC偶联策略,不包括离子相互作用和竞争性亲和力(例如生物素标记的寡核苷酸与抗体上亲和素之间的强相互作用),通常涉及通过赖氨酸或半胱氨酸残基进行化学偶联,从而导致产品异质性。应采用适当的分析方法,包括离子交换色谱法、尺寸排阻色谱法、毛细管电泳法和质谱法,来表征具有不同OAR的AOCs上的寡核苷酸分布。蛋白质工程和酶方法已成功应用于生产具有改善均一性和定点AOCs,这可能会减少缀合位点异质性带来的挑战。
以ADCs为例,液相色谱-质谱法是分析缀合位点的行业标准,因其高灵敏度、高分辨率和位点特异性分析。然而,使用这种方法分析AOCs中的偶联位点具有挑战性。寡核苷酸相对较大的分子量和负电荷会显著改变抗体的电荷,并可能主导AOC的净电荷。这些差异影响了检测模式(正离子或负离子模式)的选择,并增加了串联质谱中离子碎裂的难度,阻碍了偶联位点的准确识别。为了应对这些挑战,应引入样品制备步骤,去除寡核苷酸部分,以提高偶联水平的定量准确性和离子碎裂质量。去除寡核苷酸部分的常用方法包括酶消化(例如使用核酸酶P1或磷酸二酯酶I)将寡核苷酸消化成短核苷酸序列甚至单个核苷酸。酶消化对天然寡核苷酸和化学修饰的寡核苷酸都有效。该策略已成功应用于ADCs中偶联位点的识别和定量,显著提高了缀合位点的识别率和缀合水平的定量准确性。
对于非偶联抗体,使用强阴离子交换色谱法或尺寸排阻色谱法进行质量控制。在强阴离子交换中,通过带负电荷的分析物与固定相中带正电荷的季铵基团之间的静电相互作用实现保留。保留强度由目标分子上的负电荷决定。典型的洗脱顺序如下:非偶联抗体、具有不同OAR的AOCs(较高OAR洗脱较晚)和游离寡核苷酸。大多数非偶联抗体不携带负电荷。因此,它们倾向于不保留地流过,与其他组分(如AOCs)分离。然而,确保反应溶液和储存缓冲液在检测波长处没有特征吸收至关重要,因为这可能导致高估。值得注意的是,强阴离子交换色谱法不适用于中性电荷的寡核苷酸有效载荷(如PMOs);因此,应采用替代分析方法来分析这些有效载荷。基于尺寸排阻色谱的分离机制,洗脱顺序通常如下:具有不同OAR的AOCs(较高OAR洗脱较早)、非偶联抗体和游离寡核苷酸。尺寸排阻色谱法也可用于检测分子量与其他组分显著不同的非偶联抗体。偶联位点分布和非偶联mAbs的分析可以与OAR相关联,以提高产品质量控制的全面性。
生物活性:生物活性是产品质量和效力的关键指标。对于AOCs,应建立生物活性测定以反映体内药效学机制。这些测定是评估产品功能活性的基础。AOCs中的抗体与靶抗原结合,随后AOC-受体复合物内在化形成内体。连接子的裂解促进寡核苷酸从内体释放到细胞质中,在那里发挥其生物效应。应采用适当的分析方法,包括表面等离子体共振和酶联免疫吸附测定,来评估AOC与靶抗原的结合。应开发使用表达靶抗原的细胞系的基于细胞的测定来分析生物活性。可以根据评估靶细胞中小核酸药物效力的方法来评估AOC治疗药物的体外效力。应评估靶mRNAs、蛋白质、细胞表型和功能干扰。在选择生物活性测定时,应优先考虑变异性低、操作简单、可有效评估和质量控制的测定。
游离寡核苷酸:未与抗体偶联的寡核苷酸以多种形式存在,包括游离寡核苷酸和寡核苷酸-连接子复合物。游离寡核苷酸的毒性源于由于碱基互补配对而产生的杂交依赖性毒性;与杂交无关的毒性与其化学修饰、物理化学性质和递送载体有关。这些毒性可能导致血小板减少症、凝血抑制以及高暴露水平器官的毒性作用。可以通过基于其毒性和清除率建立适当的限度来控制游离寡核苷酸。此外,在稳定性研究期间,应注意有效载荷脱落的风险,这可以通过使用强阴离子交换色谱法和尺寸排阻色谱法监测AOC产品中游离寡核苷酸的水平来评估。
其他关键质量属性:
AOC和蛋白质浓度:应采用适当的物理、化学或免疫学方法来量化AOC产品。当使用分光光度法进行浓度测量时,必须考虑寡核苷酸在测量波长处对吸光度的潜在贡献。寡核苷酸在260 nm处表现出最大吸收,在计算AOC散装溶液或制剂的浓度时通常需要适当的校正因子。Cochran等人使用280 nm处的吸光度和药物-抗体比率1和2的消光系数确定了AOC浓度。蛋白质浓度也可以使用BCA测定等方法测量。评估裸抗体中间体、散装溶液和制剂的蛋白质含量,以确保产品稳定性和效率。
产品相关杂质:AOC散装溶液中的产品相关杂质包括由物理化学异质性产生的分子变异。应分离、识别和分析目标产物的分子变异。常见的产品相关杂质包括电荷变异、分子大小变异和降解产物。例如,在使用马来酰亚胺试剂修饰抗体期间,可能通过与邻近赖氨酸残基的反应形成非特异性分子内交联副产物。表现出与目标产品等效活性的变异包括产品相关物质。
对于在散装溶液生产或储存过程中由AOC降解产生的裸抗体或寡核苷酸杂质,应利用适当的预处理策略来最小化或消除分析此类杂质相关的挑战。例如,可以对AOC进行蛋白水解消化以分析siRNA或ASO,并应用寡核苷酸的磷酸二酯酶消化来分析抗体。这些策略涉及可能对产品质量分析构成风险的样品预处理步骤。因此,必须系统评估预处理对产品的影响,以避免将预处理引入的杂质误判为产品相关杂质或高估其水平。
工艺相关杂质:工艺相关杂质是在制造过程中引入的,包括由抗体和连接子缀合的寡核苷酸之间反应产生的杂质。这些杂质包括酶、有机试剂和元素杂质。应对这些杂质的残留水平进行彻底的安全风险评估,并应将具有潜在安全风险的残留杂质纳入质量控制标准。
3. 成品AOC产品
对于成品AOC产品的质量控制,应遵循药典标准,同时考虑具体产品类型和剂型。控制参数通常包括外观、pH、渗透压、可见异物、不溶性微粒、灌装体积和辅料含量。对于冻干形式,应控制复溶时间和水分含量。值得注意的是,化学修饰的寡核苷酸在储存过程中可能产生内源性可见颗粒。此外,抗体和寡核苷酸可以形成非共价复合物作为副产物,可能会沉淀。这些风险应在AOC制剂开发过程中仔细考虑,并实施主动监测策略。此外,应评估源自起始物料、散装溶液、中间体以及与产品接触的材料或设备的可提取物的风险。检测到的可提取物应根据ICH Q3E进行安全评估,以防止对产品安全产生任何不利影响。
-04-
结语
总而言之,AOCs的制造与质量控制是一个多学科交叉的复杂系统工程。从抗体的工程化改造、连接子的理性设计、寡核苷酸的化学合成,到最终的偶联、纯化及制剂,每一步都需要精细的工艺优化和严格的过程监控。建立稳健、可放大的生产工艺,并辅以能够全面表征其复杂结构和功能的质量控制方法,是AOC药物成功实现临床转化和商业化生产的基石。随着行业经验的积累和监管科学的进步,标准化的AOC生产与质控指南将应运而生,进一步推动这一新兴治疗平台的发展。
参考文献:
Advances in the pharmaceutical development of antibody-oligonucleotide conjugates.
Eur J Pharm Sci. 2025 Dec 1:215:107292.
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
