
2025年3月24日,比利时生物技术公司Augustine Therapeutics完成7770万欧元(约8480万美元)超额认购的A轮融资,由Novo Holdings和Jeito Capital领投,Asabys Partners、礼来、AdBio Partners、V - Bio Ventures、PMV、VIB、Gemma Frisius Fund、美国腓骨肌萎缩症(CMT)研究基金会和Newton Biocapital等现有投资者跟投。
此前公司已于2024年完成1700万欧元A轮首轮融资。本轮资金将用于推进其主要候选药物ACT-100216(外周限制性HDAC6抑制剂)在腓骨肌萎缩症(CMT)的1/2期概念验证临床试验,同时支持另外两个针对神经退行性疾病和心血管代谢疾病的HDAC6抑制剂项目研发。
01
以改变CMT患者命运为使命的研发团队
Augustine成立于2019年,专注于开发神经肌肉、神经退行性疾病和心代谢疾病新疗法,是VIB与比利时鲁汶大学VIB-KU Leuven癌症生物学中心联合孵化的分拆企业。
公司名称的灵感源自19世纪法国神经学家让-马丁·夏科(Jean-Martin Charcot)收治的一位特殊患者。这位患者所罹患的遗传性周围神经病变,经后世医学界系统研究后被正式命名为夏科-马里-图斯病(Charcot-Marie-Tooth disease,简称CMT)。
作为全球最常见的遗传性神经疾病之一,CMT又称遗传性运动感觉神经病,患病率约为1/2500,多在儿童至青年期发病。其核心病理特征为周围神经轴突或髓鞘的进行性退化,临床表现为肌肉萎缩无力、感觉丧失、剧烈疼痛及足部畸形等并发症。令人遗憾的是,这种严重影响生活质量的疾病至今尚无获批治疗方案。Augestine以该病命名,不仅是对医学先驱探索精神的致敬,更承载着改变患者命运的使命。
Augustine拥有经验丰富的生物制药领导者与资深科研团队,并且得到国际领先专家组成的顾问委员会的支持。首席执行官Gerhard Koenig博士深耕神经退行性疾病领域,曾创立Arkuda Therapeutics(治疗包括阿尔茨海默氏病和帕金森病在内的神经退行性疾病),还在拜耳、富达生物科学集团等历任要职。
首席医疗官Carl Bjartmar博士专攻神经肌肉,神经病学及肿瘤学适应症的临床开发,支持过多款罕见病新药研发,曾担任赛诺菲旗下Genzyme的高级医学总监。首席科学官Rie Schultz Hansen拥有20余年药物发现与早期药物开发经验,此前曾任Aelin Therapeutics的首席科学官,在基于诱导蛋白聚集的降解剂平台开发(用于中和致病蛋白)中发挥关键作用。
科学顾问团队由Ludo Van Den Bosch教授领衔,其突破性研究——“借选择性HDAC6抑制剂解决外周神经轴突变性机制”奠定了公司HDAC6抑制疗法的科学基础,联合创始人Clara campàs-moya与深耕医药创新20年的Bart De Taeye博士等携手,从技术研发到商业化路径为公司提供全方位支持,共同推进靶向HDAC6创新疗法开发落地。
02
发现HDAC6与运动神经元疾病关联,开发精准靶向小分子抑制剂
在运动神经元疾病(如肌萎缩侧索硬化症,ALS)和不同的神经病变(如腓骨肌萎缩症,CMT)的研究过程中,Van Den Bosch教授发现HDAC6在这些疾病的发生发展中扮演着关键角色。
HDAC6是一种Ⅱ类组蛋白脱乙酰酶,与其他HDAC不同,它主要位于细胞质中且可使非组蛋白脱乙酰化。通过这种方式,它调节各种细胞过程,包括细胞生长、细胞迁移、细胞内运输以及细胞死亡等。此外,HDAC6还可通过其泛素结合域在泛素化蛋白的清除中发挥作用。
在正常生理状态下,微管(microtubule)由α-微管蛋白(α-tubulin)和β-微管蛋白(β-tubulin)聚合而成,是细胞内物质运输的重要通道,维持着轴突运输的正常进行,保证神经细胞的营养供应和信号传导。
然而,在CMT、ALS等疾病中,HDAC6异常激活,过度去乙酰化α-微管蛋白,导致微管结构不稳定,完整性和连续性被破坏,进而使轴突运输功能受阻,神经细胞的营养供应和信号传导通路被破坏,最终造成神经细胞变性、功能丧失。
基于上述发现,Van Den Bosch教授提出利用选择性HDAC6抑制剂来干预疾病进程。通过抑制HDAC6的活性,能够阻止其对α-微管蛋白的过度去乙酰化,保护微管的乙酰化状态和结构稳定,从而恢复轴突运输功能,促进神经细胞的修复再生,延缓神经损伤,且外周靶向特性可减少对其他组织器官的潜在副作用。
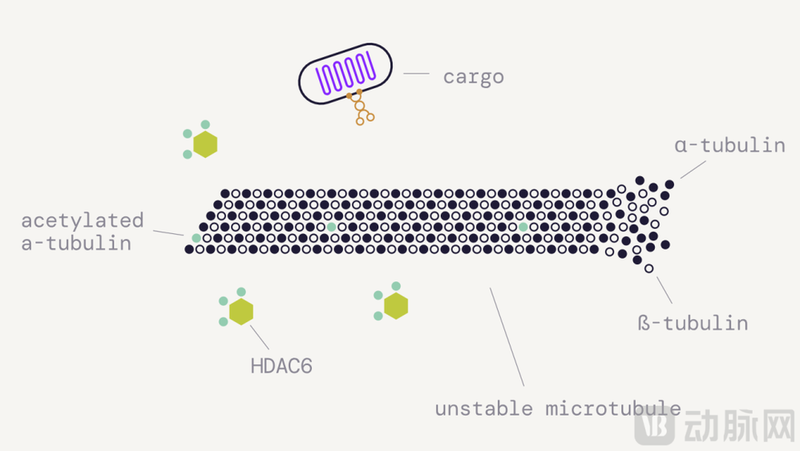
HDAC6对微管(microtubule)结构和功能的影响 来自:Augustine官网
03
围绕HDAC6靶点,聚焦三大疾病领域
Augustine的研发管线以HDAC6为核心靶点,构建覆盖周围神经病、中枢神经系统疾病和心脏代谢疾病三大领域的跨领域研发矩阵。
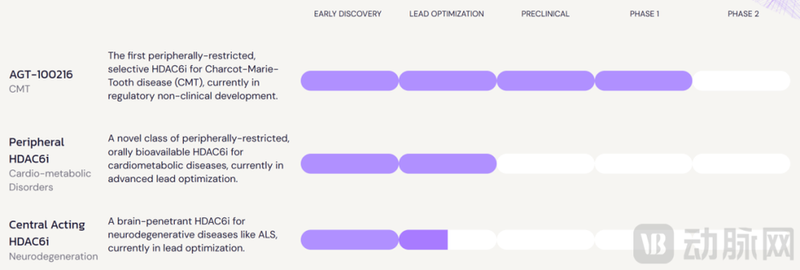
Augustine研发管线进程 来自:Augustine官网
● 周围神经病领域:CMT项目(AGT-100216)
临床前研究显示,HDAC6抑制剂可逆转CMT模型中的疾病进展。同时,对于化疗诱导周围神经病变(Chemotherapy-Induced Peripheral Neuropathy,CIPN),HDAC6抑制剂对CIPN不仅有稳健的治疗作用,还能在不损害化疗抗癌活性的前提下发挥预防作用。
针对上述特性,Augustine研发了AGT-100216——一款外周限制性、选择性小分子HDAC6抑制剂,具有独特的“非异羟肟酸(non-hydroxamic acid)、非酰肼(non-hydrazide)”化学结构,口服生物可利用,适用于慢性疾病的长期治疗。
目前,Augustine已启动针对CMT的Ⅰ期临床试验。该试验是一项随机、双盲、安慰剂对照的首次人体试验,旨在评估口服AGT-100216在健康成年志愿者中的安全性、耐受性、药代动力学和探索性药效学。
● 中枢神经系统疾病领域:神经退行性疾病药物(Central Acting HDAC6i)
基于Van Den Bosch教授的研究延伸,HDAC6异常激活在阿尔茨海默病(AD)、肌萎缩侧索硬化症(ALS)等中枢神经退行性疾病中同样扮演关键角色。其过度去乙酰化α-微管蛋白会破坏脑内神经元轴突运输,加剧β-淀粉样蛋白沉积(AD)或运动神经元变性(ALS)。
Augustine据此开发针对脑内神经元病理微环境设计的脑渗透型HDAC6抑制剂,旨在穿透血脑屏障(BBB)后选择性抑制中枢HDAC6,恢复神经元物质运输功能,以此突破外周药物无法作用于中枢的局限。
目前,该药物处于“先导优化期(lead optimization)”,需通过结构优化提升脑渗透效率、增强靶点选择性,为进入临床前研究(Preclinical)做准备。
● 心脏代谢疾病领域:心脏代谢疾病药物(Peripheral HDAC6i)
HDAC6在心肌细胞与脂肪细胞中高表达,其异常激活会通过两条路径驱动疾病:促进心肌细胞微管解聚,导致左心室舒张功能障碍(HFpEF);抑制胰岛素信号通路,加剧脂肪细胞胰岛素抵抗(2型糖尿病)。
基于此,Augustine同步开发外周限制性HDAC6抑制剂,聚焦心血管代谢疾病这两大病理环节,通过选择性抑制外周组织靶点,探索改善心血管功能、调节心脏代谢的新路径。
目前,该药物处于“先导优化后期(advanced lead optimization)”,后续将推进临床前研究及IND申报,逐步进入临床试验,潜在覆盖心力衰竭等心脏代谢疾病。
由此可看出,Augustine以HDAC6为单一靶点深度开发,系统性挖掘神经保护与代谢调节的跨疾病能力,有望为CMT、ALS等难治性疾病提供首个机制驱动的HDAC6靶向疗法,填补临床空白。
04
改善广谱抑制剂毒副作用,HDAC6靶向治疗赛道加速突破
目前,大部分已上市或临床中的HDAC抑制剂为泛HDACs抑制剂,对HDAC亚型并没有区分能力,存在潜在的毒副作用。而HDAC6作为HDAC家族最大的成员,是多种罕见病的潜在靶点,具有巨大潜力,因此众多药企纷纷布局HDAC6抑制剂领域,加速推进研发进程。
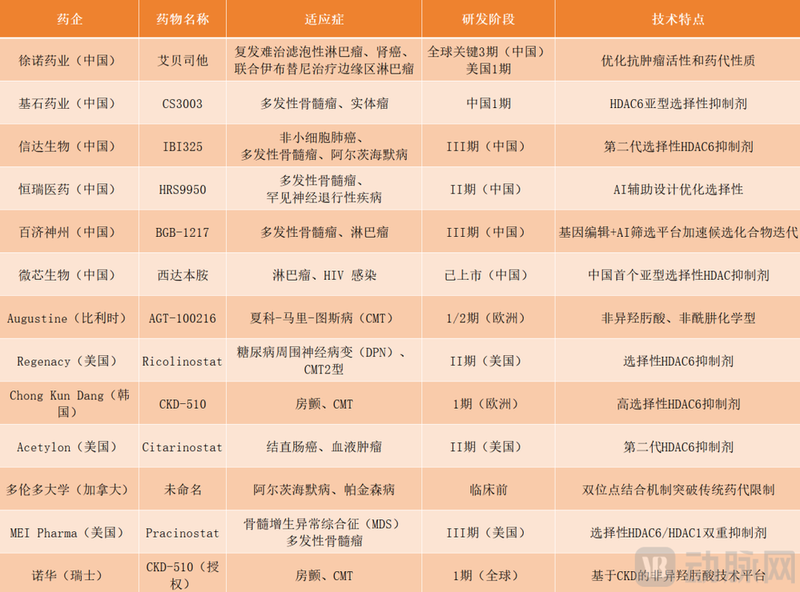
全球部分HDAC6在研管线盘点
国际方面,此前,诺华医药与韩国制药公司钟根堂(CKD)达成13亿美元合作协议,获得HDAC6抑制剂CKD-510除韩国以外的全球独家开发及商业化权利。CKD-510是一款高选择性靶向HDAC6的小分子抑制剂,2020年3月就获得了FDA授予的孤儿药资格认定。
除了诺华与CKD的合作外,国内还有多款靶向HDAC6的在研新药备受行业关注。如上海徐诺药业的艾贝司他,其涵盖不同肿瘤适应症,正在推进临床试验,全力推进药物从临床向商业化转化;中国药科大学朱雍&陆涛团队正在开发选择性抑制剂靶向HDAC6降解,用于治疗急性肝损伤。
如果您想对接文章中提到的项目,或您的项目想被动脉网报道,或者发布融资新闻,请与我们联系;也可加入动脉网行业社群,结交更多志同道合的好友。

近
期
推
荐



