
背景:
B7-H3是包括前列腺癌在内的多种实体瘤中一个具有前景的治疗靶点。本项多中心、开放标签、Ⅱ期临床研究旨在评估 HS-20093(GSK5764227)在转移性去势抵抗性前列腺癌(mCRPC)患者中的疗效与安全性。HS-20093 是一种新型靶向 B7-H3 的抗体–药物偶联物(ADC),其载荷为拓扑异构酶 I 抑制剂(注册号:NCT06001255)。
方法:
入组患者为至少接受过一线标准治疗后疾病进展者,给予 HS-20093 8.0 mg/kg 静脉输注,每 3 周一次。主要终点为基线存在靶病灶患者中,经 RECIST 1.1 及 PCWG3 标准评估的确认客观缓解率(cORR)。安全性及其他疗效终点在至少接受过 1 次 HS-20093 给药的患者中进行分析。
结果:
截至 2025 年 7 月 20 日,共入组 50 例中国成年患者,且均接受了至少 1 次 HS-20093 治疗。中位随访时间为 8.7 个月(范围:0.1–16.7 个月)。患者中位年龄为 68 岁(范围:49–79 岁),72.0% 的患者 ECOG 体能状态评分为 1 分。所有患者既往均接受过新型内分泌治疗,72.0% 曾接受过紫杉类化疗。既往治疗中位线数为 2 线(范围:1–8 线)。
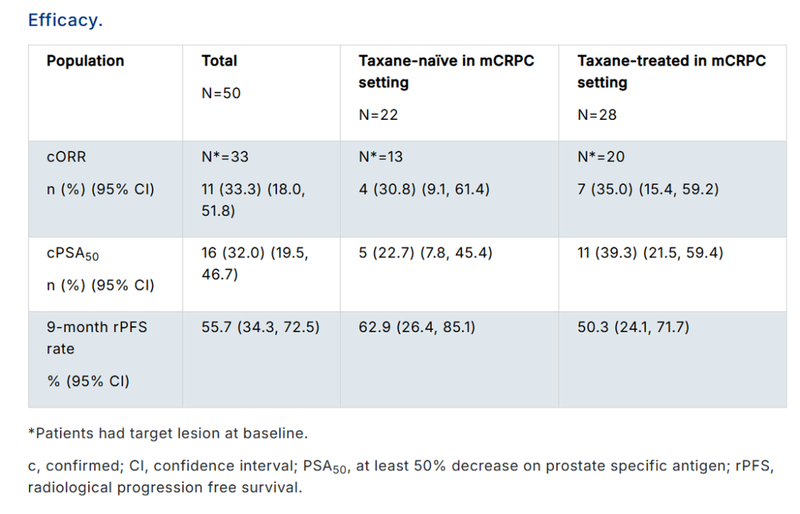
在 33 例基线存在靶病灶的患者中,cORR 为 33.3%(95% CI:18.0–51.8),疾病控制率(DCR)为 87.9%(95% CI:71.8–96.6)。中位缓解持续时间(DoR)尚未达到。共有 16 例患者前列腺特异性抗原(PSA)水平下降 ≥50%(PSA50),确认 PSA50 应答率为 32.0%。中位影像学无进展生存期(rPFS)尚未达到,9 个月 rPFS 率为 55.7%(95% CI:34.3–72.5)。在紫杉类初治及既往接受过紫杉类治疗的患者中,HS-20093 均显示出抗肿瘤活性(见表 1)。
共 49 例患者(98.0%)发生治疗相关不良事件(TRAEs),其中 ≥3 级不良事件占 54.0%,严重不良事件占 20.0%。最常见的 TRAEs 为血液学毒性和胃肠道毒性,与既往报道的安全性特征一致。另有 1 例 2 级间质性肺疾病事件。
结论:
在 mCRPC 患者中,HS-20093 单药治疗显示出令人鼓舞的抗肿瘤活性,且总体耐受性良好,安全性可控。
公众号已建立“小药说药专业交流群”微信行业交流群以及读者交流群,扫描下方小编二维码加入,入行业群请主动告知姓名、工作单位和职务。
